Topné Křivky
Obrázek \(\PageIndex{3}\) zobrazuje topné křivky, graf teplota versus čas vytápění, pro 75 g vzorku vody. Vzorek je zpočátku LED při 1 atm a -23°C; jak se přidává teplo, teplota ledu se lineárně zvyšuje s časem. Sklon přímky závisí na hmotnosti ledu a měrné teplo (Cs) led, což je počet joulů potřebné ke zvýšení teploty 1 g ledu o 1°C. Jak se teplota ledu zvyšuje, molekuly vody v ledovém krystalu absorbují stále více energie a intenzivněji vibrují. V bodě tání mají dostatek kinetické energie k překonání atraktivních sil a pohybu vůči sobě navzájem. Jak se přidává více tepla, teplota systému se dále nezvyšuje, ale zůstává konstantní při 0°C, dokud se veškerý led neroztaví. Jakmile je veškerý led přeměněn na kapalnou vodu, teplota vody se opět začne zvyšovat. Nyní se však teplota zvyšuje pomaleji než dříve, protože měrná tepelná kapacita vody je větší než u ledu. Když teplota vody dosáhne 100°C, voda začne vařit. I zde zůstává teplota konstantní při 100°C, dokud nebude veškerá voda přeměněna na páru. V tomto okamžiku, teplota opět začne stoupat, ale rychlejším tempem než v jiných fázích, protože tepelná kapacita páry je menší než u ledu nebo vody.
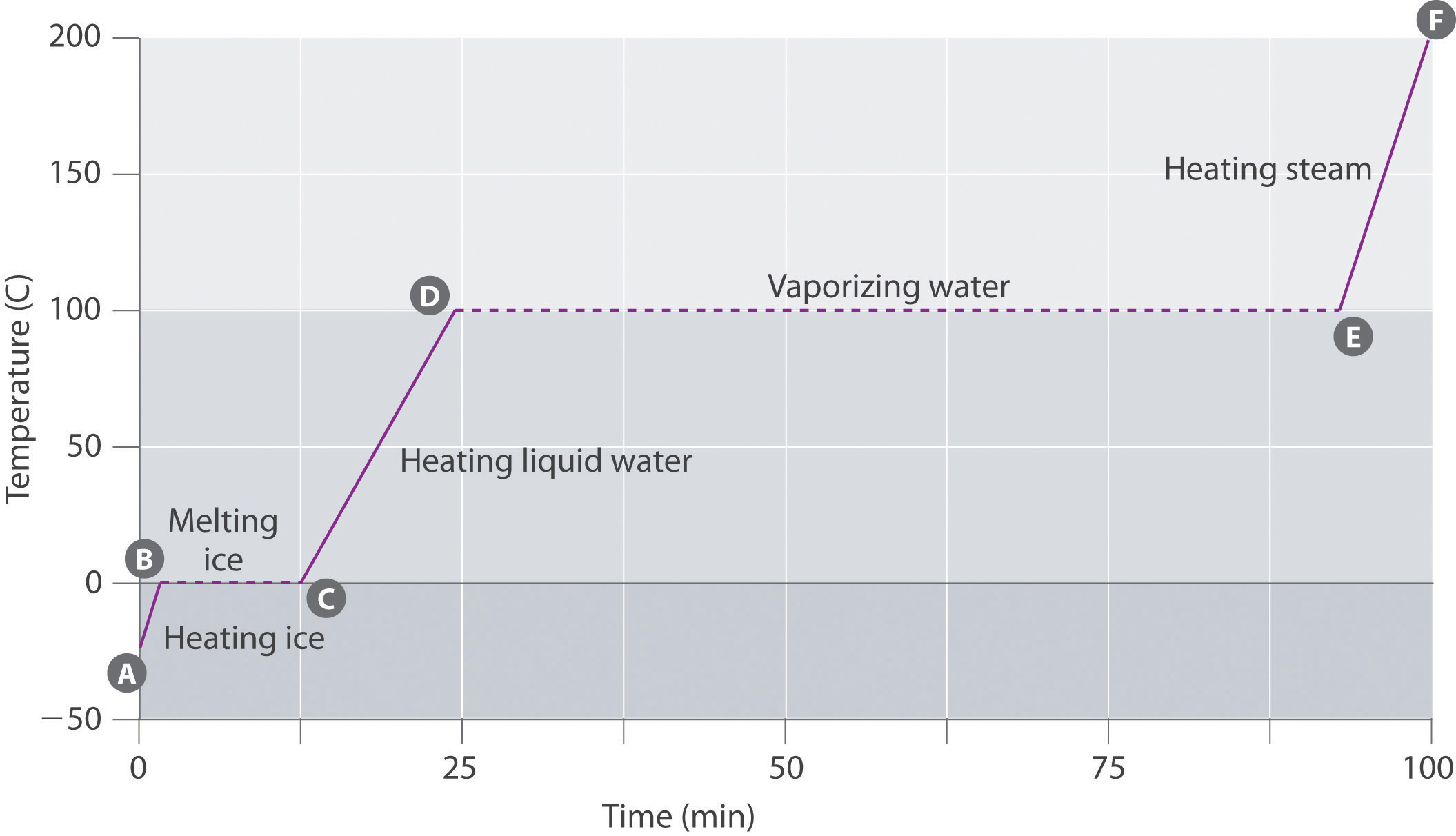
teplota systému se tedy během změny fáze nemění. V tomto příkladu, tak dlouho, jak i malé množství ledu je přítomen, teplota soustavy zůstává na 0°C během tavení, a tak dlouho, jak i malé množství tekuté vody, teplota soustavy zůstává při 100°C během procesu varu. Rychlost, při které je teplo dodané nemá vliv teploty led/voda nebo voda/pára směs, protože přidané teplo je používán výhradně k překonání přitažlivé síly, které drží více kondenzované fáze spolu. Mnoho kuchařů si myslí, že jídlo bude vařit rychleji, pokud se teplo zvýší, takže voda rychleji vaří. Místo toho se hrnec vody vaří do sucha dříve, ale teplota vody nezávisí na tom, jak energicky se vaří.
teplota vzorku se během změny fáze nemění.
Když je teplo dodané při konstantní rychlosti, jako na Obrázku \(\PageIndex{3}\), pak délka vodorovné čáry, které představuje čas, během něhož teplota nemění, je přímo úměrná velikosti enthalpies spojena s fází změny. Na obrázku \(\PageIndex{3}\) je vodorovná čára při 100°C mnohem delší než čára při 0°C, protože entalpie odpařování vody je několikrát větší než entalpie fúze.
přehřátá kapalina je vzorek kapaliny při teplotě a tlaku, při kterém by měl být plyn. Přehřáté kapaliny nejsou stabilní; kapalina se nakonec vaří, někdy násilně. Fenomén přehřívání způsobuje „nárazy“, když se kapalina zahřívá v laboratoři. Když se například zkumavka obsahující vodu zahřívá nad bunsenovým hořákem, může se jedna část kapaliny snadno zahřát. Když se přehřátá kapalina přemění na plyn, může vytlačit nebo“ narazit “ zbytek kapaliny ze zkumavky. Umístění míchací tyč nebo malý kousek keramiky („boiling chip“) ve zkumavce umožňuje bubliny páry se tvoří na povrchu objektu, takže kapalina vaří místo stává přehřátou. Přehřátí je důvod, proč kapalina zahřívá v hladké pohár v mikrovlnné troubě nemusí vařit, dokud pohár je dojat, když pohyb šálku umožňuje bubliny tvořit.