jako příklad izobarického procesu lze použít reverzibilní expanzi ideálního plynu. Zvláště zajímavý je způsob přeměny tepla na práci, když se expanze provádí při různých pracovních tlacích plynu / okolního plynu.
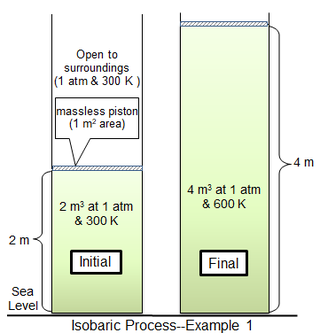
V prvním procesu příklad, válcová komora 1 m2 uzavírá 81.2438 mol ideálního dvouatomová molekula, plyn molekulární hmotnost 29 g mol−1 při 300 K. Okolní plyn je při 1 atm a 300 K a oddělen od plynného válce tenkým pístem. Pro omezující případ bezhmotného pístu je plyn válce také při tlaku 1 atm, s počátečním objemem 2 m3. Teplo se přidává pomalu, dokud teplota plynu není rovnoměrně 600 K, poté je objem plynu 4 m3 a píst je 2 m nad svou počáteční polohou. Pokud je pohyb pístu dostatečně pomalý, bude mít tlak plynu v každém okamžiku prakticky stejnou hodnotu (psys = 1 atm).
Pro tepelně perfektní dvouatomová molekula plynu, molární měrná tepelná kapacita při konstantním tlaku (cp) 7/2R nebo 29.1006 J mol−1 deg−1. Molární tepelná kapacita při konstantním objemu (cv) je 5/2R nebo 20.7862 J mol−1 deg−1. Poměr γ {\displaystyle \ gamma }

obou tepelných kapacit je 1,4.
teplo Q potřebné k přivést plyn od 300 do 600 K, je,
Q = Δ H = n c p Δ T = 81.2438 × 29.1006 × 300 = 709 , 274 J {\displaystyle Q={\Delta \mathrm {H} }=n\,c_{p}\,\Delta, \mathrm {T} =81.2438\times 29.1006\times 300=709,274{\text{ J}}}

.
zvýšení vnitřní energie je
Δ U = n c v Δ T = 81.2438 × 20.7862 × 300 = 506 , 625 J {\displaystyle \Delta \ U=n\,c_{v}\,\Delta, \mathrm {T} =81.2438\times 20.7862\times 300=506,625{\text{ J}}}

Proto, W = Q − Δ U = 202 , 649 J = n R Δ T {\displaystyle W=Q-\Delta U=202,649{\text{ J}}=nR\Delta \mathrm {T} }

W = p Δ ν = 1 atm × 2 m3 × 101325 Pa = 202 , 650 J {\displaystyle T={p\Delta \nu }=1~{\text{atm}}\times 2{\text{m3}}\times 101325{\text{Pa}}=202,650{\text{ J}}}

, což je samozřejmě totožné s rozdílem mezi ΔH a ΔU.
zde je práce zcela spotřebována expanzí proti okolí. Z celkového aplikovaného tepla (709,3 kJ) je vykonaná práce (202,7 kJ) asi 28,6% dodávaného tepla.

druhý příklad procesu je podobný prvnímu, s výjimkou toho, že bezhmotný píst je nahrazen pístem o hmotnosti 10,332.2 kg, což zdvojnásobuje tlak plynného válce na 2 atm. Objem plynného válce je pak 1 m3 při počáteční teplotě 300 K. Teplo se přidává pomalu, dokud teplota plynu není rovnoměrně 600 K, poté je objem plynu 2 m3 a píst je 1 m nad svou počáteční polohou. Pokud je pohyb pístu dostatečně pomalý, bude mít tlak plynu v každém okamžiku prakticky stejnou hodnotu (psys = 2 atm).
Od entalpie a vnitřní energie jsou nezávislé na tlaku,
Q = Δ H = 709 , 274 J {\displaystyle Q={\Delta \mathrm {H} }=709,274{\text{ J}}}

a Δ U = 506 , 625 J {\displaystyle \Delta U=506,625{\text{ J}}}

. W = p Δ V = 2 atm × 1 m3 × 101325 Pa = 202 , 650 J {\displaystyle T={p\Delta V}=2~{\text{atm}}\times 1~{\text{m3}}\times 101325{\text{Pa}}=202,650{\text{ J}}}

stejně Jako v prvním příkladu, o 28,6% dodaného tepla se přemění na práci. Ale tady, v práci je aplikován dvěma různými způsoby: jednak rozšiřuje okolní atmosféry a částečně zvedání 10,332.2 kg vzdálenost h 1 m.
W l i f t = 10 332.2 kg × 9.80665 m/s2 × 1 m = 101 , 324 J {\displaystyle W_{\rm {výtah}}=10\,332.2~{\text{kg}}\times 9.80665~{\text{m/s2}}\times 1{\text{m}}=101,324{\text{ J}}}

to Znamená, že polovina práce výtahy pístu hmotnost (fungovat gravitace, nebo „použitelné“ práce), zatímco druhá polovina se rozšiřuje do okolí.
výsledky těchto dvou příkladů procesu ilustrují rozdíl mezi podílem tepla převedeného na použitelnou práci (mgΔh) vs. frakce se přeměnila na práci s tlakem a objemem proti okolní atmosféře. Použitelná práce se blíží nule, protože pracovní tlak plynu se blíží tlaku okolí, zatímco maximální použitelná práce se dosáhne, když není okolní tlak plynu. Poměr všech provedených prací na tepelném příkonu pro ideální plyn izobarický expanze je
W Q = n R Δ T n c p Δ T = 2 5 {\displaystyle {\frac {W}{Q}}={\frac {nR\Delta \mathrm {T} }{nc_{p}\Delta \mathrm {T} }}={\frac {2}{5}}}
