Většina bakteriální infekce mohou být léčeny antibiotiky, jako je penicilin, objevené před několika desítkami let. Takové léky jsou však zbytečné proti virovým infekcím, včetně chřipky, běžného nachlazení a smrtelných hemoragických horeček, jako je Ebola.
Nyní, v rozvoji, který by mohl proměnit jak virové infekce se léčí, tým výzkumníků z MIT Lincoln Laboratory navrhl lék, který může identifikovat buňky, které byly napadeny jakéhokoli typu viru, pak zabít ty buňky, ukončit infekce.
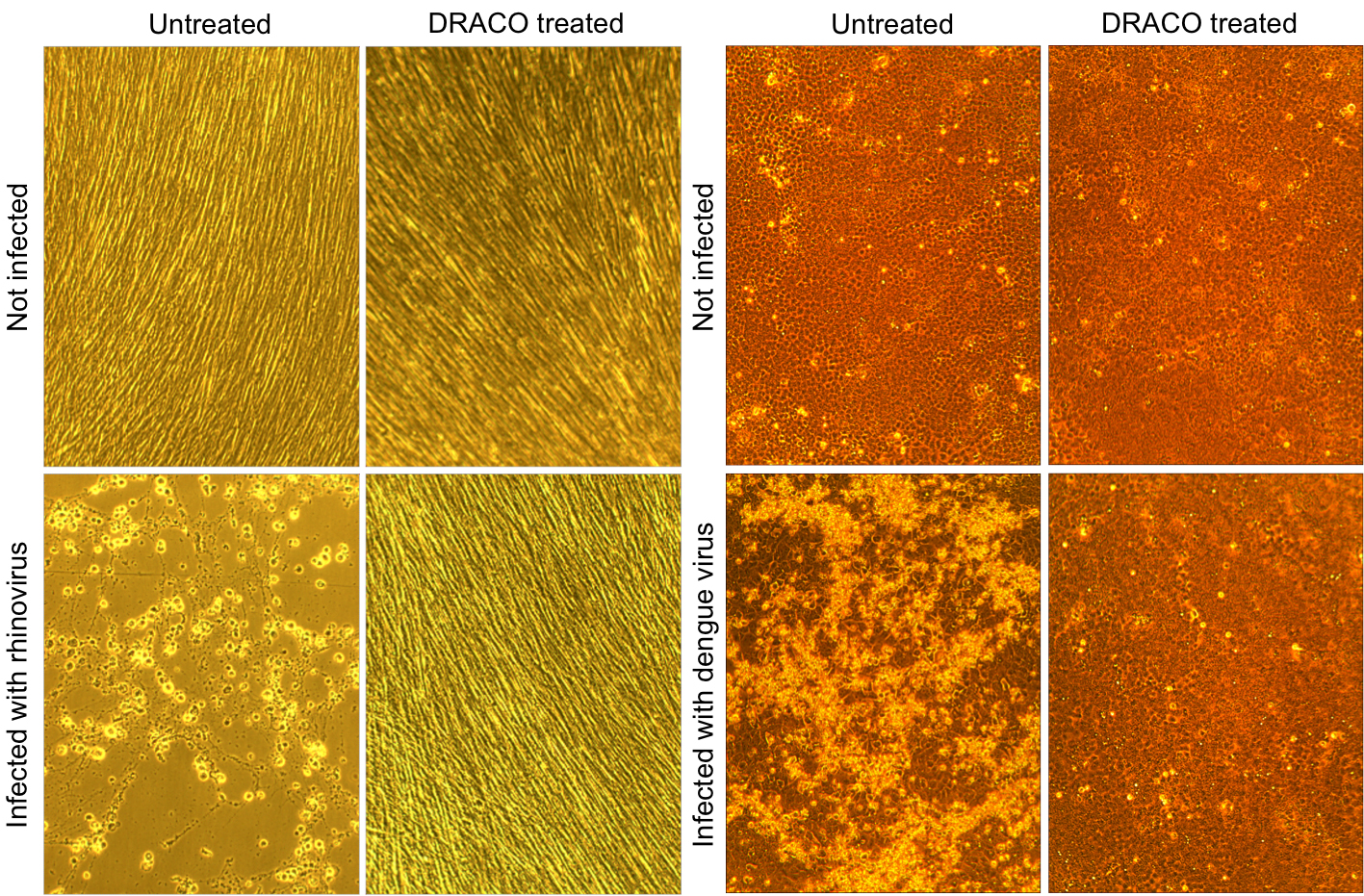
obrázky mikroskopu výše ukazují, že DRACO úspěšně léčí virové infekce. V levé sadě čtyř fotografií rhinovirus (virus běžného nachlazení) zabíjí neošetřené lidské buňky (vlevo dole), zatímco DRACO nemá toxicitu v neinfikovaných buňkách (vpravo nahoře) a léčí infikovanou buněčnou populaci (vpravo dole). Podobně v pravé sadě čtyř fotografií virus hemoragické horečky dengue zabíjí neošetřené opičí buňky (vlevo dole), zatímco DRACO nemá toxicitu v neinfikovaných buňkách (vpravo nahoře) a léčí infikovanou buněčnou populaci (vpravo dole). | Zvětšení obrázku
V článku publikovaném 27. července v časopise PLoS One, výzkumníci testovali jejich lék proti 15 viry, a zjistil, že je účinný proti všem z nich — včetně rhinovirů, které způsobují nachlazení, chřipky H1N1, žaludeční virus, virus dětské obrny, horečka dengue a některé další typy hemoragické horečky.
lék působí tak, že cílí na typ RNA produkovaný pouze v buňkách, které byly infikovány viry. „Teoreticky by to mělo fungovat proti všem virům,“ říká Todd Jezdec, vedoucí pracovníci vědec v Lincolnově Laboratoři Chemické, Biologické a Nano Technologies Group, který vynalezl nové technologie.
, Protože technologie je tak širokospektrální, to může také být použit v boji proti vypuknutí nové viry, jako v roce 2003 SARS (těžký akutní respirační syndrom) ohnisko, říká Jezdec.
dalšími členy výzkumného týmu jsou zaměstnanci Lincoln Lab Scott Wick, Christina Zook, Tara Boettcher, Jennifer Pancoast a Benjamin Zusman.
Několika antivirotik k dispozici
Jezdec měl nápad, že se rozvíjí široké spektrum protivirové terapie asi před 11 lety, po vymýšlení CANARY (Buněčné Analýzy a Oznamování Antigen Rizika a Výnosy), biosenzor, které mohou rychle identifikovat patogeny. „Pokud zjistíte patogenní bakterie v prostředí, pravděpodobně existuje antibiotikum, které by mohlo být použito k léčbě někoho, kdo je tomu vystaven, ale uvědomil jsem si, že existuje jen velmi málo léčby virů,“ říká.
Existuje několik léky, které boj proti specifické viry, jako jsou inhibitory proteázy používané ke kontrole HIV infekce, ale ty jsou poměrně málo početné a vnímavé k virové rezistenci.
Rider čerpal inspiraci pro své terapeutické látky, nazvané DRACOs (dvouvláknové RNA aktivované Kaspázové Oligomerizátory), z vlastních obranných systémů živých buněk.
když viry infikují buňku, přebírají její buněčné stroje pro svůj vlastní účel — to znamená, že vytvářejí více kopií viru. Během tohoto procesu viry vytvářejí dlouhé řetězce dvouvláknové RNA (dsRNA), která se nenachází v lidských nebo jiných živočišných buňkách.
Jako součást jejich přirozené obrany proti virové infekci, lidské buňky mají proteiny, které se přilepí na dsRNA, spustil kaskádu reakcí, která zabraňuje replikaci viru sám. Mnoho virů však může tento systém překonat blokováním jednoho z kroků dále po kaskádě.
Jezdec měl nápad spojit dsRNA vázající protein s další protein, který indukuje buňky podstupují apoptózu (programovanou buněčnou sebevraždu) — zahájila, například, když buňka určuje, že je na cestě, aby se stal rakovinné. Proto, když se jeden konec Draca váže na dsRNA, signalizuje druhý konec Draca, aby zahájil buněčnou sebevraždu.
kombinace těchto dvou prvků je „skvělý nápad“ a velmi nový přístup, říká Karla Kirkegaard, profesorka mikrobiologie a imunologie na Stanfordské univerzitě. „Viry jsou docela dobré v rozvoji rezistence vůči věcem, které se proti nim snažíme, ale v tomto případě je těžké vymyslet jednoduchou cestu k rezistenci na léky,“ říká.
Každý DRACO také zahrnuje „dodávka tag,“ odebraných z přirozeně se vyskytujících bílkovin, který umožňuje, aby přes buněčné membrány a zadejte jakékoli lidské nebo zvířecí buňky. Pokud však není přítomna žádná dsRNA, Draco opustí buňku nezraněnou.
většina testů hlášených v této studii byla provedena v lidských a zvířecích buňkách kultivovaných v laboratoři, ale vědci také testovali DRACO u myší infikovaných virem chřipky H1N1. Když byly myši léčeny přípravkem DRACO, byly z infekce zcela vyléčeny. Testy také ukázaly, že DRACO samo o sobě není pro myši toxické.
vědci nyní testují DRACO proti více virům u myší a začínají získávat slibné výsledky. Rider říká, že doufá, že licenci na technologii pro pokusy u větších zvířat a pro případné klinických studiích u lidí.
Tato práce je financována grantem z Národního Institutu pro Alergie a Infekční Choroby a New England Regional Center of Excellence pro Biodefense a Vznikajících Infekčních Onemocnění, s předchozí financování z Defense Advanced Research Projects Agency, Obrany Omezení hrozeb Agentura, a Ředitel Obranného Výzkumu & Engineering (nyní náměstek Ministra Obrany pro Výzkum a Inženýrství).