læringsmål
Ved udgangen af dette afsnit vil du være i stand til at:
- Forklar processerne for glycolyse
- beskriv vejen for et pyruvatmolekyle gennem Krebs-cyklussen
- Forklar transporten af elektroner gennem elektrontransportkæden
- beskriv processen med ATP-produktion gennem oksidativ phosphorylering
- Opsummer processen med glukoneogenese
kulhydrater er organiske molekyler sammensat af kulstof -, brint-og iltatomer. Familien af kulhydrater omfatter både enkle og komplekse sukkerarter. Glukose og fruktose er eksempler på simple sukkerarter, og stivelse, glykogen og cellulose er alle eksempler på komplekse sukkerarter. De komplekse sukkerarter kaldes også polysaccharider og er lavet af flere monosaccharidmolekyler. Polysaccharider tjener som energilagring (f.eks. stivelse og glykogen) og som strukturelle komponenter (f. eks. chitin i insekter og cellulose i planter).
under fordøjelsen opdeles kulhydrater i enkle, opløselige sukkerarter, der kan transporteres over tarmvæggen ind i kredsløbssystemet, der skal transporteres gennem hele kroppen. Kulhydratfordøjelsen begynder i munden med virkningen af spytamylase på stivelse og slutter med, at monosaccharider absorberes over tyndtarmens epitel. Når de absorberede monosaccharider transporteres til vævene, begynder processen med cellulær respiration (Figur 1). Dette afsnit vil først fokusere på glykolyse, en proces, hvor monosaccharidglukosen iltes og frigiver den energi, der er lagret i dens bindinger for at producere ATP.
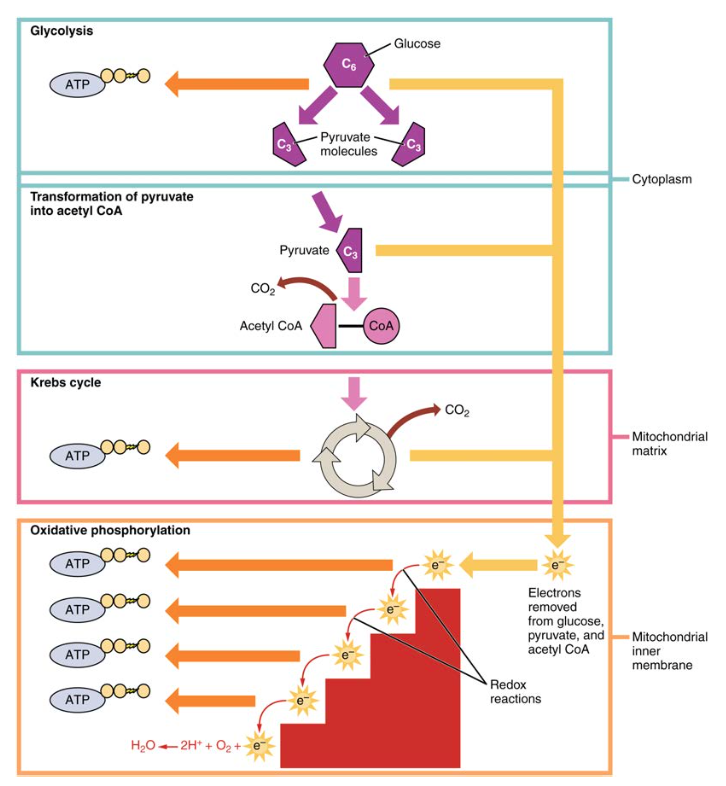
Figur 1. Cellulær respiration ilter glukosemolekyler gennem glykolyse, Krebs-cyklussen og iltning af phosphorylering for at producere ATP.
glykolyse
glukose er kroppens mest tilgængelige energikilde. Efter fordøjelsesprocesserne bryder polysaccharider ned i monosaccharider, herunder glucose, transporteres monosacchariderne over tyndtarmens væg og ind i kredsløbssystemet, som transporterer dem til leveren. I leveren passerer hepatocytter enten glukosen gennem kredsløbssystemet eller opbevarer overskydende glukose som glykogen. Celler i kroppen optager den cirkulerende glukose som reaktion på insulin og overfører gennem en række reaktioner kaldet glykolyse noget af energien i glukose til ADP for at danne ATP (figur 2). Det sidste trin i glykolyse producerer produktet pyruvat.glycolyse begynder med phosphorylering af glucose geksokinase til dannelse af glucose-6-phosphat. Dette trin bruger en ATP, som er donoren af fosfatgruppen. Under virkningen af phosphofructokinase omdannes glucose-6-phosphat til fructose-6-phosphat. På dette tidspunkt donerer en anden ATP sin fosfatgruppe, der danner fructose-1,6-bisphosphat. Denne seks-carbon sukker er opdelt til dannelse af to phosphorylerede tre-carbon molekyler, glyceraldehyd-3-phosphat og dihydroksyacetonphosphat, som begge omdannes til glyceraldehyd-3-phosphat. Glyceraldehyd-3-phosphatet phosphoryleres yderligere med grupper doneret af dihydrogenphosphat til stede i cellen til dannelse af tre-carbonmolekylet 1,3-bisphosphoglycerat. Energien i denne reaktion kommer fra iltningen af (fjernelse af elektroner fra) glyceraldehyd-3-phosphat. I en række reaktioner, der fører til pyruvat, overføres de to fosfatgrupper derefter til to ADP ‘er for at danne to ATP’ er. Således bruger glycolyse to ATP ‘er, men genererer fire ATP’ er, hvilket giver en nettogevinst på to ATP ‘ er og to molekyler pyruvat. I nærvær af ilt fortsætter pyruvat videre til Krebs-cyklussen (også kaldet citronsyrecyklus eller TCA), hvor yderligere energi ekstraheres og overføres.
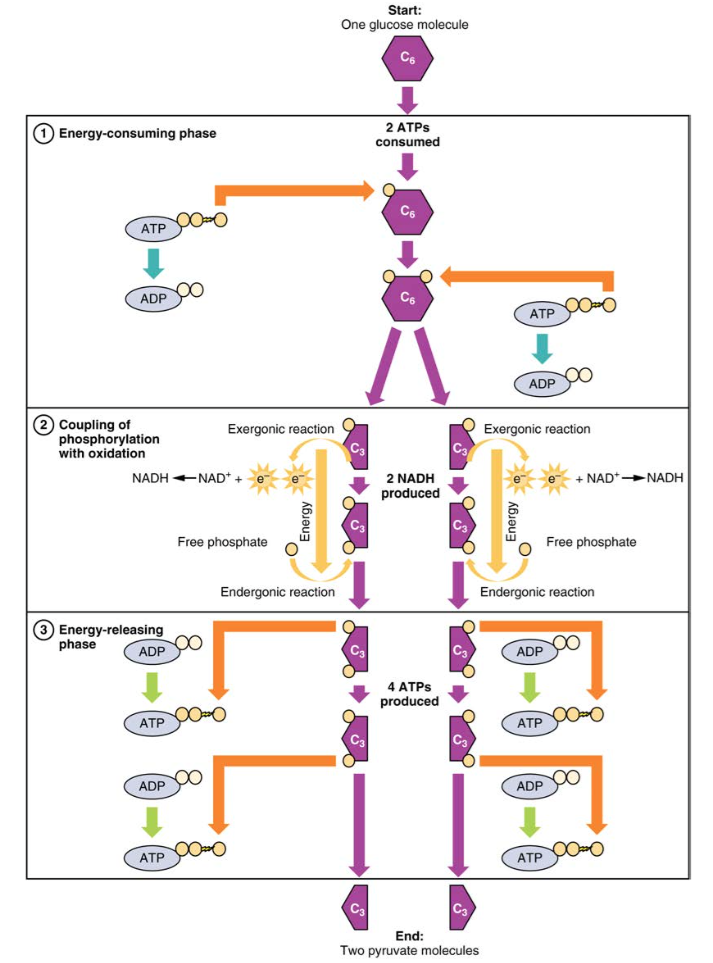
figur 2. Under den energiforbrugende fase af glycolyse forbruges to ATP ‘ er, der overfører to fosfater til glucosemolekylet. Glukosemolekylet opdeles derefter i to tre-carbonforbindelser, der hver indeholder et phosphat. I anden fase tilsættes et yderligere phosphat til hver af de tre carbonforbindelser. Energien til denne endergoniske reaktion tilvejebringes ved fjernelse (iltning) af to elektroner fra hver tre-carbonforbindelse. Under den energifrigivende fase fjernes fosfaterne fra begge tre-carbonforbindelser og bruges til at producere fire ATP-molekyler.
se denne video for at lære om glykolyse:
glykolyse kan opdeles i to faser: energiforbrugende (også kaldet kemisk priming) og energigivende. Den første fase er den energiforbrugende fase, så det kræver to ATP-molekyler for at starte reaktionen for hvert glukosemolekyle. Imidlertid producerer slutningen af reaktionen fire ATP ‘ er, hvilket resulterer i en nettogevinst på to ATP-energimolekyler.
glykolyse kan udtrykkes som følgende ligning:
\text{Glucose}+2\text{ATP}+2\text{NAD}^{+}+4\text{ADP}+2\text{P}_{i}\to\text{Pyruvate}+4\text{ATP}+2\text{NADH}+2\text{H}^{+}
denne ligning angiver, at glukose i kombination med ATP (energikilden), NAD+ (et coensym, der tjener som en elektronacceptor) og uorganisk fosfat nedbrydes i to pyruvatmolekyler, der genererer fire ATP—molekyler—til et nettoudbytte på to ATP-og to energiholdige NADH-coensymer. NADH, der produceres i denne proces, vil blive brugt senere til at producere ATP i mitokondrier. Det er vigtigt, at ved afslutningen af denne proces genererer et glukosemolekyle to pyruvatmolekyler, to højenergi-ATP-molekyler og to elektronbærende NADH-molekyler.følgende diskussioner af glykolyse omfatter de reaktioner, der er ansvarlige for reaktionerne. Når glukose kommer ind i en celle, tilføjer glucokinase (eller glucokinase i leveren) hurtigt et fosfat for at omdanne det til glucose-6-phosphat. En kinase er en type, der tilføjer et fosfatmolekyle til et substrat (i dette tilfælde glucose, men det kan også være tilfældet for andre molekyler). Dette konverteringstrin kræver en ATP og fælder i det væsentlige glukosen i cellen og forhindrer den i at passere tilbage gennem plasmamembranen, hvilket tillader glykolyse at fortsætte. Det fungerer også til at opretholde en koncentrationsgradient med højere glukoseniveauer i blodet end i vævene. Ved at etablere denne koncentrationsgradient vil glukosen i blodet kunne strømme fra et område med høj koncentration (blodet) til et område med lav koncentration (vævene), der enten skal bruges eller opbevares. Geksokinase findes i næsten alle væv i kroppen. Glucokinase udtrykkes derimod i væv, der er aktive, når blodsukkerniveauet er højt, såsom leveren. Glucokinase har en højere affinitet for glucose end glucokinase og er derfor i stand til at omdanne glucose hurtigere end glucokinase. Dette er vigtigt, når glukoseniveauerne er meget lave i kroppen, da det tillader glukose at rejse fortrinsvis til de væv, der kræver det mere.i det næste trin i den første fase af glycolyse omdanner glucose-6-phosphatisomerasen glucose-6-phosphat til fructose-6-phosphat. Ligesom glukose er fruktose også et seks kulstofholdigt sukker. Fosfofructokinase-1 tilføjer derefter endnu et fosfat til at omdanne fructose-6-phosphat til fructose-1-6-bisphosphat, et andet seks-carbon sukker, ved hjælp af et andet ATP-molekyle. Aldolase nedbryder derefter denne fructose-1-6-der er to molekyler, der består af tre carbonhydrider, glyceraldehyd-3-phosphat og dihydroksyacetonphosphat. Derefter omdannes diosefosfatphosphat til et andet glyceraldehyd-3-phosphatmolekyle. Derfor er et glukosemolekyle ved afslutningen af denne kemiske priming eller energiforbrugende fase opdelt i to glyceraldehyd – 3-phosphatmolekyler.
den anden fase af glykolyse, den energibesparende fase, skaber den energi, der er produktet af glykolyse. Glyceraldehyd-3-phosphatdehydrogenase omdanner hvert tre-carbon glyceraldehyd-3-phosphat produceret i den
energiforbrugende fase til 1,3-bisphosphoglycerat. Denne reaktion frigiver en elektron, der derefter afhentes af NAD+ for at skabe et NADH-molekyle. NADH er et højenergimolekyle, som ATP, men i modsætning til ATP bruges det ikke som energivaluta af cellen. Fordi der er to glyceraldehyd-3-phosphatmolekyler, syntetiseres to NADH-molekyler under dette trin. Hvert 1,3-bisphosphoglycerat dephosphoryleres efterfølgende (dvs.et phosphat fjernes) af phosphoglyceratkinase til 3-phosphoglycerat. Hvert fosfat frigivet i denne reaktion kan konvertere et molekyle ADP til et højenergi – ATP-molekyle, hvilket resulterer i en gevinst på to ATP-molekyler.fosfoglyceratmutasen omdanner derefter 3-phosphoglyceratmolekylerne til 2-phosphoglycerat. Enolase virker derefter på 2-phosphoglyceratmolekylerne for at omdanne dem til phosphoenolpyruvatmolekyler. Det sidste trin i glykolyse involverer dephosphorylering af de to phosphoenolpyruvatmolekyler med pyruvatkinase for at skabe to pyruvatmolekyler og to ATP-molekyler.
sammenfattende nedbrydes et glukosemolekyle i to pyruvatmolekyler og skaber to netto ATP-molekyler og to NADH-molekyler ved glykolyse. Derfor genererer glykolyse energi til cellen og skaber pyruvatmolekyler, der kan behandles yderligere gennem den aerobe Krebs-cyklus (også kaldet citronsyrecyklus eller tricarboksilsyrecyklus); omdannes til mælkesyre eller alkohol (i gær) ved gæring; eller bruges senere til syntese af glukose gennem glukoneogenese.
anaerob Respiration
når ilt er begrænset eller fraværende, kommer pyruvat ind i en anaerob vej. I disse reaktioner kan pyruvat omdannes til mælkesyre. Ud over at generere en yderligere ATP tjener denne vej til at holde pyruvatkoncentrationen lav, så glykolyse fortsætter, og den ilter NADH ind i nad+, der kræves af glykolyse. I denne reaktion erstatter mælkesyre ilt som den endelige elektronacceptor. Anaerob respiration forekommer i de fleste celler i kroppen, når ilt er begrænset, eller mitokondrier er fraværende eller ikke-funktionelle. For eksempel, fordi erythrocytter (røde blodlegemer) mangler mitokondrier, skal de producere deres ATP fra anaerob respiration. Dette er en effektiv vej til ATP-produktion i korte perioder, der spænder fra sekunder til et par minutter. Den producerede mælkesyre diffunderer ind i plasmaet og føres til leveren, hvor den omdannes tilbage til pyruvat eller glukose via Cori-cyklussen. Tilsvarende, når en person træner, bruger musklerne ATP hurtigere end ilt kan leveres til dem. De er afhængige af glykolyse og mælkesyreproduktion for hurtig ATP-produktion.
aerob Respiration
i nærvær af ilt kan pyruvat komme ind i Krebs-cyklussen, hvor yderligere energi ekstraheres, når elektroner overføres fra pyruvatet til receptorerne NAD+, BNP og FAD, hvor kulsyre er et “affaldsprodukt” (figur 3). NADH og FADH2 sender elektroner videre til elektrontransportkæden, der bruger den overførte energi til at producere ATP. Som det terminale trin i elektrontransportkæden er ilt den terminale elektronacceptor og skaber vand inde i mitokondrierne.
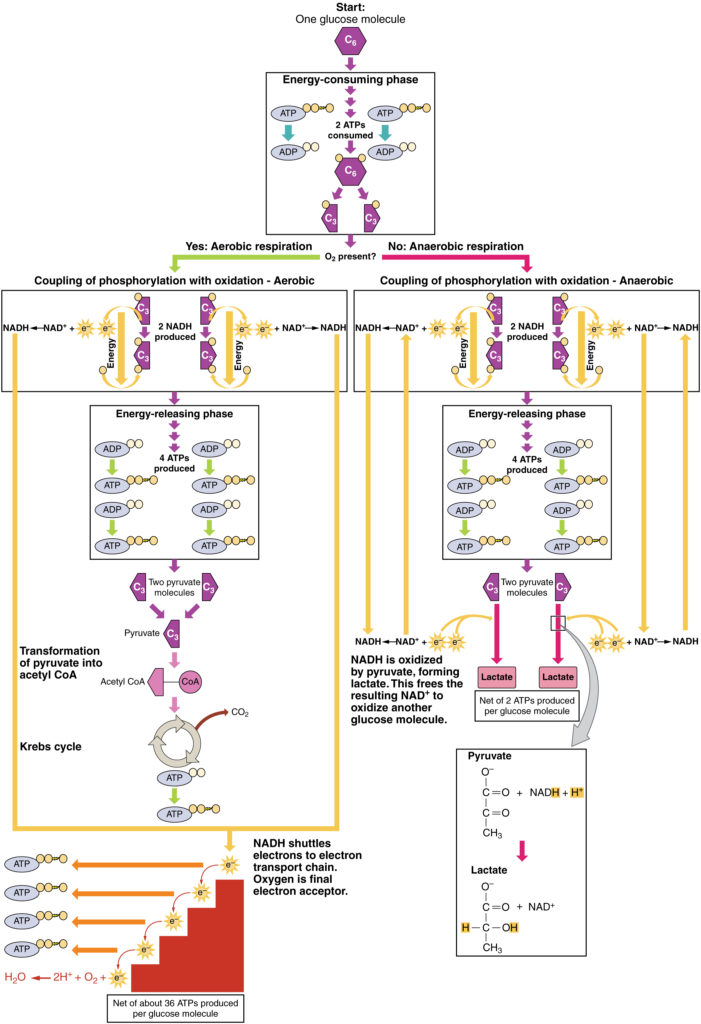
figur 3. Klik for at se et større billede. Processen med anaerob respiration omdanner glukose til to lactatmolekyler i fravær af ilt eller inden for erythrocytter, der mangler mitokondrier. Under aerob respiration iltes glukose i to pyruvatmolekyler.
Krebs-cyklus/citronsyrecyklus / Tricarboksysyre-cyklus
pyruvatmolekylerne, der genereres under glykolyse, transporteres over mitokondriemembranen ind i den indre mitokondrielle matrice, hvor de metaboliseres af Krebs i en vej kaldet Krebs-cyklus (figur 4). Krebs-cyklussen kaldes også almindeligvis citronsyrecyklussen eller TCA-cyklussen. Under Krebs cyklus, høj-energi molekyler, herunder ATP, NADH, og FADH2, er skabt. NADH og FADH2 passerer derefter elektroner gennem elektrontransportkæden i mitokondrierne for at generere flere ATP-molekyler.
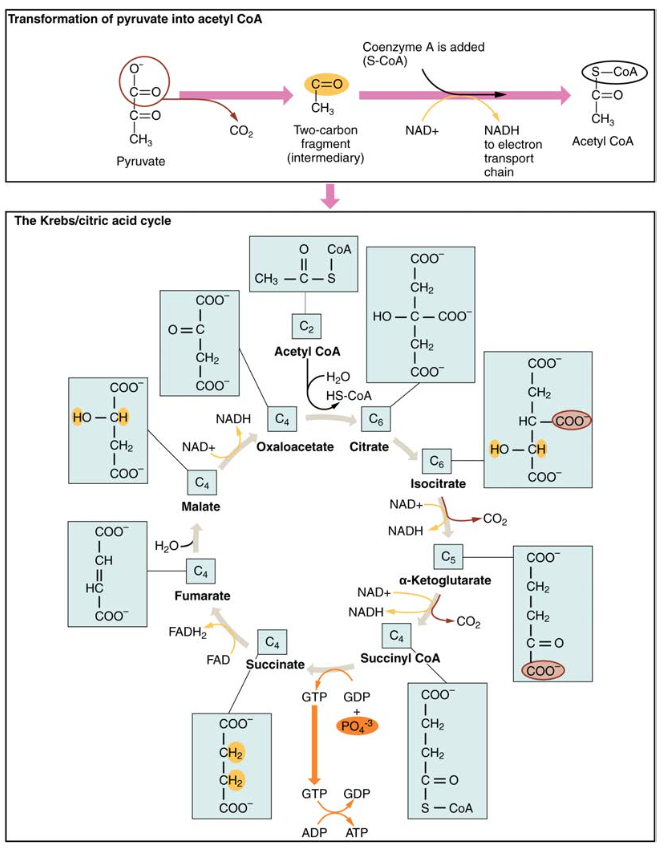
figur 4. Under Krebs-cyklussen omdannes hvert pyruvat, der genereres ved glykolyse, til et to-carbon acetyl CoA-molekyle. Acetyl CoA behandles systematisk gennem cyklussen og producerer højenergi NADH -, FADH2-og ATP-molekyler.
se denne animation for at observere Krebs cyklus.et af de mest almindelige typer af pyruvatmolekyler, der dannes under glykolysen, er de tre carbon-pyruvatmolekyler, der dannes under glykolysen, og som omdannes til et to-carbon-acetyl-CoA-molekyle (acetyl-CoA). Denne reaktion er en iltningsreaktion. Det omdanner tre-carbon pyruvat til et to-carbon acetyl CoA-molekyle, frigiver kulsyre og overfører to elektroner, der kombineres med NAD+ for at danne NADH. Acetyl CoA kommer ind i Krebs-cyklussen ved at kombinere med et fire-carbonmolekyle, oksaloacetat, for at danne sekskulstofmolekylet citrat, eller citronsyre, samtidig frigive coensymet et molekyle.seks-carbon citratmolekylet omdannes systematisk til et fem-carbonmolekyle og derefter et fire-carbonmolekyle, der slutter med oksaloacetat, begyndelsen af cyklussen. Undervejs vil hvert citratmolekyle producere en ATP, en FADH2 og tre NADH. FADH2 og NADH kommer ind i det oksidative phosphoryleringssystem placeret i den indre mitokondriemembran. Derudover leverer Krebs-cyklussen udgangsmaterialerne til at behandle og nedbryde proteiner og fedtstoffer.for at starte Krebs-cyklussen kombinerer citratsyntase acetyl CoA og oksaloacetat til dannelse af et seks-carbon citratmolekyle; CoA frigives efterfølgende og kan kombineres med et andet pyruvatmolekyle for at starte cyklussen igen. Dette er en af de mest almindelige årsager til, at citrat omdannes til isocitrat. To CO2-molekyler og to NADH-molekyler produceres, når isocitrat-dehydrogenase omdanner isocitrat til fem-carbon-Kurt-ketoglutaratet, som derefter katalyseres og omdannes til fire-carbon-succinyl-CoA ved hjælp af Kurt-ketoglutaratdehydrogenase. Succinyl CoA dehydrogenase omdanner derefter succinyl CoA til succinat og danner højenergimolekylet GTP, som overfører sin energi til ADP for at producere ATP. Succinatdehydrogenase omdanner derefter succinat til fumarat og danner et molekyle af FADH2. Fumarase omdanner derefter fumarat til malat, hvilket malatdehydrogenase derefter omdannes til oksaloacetat, mens nad+ reduceres til NADH. Derefter er han klar til at kombinere med den næste acetyl CoA for at starte Krebs-cyklussen igen (se figur 4). For hver drejning af cyklussen oprettes tre NADH, en ATP (gennem GTP) og en FADH2. Hvert carbon af pyruvat omdannes til CO2, som frigives som et biprodukt af iltningsmiddel (aerob) respiration.
iltning af phosphorylering og elektrontransportkæden
elektrontransportkæden (ETC) bruger NADH og FADH2 produceret af Krebs-cyklussen til at generere ATP. Elektroner fra NADH og FADH2 overføres gennem proteinkomplekser indlejret i den indre mitokondriemembran ved en række fermatiske reaktioner. Elektrontransportkæden består af en serie på fire komplekser (kompleks i – kompleks IV) og to coensymer (allestedsnærværende og cytokrom c), der fungerer som elektronbærere og protonpumper, der bruges til at overføre H+ – ioner til rummet mellem de indre og ydre mitokondriemembraner (figur 5). ETC parrer overførslen af elektroner mellem en donor (som NADH) og en elektronacceptor (som O2) med overførslen af protoner (H+ ioner) over den indre mitokondriemembran, hvilket muliggør processen med iltning phosphorylering. I nærvær af ilt ledes energi trinvis gennem elektronbærerne for gradvist at opsamle den energi, der er nødvendig for at fastgøre et fosfat til ADP og producere ATP. Rollen af molekylært ilt, O2, er som den terminale elektronacceptor for ETC. Dette betyder, at når elektronerne har passeret gennem hele ETC, skal de overføres til et andet, separat molekyle. Disse elektroner, O2 og H+ ioner fra matricen kombineres for at danne nye vandmolekyler. Dette er grundlaget for dit behov for at indånde ilt. Uden ilt ophører elektronstrømmen gennem ETC.
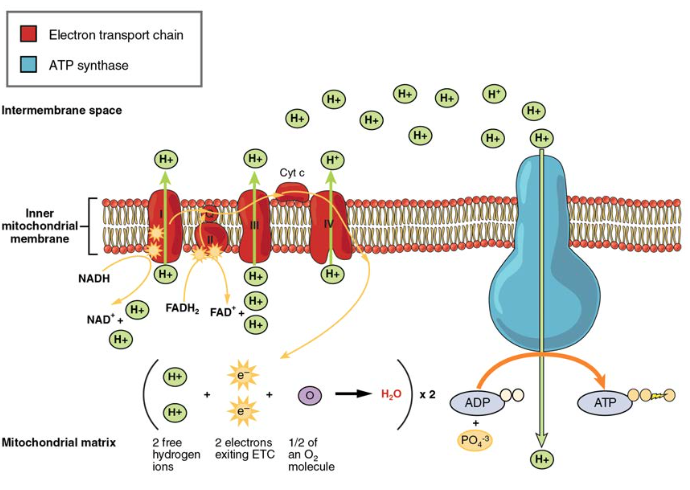
figur 5. Elektrontransportkæden er en serie af elektronbærere og ionpumper, der bruges til at pumpe H+ ioner ud af den indre mitokondrielle matrice.
se denne video for at lære om elektrontransportkæden.
elektronerne frigivet fra NADH og FADH2 føres langs kæden af hver af bærerne, som reduceres, når de modtager elektronen og iltes, når de overføres til den næste bærer. Hver af disse reaktioner frigiver en lille mængde
energi, som bruges til at pumpe H+ ioner over den indre membran. Akkumuleringen af disse protoner i rummet mellem membranerne skaber en protongradient med hensyn til mitokondriematricen.
også indlejret i den indre mitokondriemembran er et fantastisk proteinporekompleks kaldet ATP-syntase. Effektivt er det en turbine, der drives af strømmen af H+ – ioner over den indre membran ned ad en gradient og ind i mitokondriematricen. Når h+ – ionerne krydser komplekset, roterer kompleksets aksel. Denne rotation gør det muligt for andre dele af ATP-syntase at tilskynde ADP og Pi til at skabe ATP. Glucosemolekyle gennem aerob respiration er det vigtigt at huske følgende punkter:
- et net på to ATP produceres gennem glykolyse (fire produceret og to forbruges i det energiforbrugende Stadium). Imidlertid anvendes disse to ATP til transport af NADH produceret under glykolyse fra cytoplasma til mitokondrier. Derfor er nettoproduktionen af ATP under glykolyse nul.
- i alle faser efter glykolyse skal antallet af producerede ATP, NADH og FADH2 ganges med to for at afspejle, hvordan hvert glukosemolekyle producerer to pyruvatmolekyler.
- i ETC produceres ca. tre ATP for hver oksidiseret NADH. Imidlertid produceres kun ca.to ATP for hver iltet FADH2. Elektronerne fra FADH2 producerer mindre ATP, fordi de starter på et lavere punkt i ETC (kompleks II) sammenlignet med elektronerne fra NADH (kompleks i) (figur 5).
derfor produceres der for hvert glukosemolekyle, der kommer ind i aerob respiration, en nettotal på 36 ATP ‘ er (se figur 6).
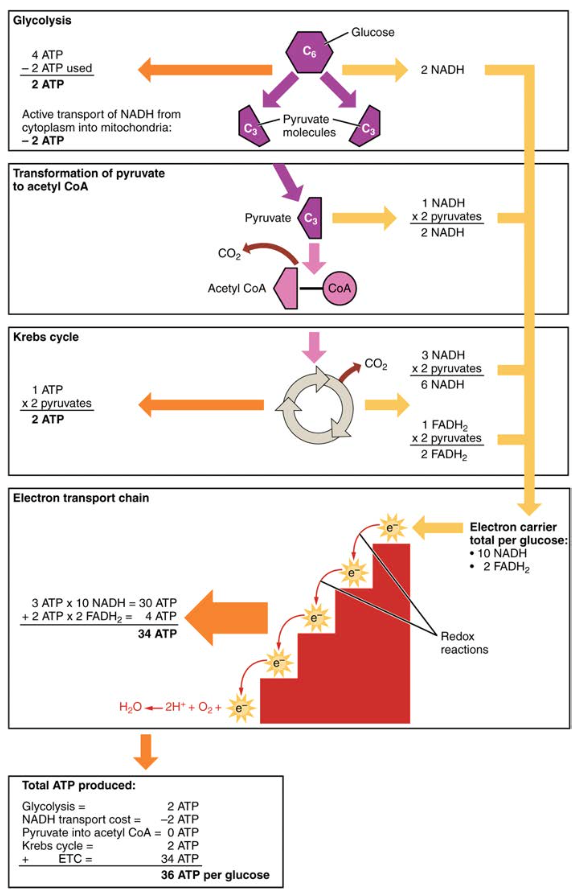
figur 6. Kulhydratmetabolisme involverer glykolyse, Krebs-cyklussen og elektrontransportkæden.
glukoneogenese
glukoneogenese er syntesen af nye glukosemolekyler fra pyruvat, lactat, glycerol eller aminosyrerne alanin eller glutamin. Denne proces foregår primært i leveren i perioder med lav glukose, det vil sige under betingelser med faste, sult og lavt kulhydratdiet. Så spørgsmålet kan rejses om, hvorfor kroppen ville skabe noget, den lige har brugt en hel del indsats for at nedbryde? Visse nøgleorganer, herunder hjernen, kan kun bruge glukose som energikilde; derfor er det vigtigt, at kroppen opretholder en minimal blodglukosekoncentration. Når blodglukosekoncentrationen falder under det bestemte punkt, syntetiseres ny glukose af leveren for at hæve blodkoncentrationen til normal.
glukoneogenese er ikke blot det modsatte af glykolyse. Der er nogle vigtige forskelle (Figur 7). Pyruvat er et almindeligt udgangsmateriale til glukoneogenese. For det første omdannes pyruvatet til oksaloacetat. En af de mest almindelige årsager til denne sygdom er, at det er en sygdom, der kan føre til en alvorlig sygdom. Fra dette trin er glukoneogenese næsten det modsatte af glykolyse. PEP omdannes tilbage til 2-phosphoglycerat, som omdannes til 3-phosphoglycerat. Derefter omdannes 3-phosphoglycerat til 1,3 bisphosphoglycerat og derefter til glyceraldehyd-3-phosphat. To molekyler glyceraldehyd-3-phosphat kombineres derefter til dannelse af fruktose-1-6-bisphosphat, som omdannes til fructose 6-phosphat og derefter til glucose-6-phosphat. Endelig genererer en række reaktioner glukose i sig selv. Ved glukoneogenese (sammenlignet med glycolyse) erstattes geksokinasen med glucose-6-phosphatase, og phosphofructokinase-1 erstattes af fructose-1,6-bisfosfatase. Dette hjælper cellen med at regulere glykolyse og glukoneogenese uafhængigt af hinanden.som det vil blive diskuteret som en del af lipolyse, kan fedtstoffer opdeles i glycerol, som kan phosphoryleres til dannelse af DIHYDROKSYACETONPHOSPHAT eller DHAP. DHAP kan enten komme ind i den glykolytiske vej eller bruges af leveren som et substrat til glukoneogenese.
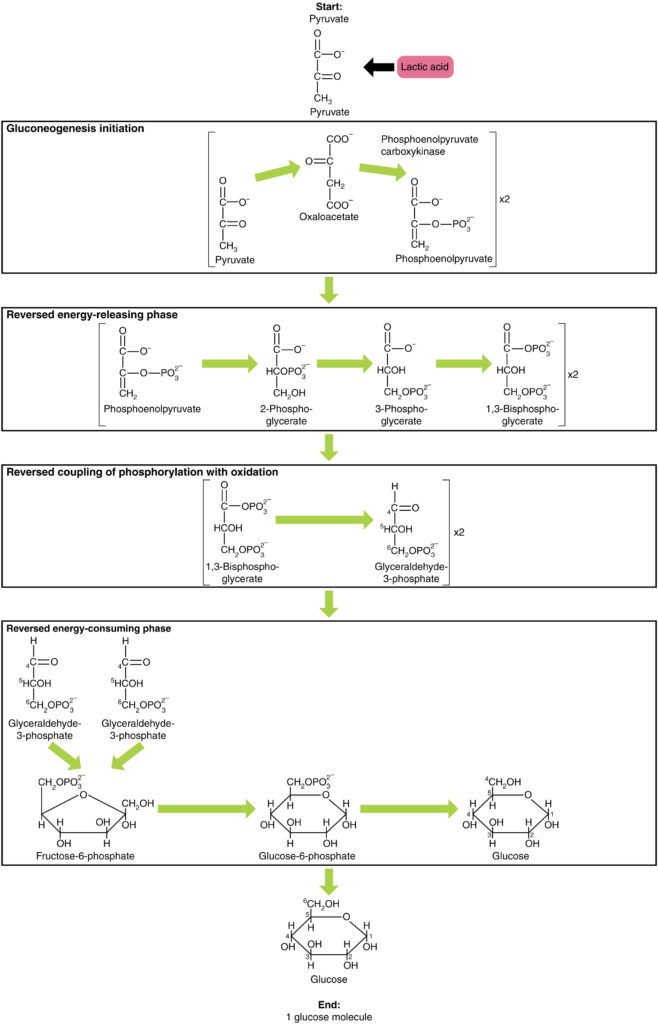
Figur 7. Klik for at se et større billede. Glukoneogenese er syntesen af glucose fra pyruvat, lactat, glycerol, alanin eller glutamat.
aldring og kroppens metaboliske hastighed
den menneskelige krops metaboliske hastighed falder næsten 2 procent pr. Ændringer i kropssammensætning, herunder reduceret magert muskelmasse, er for det meste ansvarlige for dette fald. Det mest dramatiske tab af muskelmasse og deraf følgende fald i stofskiftet forekommer mellem 50 og 70 år. Tab af muskelmasse svarer til reduceret styrke, som har tendens til at hæmme seniorer fra at engagere sig i tilstrækkelig fysisk aktivitet. Dette resulterer i et system med positiv feedback, hvor den reducerede fysiske aktivitet fører til endnu mere muskeltab, hvilket yderligere reducerer stofskiftet.
der er flere ting, der kan gøres for at forhindre generelle fald i stofskiftet og for at bekæmpe den cykliske karakter af disse fald. Disse inkluderer at spise morgenmad, spise små måltider ofte, indtage masser af magert protein, drikke vand for at forblive hydreret, træne (inklusive styrketræning) og få nok søvn. Disse foranstaltninger kan hjælpe med at holde energiniveauet fra at falde og bremse trangen til øget kalorieforbrug fra overdreven snacking. Selvom disse strategier ikke garanteres at opretholde stofskiftet, hjælper de med at forhindre muskeltab og kan øge energiniveauet. Nogle eksperter foreslår også at undgå sukker, hvilket kan føre til overskydende fedtopbevaring. Krydret mad og grøn te kan også være gavnligt. Fordi stress aktiverer cortisolfrigivelse, og cortisol bremser stofskiftet, kan det også hjælpe at undgå stress eller i det mindste øve afslapningsteknikker.
Kapitel gennemgang
metaboliske katalyserer kataboliske reaktioner, der nedbryder kulhydrater indeholdt i fødevarer. Den frigjorte energi bruges til at drive de celler og systemer, der udgør din krop. Overskydende eller uudnyttet energi opbevares som fedt eller glykogen til senere brug. Kulhydratmetabolisme begynder i munden, hvor spytamylasen begynder at nedbryde komplekse sukkerarter i monosaccharider. Disse kan derefter transporteres over tarmmembranen ind i blodbanen og derefter til kropsvæv. I cellerne behandles glucose, et seks-carbon sukker, gennem en sekvens af reaktioner i mindre sukkerarter, og den energi, der er lagret inde i molekylet, frigives. Det første trin i kulhydratkatabolisme er glykolyse, der producerer pyruvat, NADH og ATP. Under anaerobe forhold kan pyruvatet omdannes til lactat for at holde glykolyse i gang. Under aerobe forhold kommer pyruvat ind i Krebs-cyklussen, også kaldet citronsyrecyklus eller tricarksilsyrecyklus. Ud over ATP producerer Krebs-cyklussen højenergi-FADH2-og NADH-molekyler, som tilvejebringer elektroner til den iltende phosphoryleringsproces, der genererer mere højenergi-ATP-molekyler. For hvert glukosemolekyle, der behandles i glykolyse, kan der oprettes et net på 36 ATPs ved aerob respiration.
under anaerobe forhold er ATP-produktion begrænset til dem, der genereres ved glykolyse. Mens i alt fire ATP ‘ er produceres ved glykolyse, er to nødvendige for at begynde glykolyse, så der er et nettoudbytte af to ATP-molekyler.
under betingelser med lav glukose, såsom faste, sult eller diæt med lavt kulhydratindhold, kan glukose syntetiseres fra lactat, pyruvat, glycerol, alanin eller glutamat. Denne proces, kaldet glukoneogenese, er næsten det modsatte af glykolyse og tjener til at skabe glukosemolekyler til glukoseafhængige organer, såsom hjernen, når glukoseniveauerne falder under det normale.
selvkontrol
Besvar nedenstående spørgsmål for at se, hvor godt du forstår emnerne i det foregående afsnit.
kritiske Tænkningsspørgsmål
- Forklar, hvordan glukose metaboliseres for at give ATP.
- Diskuter mekanismen celler anvender til at skabe en koncentrationsgradient for at sikre kontinuerlig optagelse af glukose fra blodbanen.
ordliste
polysaccharider: komplekse kulhydrater, der består af mange monosaccharider
monosaccharid: mindste, monomere sukkermolekyle
spytamylase: af kulhydrater i munden
cellulær respiration: produktion af ATP fra glucoseoksidering via glycolyse, Krebs cyklus, og iltning phosphorylering
glycolyse: serie af metaboliske reaktioner, der nedbryder glukose i pyruvat og producerer ATP
pyruvat: tre-carbon slutprodukt af glycolyse og udgangsmateriale, der omdannes til acetyl CoA, der kommer ind i
Krebs cyklus: pyruvat til CO2 og højenergi FADH2, NADH og ATP molekyler
citronsyrecyklus (TCA): også kaldet Krebs-cyklus eller tricarbosylsyrecyklus; omdanner pyruvat til CO2 og højenergi FADH2, NADH og ATP molekyler
energiforbrugende fase, første fase af glykolyse, hvor to molekyler af ATP er nødvendige for at reducere mængden af for at starte reaktionen
glucose-6-phosphat: phosphoryleret glucose produceret i det første trin af glycolyse
geksokinase: i leveren, som omdanner glucose til glucose-6-phosphat ved optagelse i cellen
Glucokinase, som omdanner glucose til glucose-6-phosphat ved optagelse i cellen
energigivende fase: anden fase af glykolyse, hvor energi produceres
terminal elektronacceptor: ATP – produktionsvej, hvor elektroner ledes gennem en række iltningsreduktionsreaktioner, der danner vand og producerer en protongradient
Krebs cyklus: pyruvat til CO2 og højenergi FADH2, NADH og ATP molekyler
elektrontransportkæde (ETC): ATP-produktionsvej, hvor elektroner ledes gennem en række iltningsreduktionsreaktioner, der danner vand og producerer en protongradient
oksidativ phosphorylering: proces, der omdanner højenergi NADH og FADH2 til ATP
ATP-syntaseprotein: porekompleks, der skaber ATP
/p>
glukoneogenese: proces med glukosesyntese fra pyruvat eller andre molekyler