US Pharm. 2020;45 (2): HS7-HS12.
absztrakt: az akut koronária szindróma (ACS) a morbiditás és mortalitás gyakori oka az Egyesült Államokban. 2014-ben több mint 1,3 millió kórházi kibocsátás, köztük a miokardiális infarktusban szenvedő betegek 71% – a volt az ACS elsődleges vagy másodlagos diagnózisa. Az ACS megfelelő kezelése és a farmakoterápia megfelelő alkalmazása kritikus fontosságú a kardiális események megismétlődésének megelőzésében. Tekintettel a gyógyszerek betartásának fontosságára, a gyógyszerészek fontos szerepet játszanak az ACS kezelésében és a másodlagos megelőzésben.
a szív-és érrendszeri betegség a halálozás vezető oka az Egyesült Államokban, a szívkoszorúér-betegség pedig a kardiovaszkuláris halálozás leggyakoribb oka.1 az akut koszorúér-szindróma (ACS) kifejezés a szívkoszorúér-betegség három típusát foglalja magában, amelyet akut myocardialis ischaemia és/vagy myocardialis infarctus (MI) jellemez.2 Ez a cikk áttekinti az ACS-t, a jelenlegi kezeléseket és a másodlagos megelőzési ajánlásokat, és kiemeli a gyógyszerész beavatkozásának kulcsfontosságú területeit.
az ACS a morbiditás és mortalitás gyakori oka. 40 másodpercenként valaki az USA-ban infarktust tapasztal.1 2014-ben több mint 1,3 millió kórházi kibocsátás, köztük az MI-ben szenvedő betegek 71% – a volt az ACS elsődleges vagy másodlagos diagnózisa.1 A férfiak gyakrabban tapasztalják az ACS-t, mint a nők, körülbelül 1,4:1 arányban.1
betegség-állapot áttekintés
az ACS a szívizom oxigénigényének és-kínálatának hirtelen kiegyensúlyozatlanságából ered, amely leggyakrabban a koszorúér véráramlásának elzáródása miatt következik be.2 elzáródás léphet fel egy sebezhető, lipidterhelt, ateroszklerotikus plakk repedésével vagy eróziójával, rostos sapkával, amely részben vagy teljesen elzárja a koszorúér artériát.2,3 a rostos sapka megzavarása serkenti a trombogenezist.2,3 a koszorúér Trombusképződése és vazospazmusa csökkenti a véráramlást és ischaemiás mellkasi fájdalmat okoz, ami az ACS klasszikus tünete.2,3 a nyomásszerű mellkasi fájdalom gyakran a bal karra, a nyakra vagy az állkapocsra sugárzik.3 kísérő tünetek lehetnek: légszomj, izzadás, hűvös vagy nyirkos bőr, hányinger, hányás és megmagyarázhatatlan fáradtság.3 az ACS diagnózisának medián életkora az Egyesült Államokban 68 év.2
diagnózis
az ACS három diagnózisra oszlik: ST-szegmens magasságú MI (STEMI), amely jellemzően teljes koszorúér–elzáródással jár; nem ST-szegmens magasságú MI (NSTEMI); és instabil angina (UA).Az ACS altípusok 2-4 differenciálódása az EKG változásokon és a szív biomarkerek jelenlétén alapul.2 a STEMI-t az EKG tartós ST-emelkedése jellemzi, biomarkerek, például szívtroponinok felszabadulásával, ami myocardialis nekrózist jelez.4 az ACS–ben szenvedő betegek körülbelül 75%-ánál van nem ST-szegmens magasságú ACS (NSTE-ACS), amely magában foglalja az NSTEMI-t és az UA-t.2 az NSTE-ACS nem rendelkezik állandó ST-emelkedéssel az EKG-n.2 az NSTEMI-vel diagnosztizált betegek emelkedett szív biomarkerekkel rendelkeznek, míg az UA-val rendelkezők nem.2 NSTE-ACS-ben szenvedő betegek általában több társbetegségben szenvednek, mint a STEMI-ben szenvedő betegek.2
Általános kezelés
az ACS kezelése időérzékeny, sokrétű és egy adott diagnózistól függ. Az American College of Cardiology (ACC) és az American Heart Association (AHA) számos gyakorlati iránymutatást dolgozott ki az ACS kezelésére és másodlagos megelőzésére.2,4 – 6 a felülvizsgálat alapját képező iránymutatásokat részletesebb információkért meg kell vizsgálni.
reperfúziós terápia
a koszorúér-perfúzió gyors helyreállítása a STEMI-kezelés sarokköve.3,4 reperfúzió, amely mechanikus úton (pl., elsődleges perkután koszorúér-beavatkozás) vagy farmakológiai (pl. fibrinolitikus) azt jelenti, hogy minden alkalmas STEMI-betegnek be kell adni, akiknél ischaemiás tünetek több mint 12 órán át.4 az érintett terület elsődleges PCI-je a kórház megérkezésétől számított 90 percen belül előnyös a fibrinolitikus terápiával szemben, ha a kezelés késleltetésének ideje rövid, és a kórház képes PCI elvégzésére.4 A PCI-t gyakran csupasz fém vagy kábítószer-eluáló stentek elhelyezése kíséri.4 Ha a PCI nem lehetséges, fibrinolitikus terápia ajánlott a kórház megérkezésétől számított 30 percen belül.4,7 a fibrinolízist követő 24 órán belül PCI-képes kórházba történő áthelyezés szintén javíthatja az eredményeket.4,7
NSTE-ACS a megnövekedett mortalitási kockázatú betegek szintén jogosultak lehetnek korai revaszkularizációra PCI – vel vagy koszorúér bypass grafttal, míg a nem magas kockázatú betegek ischaemia által irányított stratégiával kezelhetők, amely magában foglalja a késleltetett PCI-t vagy az orvosi kezelést egyedül.2 az NSTE-ACS-ben szenvedő betegek körülbelül 32-40% – a esik át PCI-n.2 a fibrinolitikus kezelés nem javasolt NSTE-ACS esetén, mivel nem állnak rendelkezésre olyan adatok, amelyek igazolják a mortalitás vagy az MI előnyeit, valamint a megnövekedett intracranialis vérzést.2,7
a korai fibrinolitikus terápia előnyei jól megalapozottak azoknál a STEMI-betegeknél, akik nem végezhetnek PCI-t.4 az Egyesült Államokban három IV. fibrinolitikus szer áll rendelkezésre: a tenektepláz, a retepláz és az altepláz szöveti plazminogén aktivátorok.8-10 mindegyik trombolitikus hatást fejt ki a fibrinhez való kötődéssel és a plazminogén plazminná alakításával, amely megszakítja a keresztkötéseket a trombus fibrinmolekulái között.8-10 a fibrinolitikumok növelik a vérzés kockázatát, és ellenjavallt olyan helyzetekben, amikor túlzott vérzés léphet fel, mint például a közelmúltbeli stroke és az aktív belső vérzés.8-10
orvosi kezelés
a reperfúziós stratégiától függetlenül az ACS kezelésére kettős vérlemezke-gátló kezelés és antikoaguláció ajánlott.2,4,5 számos vérlemezke-gátló és antikoaguláns gyógyszer áll rendelkezésre (1.táblázat). A gyógyszerészek kulcsszerepet játszhatnak a gyógyszerek kezelésében és a betegek tanácsadásában, különös tekintettel a vérzés kockázatára.
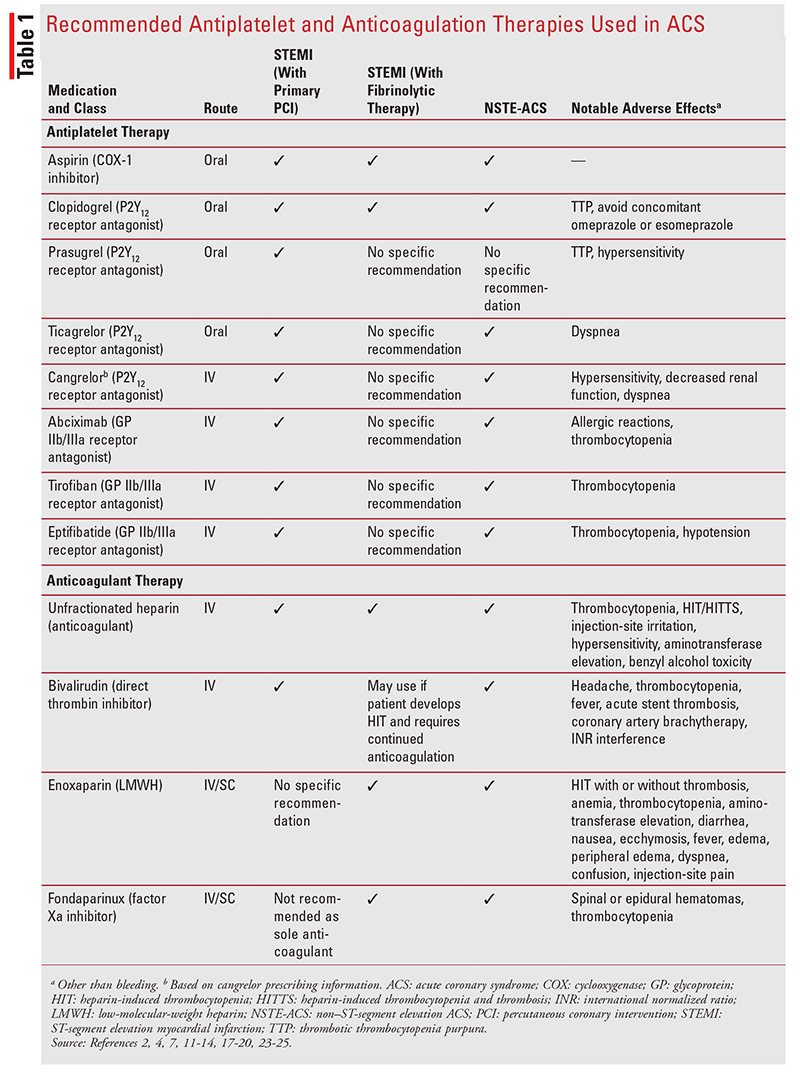
vérlemezke-gátló terápia: az aszpirin az ACS-ben szenvedő betegek ellátásának színvonala.2,4 thrombocyta-gátló hatását a vérlemezke-ciklooxigenáz-1 irreverzibilis inaktiválása közvetíti, amely megakadályozza a tromboxán A2 szintézisét, amely a vérlemezke-aggregáció erős agonistája.2 Az aszpirin megakadályozza az akut trombotikus elzáródást a PCI alatt, csökkenti a stent trombózis kockázatát, és a fibrinolitikus terápiával jótékony hatást fejt ki.4 NSTE-ACS-ben szenvedő betegeknél kimutatták, hogy az aszpirin csökkenti a kiújuló MI és halálozás incidenciáját.2 az aszpirint szájon át kell beadni a lehető leghamarabb a kezdeti megjelenéskor, és határozatlan ideig folytatni kell.2,4,7
ACS betegeknél a P2Y12 inhibitort kell aszpirinnel együtt adni a kettős vérlemezke-gátló terápia biztosítása érdekében.A 2,4 P2Y12 inhibitor gátolja a thrombocyta aktiválódást és aggregációt azáltal, hogy megakadályozza az adenozin-difoszfát kötődését a P2Y12 thrombocyta receptor helyéhez.11-14 négy P2Y12 inhibitor áll rendelkezésre az Egyesült Államokban.; a klopidogrélt, a prasugrelt és a ticagrelort orálisan adják be, és szerepelnek az ACC/AHA STEMI és NSTE-ACS irányelvekben, míg a cangrelort IV.11-14 telítő adag P2Y12 inhibitort kell beadni az elsődleges PCI vagy fibrinolitikus kezelés előtt vagy idején.Az orális szerek 4 fenntartó dózisát legfeljebb 1 évig kell folytatni.2,4
a kettős vérlemezke-gátló terápia előnyeit először a 2001-es mérföldkőnek számító vizsgálatban mutatták be, klopidogrél instabil anginában a visszatérő események megelőzése érdekében (gyógyítás).15 ebben a vizsgálatban több mint 12 000 NSTE-ACS beteg kapott kezelést aszpirin plusz klopidogrél vagy aszpirin önmagában.15 A 12. hónapban az aszpirin plusz klopidogrél csoportban csökkent a cardiovascularis halálozás, MI vagy stroke kockázata az önmagában alkalmazott aszpirin csoporthoz képest (9, 3% vs.11, 4%; relatív kockázat, 0, 80; 95% CI, 0, 72-0, 90; P <.001), nincs jelentős különbség a vérzéses stroke vagy életveszélyes vérzés epizódjaiban.15 2005-ben két tanulmány pozitív eredményeket mutatott az aszpirin plusz klopidogrél esetében STEMI-ben szenvedő betegeknél.16 azóta a klopidogrélt, a prasugrelt, a ticagrelort és a kangrelort különböző ACS-vizsgálatokban vizsgálták és hasonlították össze, amelyek mindegyike egy adott kombináció előnyeit és kockázatait mutatta.2,4,16
az Abciximab, az eptifibatid és a tirofibán IV.glikoprotein (GP) IIb/IIIa receptor antagonisták, amelyek a thrombocyta aggregáció végső közös útját célozzák meg.2 GP IIb / IIIa receptor antagonisták adjuvánsként alkalmazhatók a PCI idején STEMI-ben és NSTE-ACS-ben szenvedő kiválasztott betegeknél, akik nem frakcionált heparint kapnak.2,4 az orális antiplatelets fokozott elérhetősége miatt azonban ezeket a szereket sokkal ritkábban alkalmazzák ACS-ben szenvedő betegeknél.3 az aszpirin és a P2Y12 inhibitorok egyidejű alkalmazása fokozott vérzési kockázattal járt, és a GP IIb/IIIa inhibitorok alkalmazása rutinszerűen nem javasolt az antikoaguláns bivalirudint kapó betegeknél.4,7 egyes betegeknél az abciximab Intrakoronáris alkalmazása megfelelő lehet.4 NSTE-ACS-ben szenvedő betegeknél a tirofibánt és az eptifibatidot részesítik előnyben.2
az ACC / AHA irányelvek nem javasolják az egyik vérlemezke-gátlót a másik felett; azt tanácsolják, hogy a vérlemezke-gátló alkalmazás szorosan tükrözze a vizsgálatokban történő alkalmazást, és az előny és kockázat szempontjából egyénre szabott legyen.2,4 a thrombocyta-gátló szerek esetében általában a vérzés, amely esetenként életveszélyes vagy halálos kimenetelű.2,11-14,17-19
antikoagulációs terápia: az antikoagulációs terápia fontos szerepet játszik az ACS kezelésében.7 A PCI-n átesett STEMI betegeknek nem frakcionált heparint kell kapniuk, amelyet terápiás aktivált alvadási időre titrálnak.4,7 a Bivalirudin előzetes nem frakcionált heparinnal vagy anélkül is alkalmazható, és a nagy vérzési kockázatú betegeknél a nem frakcionált heparinnal és egy GP IIb/IIIa antagonistával szemben előnyösebb.4,7,20 az enoxaparin és a fondaparinux ilyen betegeknél történő alkalmazására vonatkozó adatok korlátozottak.4 ezenkívül a fondaparinux nem alkalmazható egyedüli antikoagulánsként PCI-vel együtt, mivel katéter trombózissal járt.4 a fibrinolitikus terápiában részesülő STEMI betegek legalább 48 órán át, legfeljebb 8 napig vagy a revaszkularizációig nem frakcionált heparint, enoxaparint vagy Fondaparinuxot kaphatnak.4
NSTE-ACS-ben szenvedő betegeknél az enoxaparin, a bivalirudin, a fondaparinux és a nem frakcionált heparin választható; az enoxaparin a leghatározottabban ajánlott.2 az enoxaparint vagy a Fondaparinuxot SC-ben adják be a kórházi kezelés időtartama alatt vagy a PCI elvégzéséig.2 ha a PCI-t fondaparinux-szal együtt alkalmazzák, a katéter trombózisának kockázatának csökkentése érdekében nem frakcionált heparint vagy bivalirudint kell alkalmazni.2 a bivalirudin alkalmazható olyan betegeknél, akiket korai invazív stratégiával kezeltek a diagnosztikai angiográfiáig vagy a PCI-ig.2 A nem frakcionált heparin 48 órán át vagy a PCI-ig adható.2
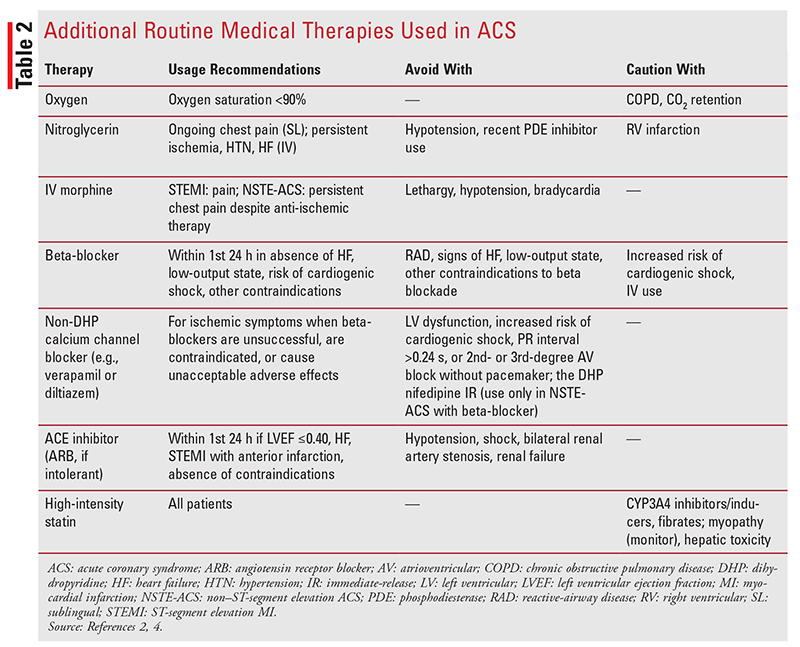
további rutinszerű orvosi kezelések: az ACS-ben szenvedő betegek egyéb rutin terápiái kiegészítő oxigén, nitroglicerin, IV morfin, béta-blokkolók, kalciumcsatorna-blokkolók, ACE-gátlók és nagy intenzitású sztatinok (2.táblázat).2,4,7 ezek a terápiák STEMI vagy NSTE-ACS-ben szenvedő betegeknél alkalmazhatók, és thrombocyta-gátló és antikoaguláns terápiával kombinálva alkalmazhatók.
másodlagos megelőzés
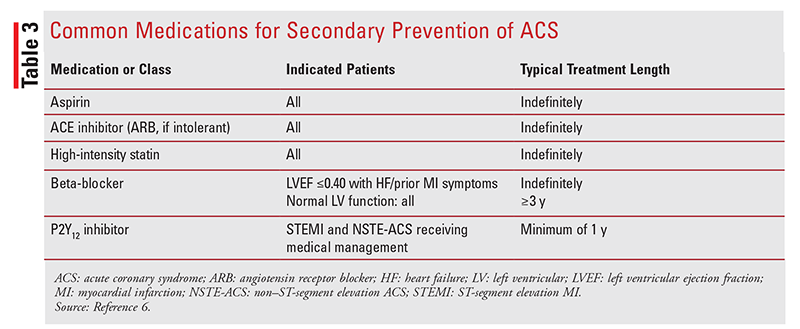
miután a beteg ACS eseményt tapasztal, a hosszú távú kezelés és az utánkövetés elengedhetetlen egy jövőbeli esemény vagy halál megelőzéséhez.6 a másodlagos megelőzésre szolgáló gyógyszereket, beleértve az aszpirint, az ACE-gátlókat, a sztatinokat, a béta-blokkolókat és a P2Y12 gátlókat (3.táblázat), a kórházi elbocsátás előtt kell elkezdeni.6 további másodlagos prevenciós terápiák megfontolásra kerülnek a vérnyomás szabályozása, a cukorbetegség kezelése, a dohányzásról való leszokás, a testsúlykezelés, a megfelelő fizikai aktivitás, az influenza elleni oltás és a szívrehabilitáció.6
A gyógyszerész szerepe
a gyógyszerek betartása kiemelkedő fontosságú az ACS kezelésében és másodlagos megelőzésében, mivel a rossz tapadás rosszabb kardiovaszkuláris kimenetelhez vezethet, beleértve a megnövekedett mortalitást.21,22 egy kanadai kohorsz tanulmány megállapította, hogy az ACS-betegek mindössze 73% – a töltötte ki a mentesítési előírásokat 1 héttel a kórházi mentesítés után, és az 1 éves halálozási arány magasabb volt azoknál a betegeknél, akik egyiket sem töltötték be, szemben néhány vagy az összes receptjükkel.21 a másodlagos adherencia (azaz a gyógyszeres kezelés folytatása) alacsonynak bizonyult az ACS-betegek számos vizsgálatában, a betegek kevesebb, mint 45%-a béta-blokkolót vagy sztatin-terápiát alkalmazott 1-2 évvel az ACS esemény után.22 Az alacsony tapadás lehetséges okai betegenként eltérőek lehetnek, de magukban foglalhatják a motiváció hiányát, a feledékenységet, a gyógyszeres oktatás hiányát, a depressziót, a kezelési komplexitást és a káros hatásokat; emellett az idősebb betegek és a társbetegségben szenvedők gyakran kevésbé ragaszkodnak.22 a gyógyszerészek kulcsszerepet játszhatnak a betegek oktatásában azáltal, hogy elmagyarázzák az egyes gyógyszerek szükségességét és a káros hatások jeleit, közvetlenül arra ösztönzik a beteget, hogy töltse fel a receptet, és a járóbeteg-gyógyszertár újratöltési emlékeztetőket biztosít, és figyelemmel kíséri a betartást.
amellett, hogy segíti a tapadást, a gyógyszerészek segíthetnek abban, hogy betegeiknek minden alapvető gyógyszert felírjanak a betegség minden szakaszában. Értékelhetik a gyógyszerkölcsönhatásokat, és adott esetben alternatív szereket javasolhatnak (pl. a klopidogrélt szedő betegek nem kaphatnak omeprazolt vagy ezomeprazolt, ami jelentősen csökkenti a thrombocyta-gátló aktivitást).11 gyógyszerész oktathatja a betegeket a gyógyszerekről, a gyakori káros hatásokról és a megfelelő életmód-módosításokról.6
1. Benjamin EJ, Muntner P, Alonso a, et al. Szívbetegség és stroke statisztikák—2019 frissítés: az American Heart Association jelentése. Keringés. 2019;139: e56-e528.
2. Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA / ACC iránymutatás a nem St-Elevációjú akut koszorúér szindrómában szenvedő betegek kezelésére: az American College of Cardiology/American Heart Association munkacsoport jelentése a gyakorlati Irányelvekről. J Am Coll Cardiol. 2014; 64: e139-e228.
3. Makki N, Brennan TM, Girotra S. akut koszorúér-szindróma. J Intenzív Ellátás Med. 2015;30:186-200.
4. O ‘ Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF / AHA iránymutatás az ST-elevációs miokardiális infarktus kezelésére: az American College of Cardiology Foundation/American Heart Association munkacsoport jelentése a gyakorlati Irányelvekről. J Am Coll Cardiol. 2013; 61: e78-e140.
5. Levine GN, Bates ER, Bittl JA, et al. A 2016. évi ACC/AHA iránymutatás a kettős vérlemezke-gátló terápia időtartamára összpontosított koszorúér-betegségben szenvedő betegeknél: az American College of Cardiology/American Heart Association munkacsoport jelentése a klinikai gyakorlati Irányelvekről. J Am Coll Cardiol. 2016;68:1082-1115.
6. Smith SC Jr, Benjamin EJ, Bonow RO, et al. AHA / ACCF másodlagos prevenciós és kockázatcsökkentő terápia koszorúér-és egyéb ateroszklerotikus érbetegségben szenvedő betegek számára: 2011 frissítés: az American Heart Association és az American College of Cardiology Foundation iránymutatása. Keringés. 2011;124:2458-2473.
7. Switaj TL, Christensen SR, Brewer DM. Akut koszorúér-szindróma: jelenlegi kezelés. Fam Orvos Vagyok. 2017;95:232-240.
8. TNKase (tenecteplase) betegtájékoztató. Dél-San Francisco, Kalifornia: Genentech, Inc; 2018. augusztus.
9. Retavase (reteplase) betegtájékoztató. Cary, NC: Chiesi USA, Inc; június 2017.
10. Activase (alteplase) betegtájékoztató. Dél-San Francisco, Kalifornia: Genentech, Inc; 2018. február.
11. Plavix (klopidogrél) használati utasítás. Bridgewater, NJ: Bristol-Myers Squibb / Sanofi Pharmaceuticals partnerség; 2019. május.
12. Effient (prasugrel) használati utasítás. Indianapolis, IN: Eli Lilly and Co; 2019. március.
13. Brilinta (ticagrelor) használati utasítás. Wilmington, DE: AstraZeneca Pharmaceuticals LP; 2019. október.
14. Kengreal (cangrelor) használati utasítás. Cary, NC: Chiesi USA, Inc; 2019. október.
15. Yusuf S, Zhao F, Mehta SR, et al. A klopidogrél hatása az aszpirin mellett akut koronária szindrómában szenvedő betegeknél ST-szegmens emelkedés nélkül. N Engl J Med. 2001;345:494-502.
16. Szummer K, Jernberg T, Wallentin L. a korai farmakológiától a legújabb farmakológiai beavatkozásokig akut koszorúér-szindrómákban: JACC korszerű áttekintés. J Am Coll Cardiol. 2019;74:1618-1636.
17. ReoPro (abciximab) betegtájékoztató. Horsham, PA: Janssen Biotech, Inc; június 2018.
18. Aggrastat (tirofiban) használati utasítás. Princeton, NJ: Medicure Pharma, Inc; 2019. május.
19. Integrilin (eptifibatid) használati utasítás. Whitehouse állomás, NJ: Merck & Co, Inc; 2019. október.
20. Angiomax (bivalirudin) betegtájékoztató. Parsippany, NJ: a gyógyszerek Co; 2016. március.
21. Jackevicius CA, Li P, Tu JV. Az akut miokardiális infarktus utáni primer nonadherencia prevalenciája, prediktorai és kimenetele. Keringés. 2008;117:1028-1036.
22. Cheng K, Ingram N, Keenan J, Choudhury RP. Az akut koszorúér-szindrómák utáni másodlagos megelőzés gyenge betartásának bizonyítéka: lehetséges gyógymódok új technológiák alkalmazásával. Nyitott Szív. 2015;2: e000166.
23. Heparin sodium injection package insert. New York, NY: Pfizer Inc; September 2019.
24. Lovenox (enoxaparin) package insert. Bridgewater, NJ: Sanofi-aventis US LLC; December 2018.
25. Arixtra (fondaparinux) package insert. Rockford, IL: Mylan Institutional LLC; August 2017.