![]()
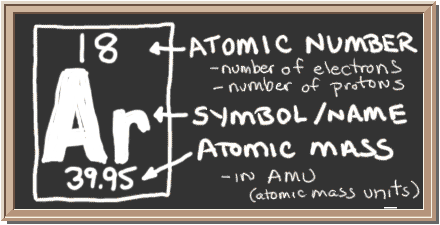
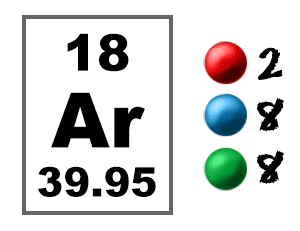
nézd meg a táblát. A bal oldali doboz tartalmazza az összes információt, amelyet tudnia kell egy elemről. Megmondja egy atom tömegét, hány darab van benne, és hol kell elhelyezni a periódusos rendszerben.
a következő részben az elektron pályákat vagy elektronhéjakat fogjuk lefedni. Lehet, hogy ez egy új téma néhányatok számára.
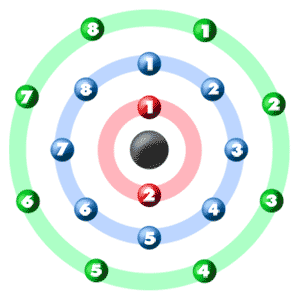
nézze meg az alábbi képet. Mindegyik színes golyó egy elektron. Egy atomban az elektronok a központ körül forognak,más néven a mag. Az elektronok szeretnek külön héjakban/pályákon lenni. Az első számú héj csak 2 elektront képes befogadni, a második héj 8-at, az első tizennyolc elemnél pedig a harmadik héj legfeljebb nyolc elektront képes befogadni. Amint megismered a tizennyolc elektronnál több elemet, rájössz, hogy a harmadik héj több mint nyolcat képes befogadni. Miután az egyik héj megtelt, a következő hozzáadott elektronnak át kell lépnie a következő héjra.
tehát… az ARGON eleméhez már tudja, hogy az atomszám megmondja az elektronok számát. Ez azt jelenti, hogy 18 elektron van egy argonatomban. A képet nézve láthatjuk, hogy az egyes héjban két elektron van, a kettesben nyolc, a harmadikban pedig nyolc.