La maggior parte delle infezioni batteriche possono essere trattati con antibiotici come la penicillina, scoperto decenni fa. Tuttavia, tali farmaci sono inutili contro le infezioni virali, tra cui l’influenza, il comune raffreddore e le febbri emorragiche mortali come l’Ebola.
Ora, in uno sviluppo che potrebbe trasformare il modo in cui le infezioni virali vengono trattate, un team di ricercatori del Lincoln Laboratory del MIT ha progettato un farmaco in grado di identificare le cellule che sono state infettate da qualsiasi tipo di virus, quindi uccidere quelle cellule per terminare l’infezione.
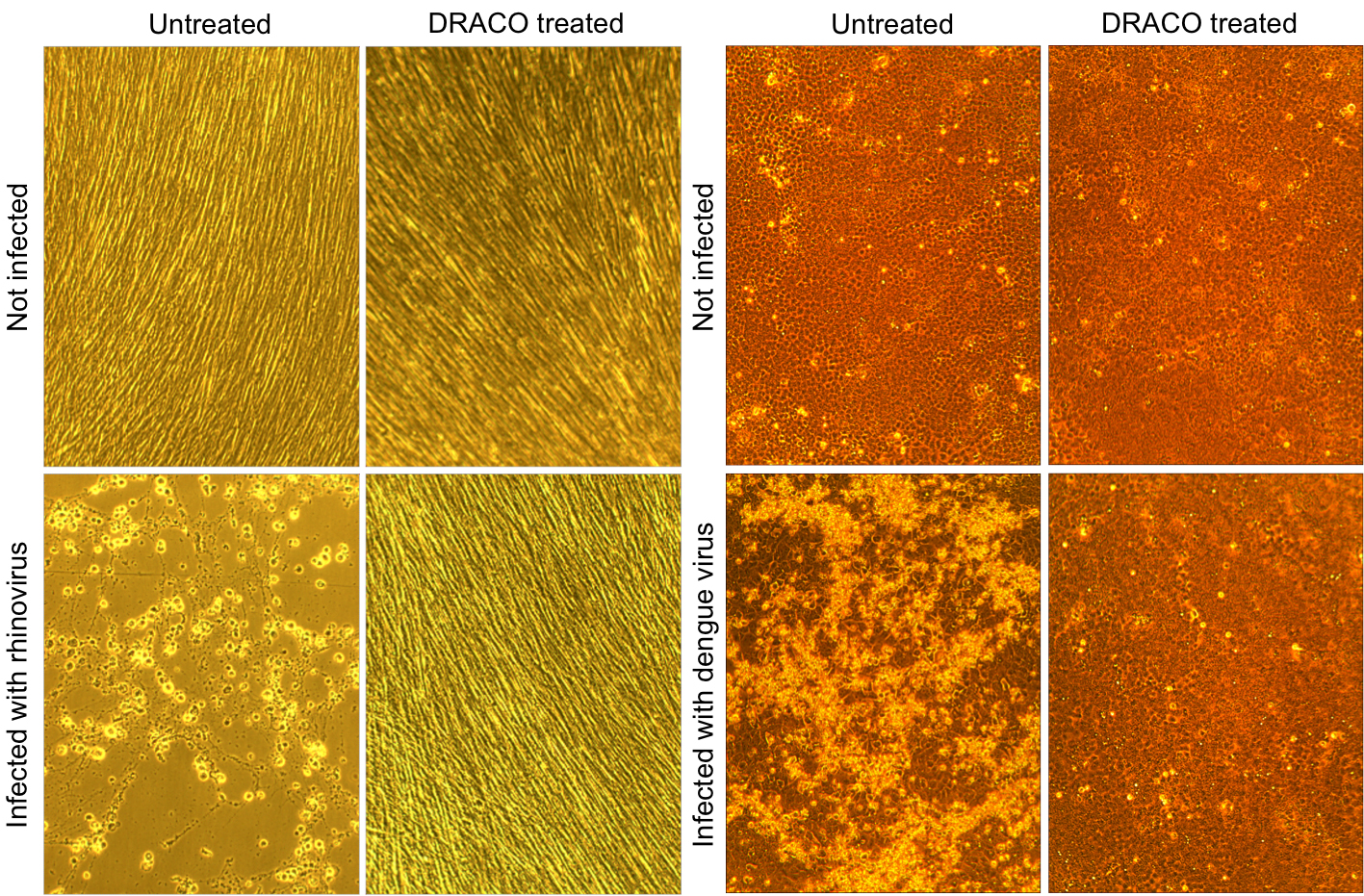
Le immagini al microscopio sopra riportate mostrano che DRACO tratta con successo le infezioni virali. Nella serie di quattro foto a sinistra, il rhinovirus (il virus del raffreddore comune) uccide le cellule umane non trattate (in basso a sinistra), mentre DRACO non ha tossicità nelle cellule non infette (in alto a destra) e cura una popolazione di cellule infette (in basso a destra). Allo stesso modo, nel giusto set di quattro foto, il virus della febbre emorragica dengue uccide le cellule di scimmia non trattate (in basso a sinistra), mentre DRACO non ha tossicità nelle cellule non infette (in alto a destra) e cura una popolazione di cellule infette (in basso a destra). | Ingrandire l’immagine
In un articolo pubblicato il 27 luglio sulla rivista PLoS One, i ricercatori hanno testato il loro farmaco contro 15 virus, e l’ho trovato era efficace contro tutti — compresi i rinovirus che causa il comune raffreddore, l’influenza H1N1, un virus allo stomaco, un virus della poliomielite, febbre dengue e molti altri tipi di febbre emorragica.
Il farmaco funziona prendendo di mira un tipo di RNA prodotto solo in cellule che sono state infettate da virus. ” In teoria, dovrebbe funzionare contro tutti i virus”, afferma Todd Rider, uno scienziato senior del Lincoln Laboratory Chemical, Biological and Nanoscale Technologies Group che ha inventato la nuova tecnologia.
Perché la tecnologia è così ampio spettro, potrebbe potenzialmente essere utilizzato anche per combattere focolai di nuovi virus, come la SARS 2003 (sindrome respiratoria acuta grave) focolaio, Rider dice.
Altri membri del gruppo di ricerca sono membri dello staff del Lincoln Lab Scott Wick, Christina Zook, Tara Boettcher, Jennifer Pancoast e Benjamin Zusman.
Pochi antivirali disponibili
Rider ha avuto l’idea di provare a sviluppare una terapia antivirale ad ampio spettro circa 11 anni fa, dopo aver inventato CANARY (Analisi cellulare e notifica dei rischi e delle rese dell’antigene), un biosensore in grado di identificare rapidamente gli agenti patogeni. “Se rilevi un batterio patogeno nell’ambiente, probabilmente c’è un antibiotico che potrebbe essere usato per trattare qualcuno esposto a questo, ma mi sono reso conto che ci sono pochissimi trattamenti là fuori per i virus”, dice.
Ci sono una manciata di farmaci che combattono virus specifici, come gli inibitori della proteasi utilizzati per controllare l’infezione da HIV, ma questi sono relativamente pochi in numero e suscettibili di resistenza virale.
Rider trasse ispirazione per i suoi agenti terapeutici, soprannominati DRACOs (oligomerizzatori Caspasi attivati a doppio filamento di RNA), dai sistemi di difesa delle cellule viventi.
Quando i virus infettano una cellula, prendono in consegna il suo macchinario cellulare per il proprio scopo — cioè, la creazione di più copie del virus. Durante questo processo, i virus creano lunghe stringhe di RNA a doppio filamento (dsRNA), che non si trova nelle cellule umane o di altri animali.
Come parte delle loro difese naturali contro l’infezione virale, le cellule umane hanno proteine che si attaccano al dsRNA, innescando una cascata di reazioni che impedisce al virus di replicarsi. Tuttavia, molti virus possono superare in astuzia quel sistema bloccando uno dei passaggi più in basso la cascata.
Rider ha avuto l’idea di combinare una proteina dsRNA-binding con un’altra proteina che induce le cellule a subire apoptosi (suicidio cellulare programmato) — lanciato, per esempio, quando una cellula determina che è in rotta per diventare cancerose. Pertanto, quando un’estremità del DRACO si lega al dsRNA, segnala l’altra estremità del DRACO per avviare il suicidio cellulare.
Combinare questi due elementi è una “grande idea” e un approccio molto nuovo, dice Karla Kirkegaard, professore di microbiologia e immunologia alla Stanford University. “I virus sono abbastanza bravi a sviluppare la resistenza alle cose che proviamo contro di loro, ma in questo caso è difficile pensare a un semplice percorso per la resistenza ai farmaci”, dice.
Ogni DRACO include anche un “tag di consegna”, preso da proteine presenti in natura, che gli consente di attraversare le membrane cellulari ed entrare in qualsiasi cellula umana o animale. Tuttavia, se non è presente dsRNA, DRACO lascia la cellula illesa.
La maggior parte dei test riportati in questo studio sono stati fatti in cellule umane e animali coltivate in laboratorio, ma i ricercatori hanno anche testato DRACO in topi infettati con il virus dell’influenza H1N1. Quando i topi sono stati trattati con DRACO, sono stati completamente guariti dall’infezione. I test hanno anche dimostrato che DRACO stesso non è tossico per i topi.
I ricercatori stanno ora testando DRACO contro più virus nei topi e iniziando a ottenere risultati promettenti. Rider dice che spera di concedere in licenza la tecnologia per le prove in animali più grandi e per eventuali studi clinici umani.
Questo lavoro è finanziato da una sovvenzione da parte del National Institute of Allergy e Malattie Infettive e il New England, Centro Regionale di Eccellenza per la Biodifesa e Malattie Infettive Emergenti, con precedenti finanziamenti dalla Defense Advanced Research Projects Agency, Defense Threat Reduction Agency, e il Direttore della Defense Research & Ingegneria (ora Assistente del Segretario della Difesa per la Ricerca e l’Ingegneria).