Supponiamo di avere questo alogenuro alchilico e di dover determinare tutti i prodotti di una reazione E2 quando viene trattata con una base forte come l’etossido di sodio.
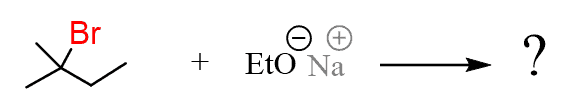
Ricorda nelle reazioni E2, per prima cosa identifichiamo tutti gli idrogeni β e disegniamo i prodotti di eliminazione in base a ciascun insieme di questi idrogeni β. In questo caso, abbiamo β idrogeni sul lato destro del gruppo di partenza (Br) e sui due gruppi metilici.
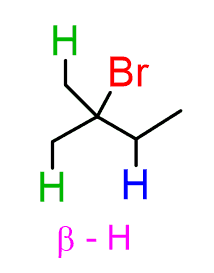
Così, un prodotto sta per essere l’alchene in cui il doppio legame è nel mezzo:
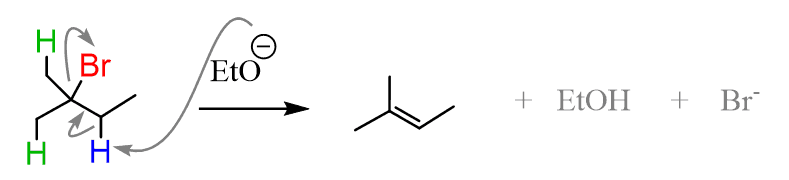
d’altra parte, gli atomi di idrogeno in ogni gruppo metilico dare la stessa alchene, poiché essi sono equivalenti come confermato dal piano di simmetria e la struttura degli alcheni:
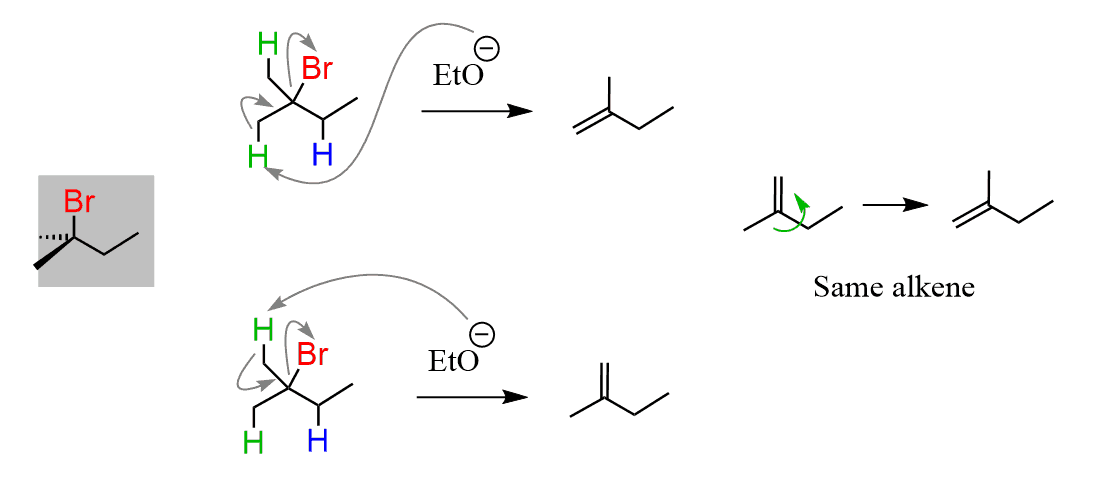
Ciò che è interessante è che si scopre che solo uno di questi due alcheni è il principale prodotto. Il rapporto è di circa 80: 20 a favore dell’alchene più sostituito:

La ragione di ciò è la stabilità degli alcheni. Ricorda che gli alcheni più sostituiti sono più stabili. L’aggiunta di gruppi sul doppio legame aumenta la stabilità dell’alchene:

Ora, controllando i nostri prodotti, possiamo vedere che è una miscela di un alchene trisostituito con un alchene disostituito e l’alchene trisostituito è il prodotto principale di questa reazione di eliminazione:
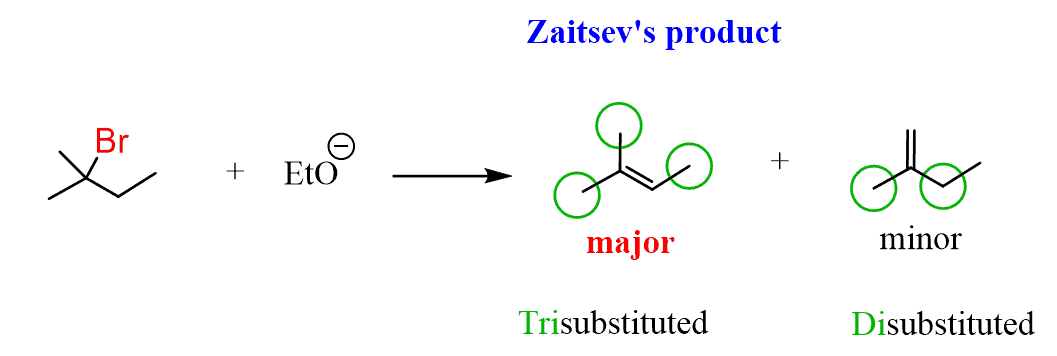
Quindi, l’alchene più sostituito è il principale prodotto dell’eliminazione di E2 a causa della sua maggiore stabilità.
Il chimico russo Alexander Zaitsev è stato il primo ad osservare questo schema e la reazione prende il nome da lui. La regola di Zaitsev afferma che in una reazione di eliminazione, l’alchene più sostituito è il prodotto principale.
La regola di Zaitsev non è sempre seguita nelle reazioni E2.
Ad esempio, se trattiamo lo stesso alogenuro alchilico con una base stericamente ostacolata (grande/ingombrante) come ad esempio il terz-butossido di potassio, vediamo la tendenza opposta. L’alchene meno sostituito è il prodotto principale nonostante sia meno stabile.
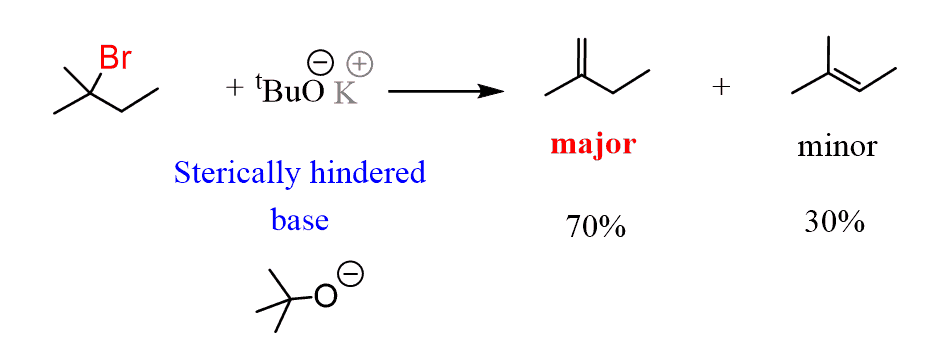
Questo è noto come la regola di Hoffman che afferma che se trattiamo l’alogenuro alchilico (o altri substrati adatti) con una forte base stericamente ostacolata, il prodotto principale sarà l’alchene meno sostituito.
La ragione di ciò è che è più facile per la base ingombrante accedere ai protoni che non sono ostacolati da altri carboni.
E poiché i protoni dei gruppi metilici sono più accessibili dei protoni del gruppo CH2, l’alchene meno sostituito si forma più velocemente ed è il prodotto principale in questo caso.
Quindi, per riassumere, se hai bisogno dell’alchene più sostituito, usa una base stericamente non ostacolata.
Se l’alchene sostituito dalle fecce è il bersaglio, utilizzare una base stericamente ostacolata.

Le basi stericamente ostacolate e non ostacolate più comuni sono mostrate sopra.
Queste due regole sono molto applicabili nella sintesi organica perché permettono di controllare quale alchene vogliamo sintetizzare. E questi alcheni possono essere ulteriormente utilizzati per la preparazione di altri prodotti.
Regioselettività della reazione E2
Le regole di Zaitsev e Hoffman dimostrano il principio della regioselettività nelle reazioni di eliminazione.
Regioselettivo significa che la reazione produce selettivamente un regioisomero come prodotto principale. I due alcheni sono regioisomeri poiché i doppi legami si trovano in regioni diverse. Questo è un modo per ricordare questo, ma anche notare che gli alcheni sono isomeri costituzionali. Quindi la regioselettività è la formazione preferita di un isomero costituzionale.