加熱曲線
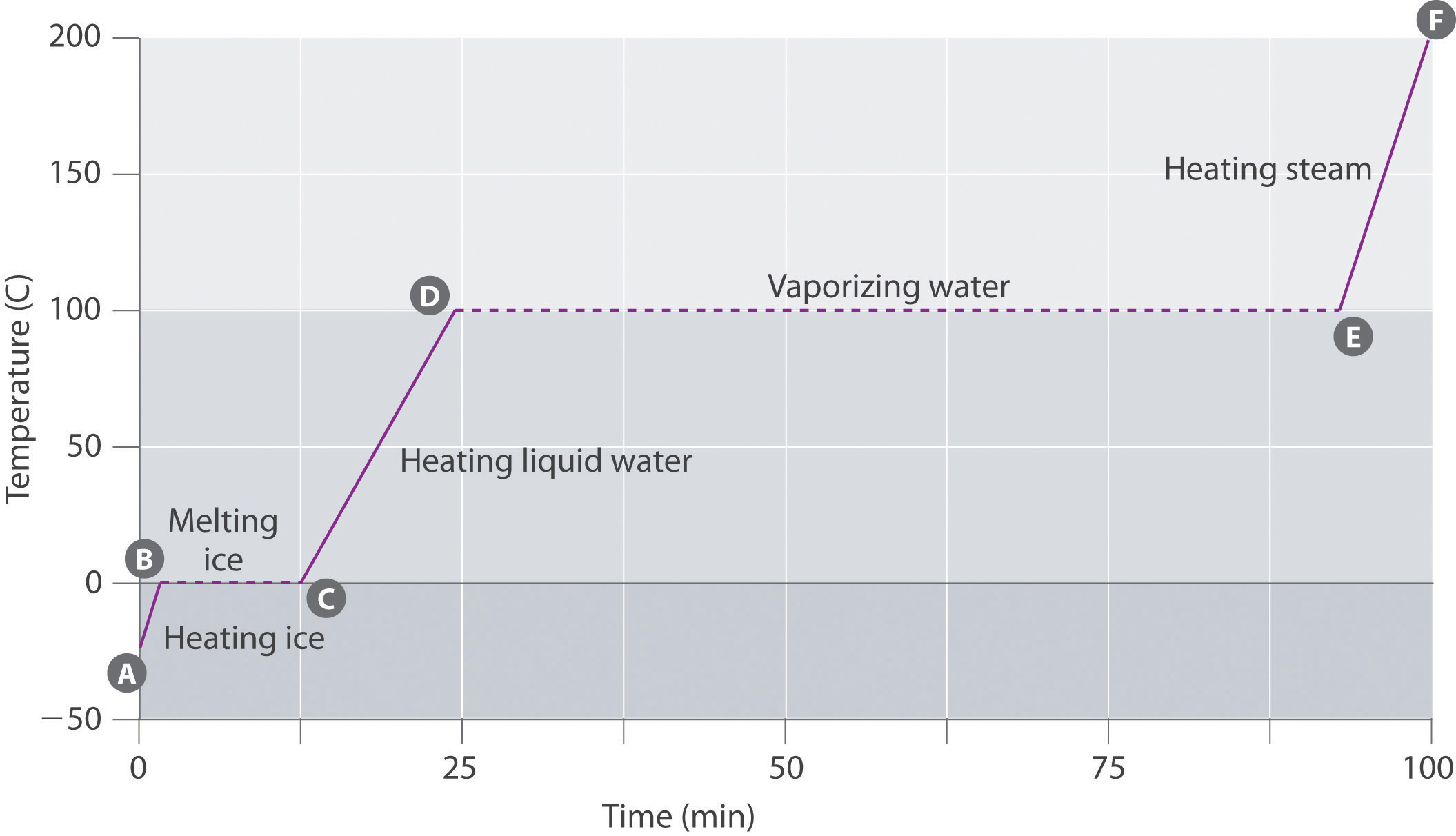
図\(\PageIndex{3}\)は、水の75gのサンプルのための加熱曲線、温度対加熱時間のプロッ サンプルは最初に1気圧および-23°Cに氷である;熱が加えられると同時に、氷の温度は時間と直線的に増加する。 線の傾きは、氷の質量と氷の比熱(Cs)の両方に依存し、これは1gの氷の温度を1℃上昇させるのに必要なジュール数である。 氷の温度が上昇するにつれて、氷の結晶中の水分子はますます多くのエネルギーを吸収し、より激しく振動する。 融点では、それらは引力を克服して互いに移動するのに十分な運動エネルギーを有する。 より多くの熱が加えられると同時に、システムの温度はそれ以上増加しないが、すべての氷が溶けたまで0°Cで一定している残る。 すべての氷が液体の水に変換されると、水の温度が再び上昇し始めます。 しかし、今では、水の比熱容量が氷の比熱容量よりも大きいため、温度は以前よりもゆっくりと上昇します。 水の温度が100℃に達すると、水は沸騰し始める。 ここでも、すべての水が蒸気に変換されるまで、温度は100℃で一定のままです。 この時点で、温度は再び上昇し始めますが、蒸気の熱容量が氷または水の熱容量よりも小さいため、他の相よりも速い速度で上昇します。P>
したがって、システムの温度は相変化中に変化しません。 この例では、少量の氷が存在する限り、系の温度は溶融プロセス中に0℃のままであり、少量の液体水が存在する限り、系の温度は沸騰プロセス中に100℃のままである。 熱が加えられる率は氷/水または水/蒸気の混合物の温度に影響を与えません加えられた熱がより凝縮させた段階を一緒に握る引力を克服するのに 多くの料理人は、熱が高くなって水がより急速に沸騰すると、食べ物がより速く調理されると考えています。 代わりに、水の鍋はすぐに乾燥するまで沸騰しますが、水の温度はそれがどれくらい激しく沸騰するかに依存しません。
サンプルの温度は相変化中に変化しません。
図\(\PageIndex{3}\)のように一定の速度で熱を加えると、温度が変化しない時間を表す水平線の長さは、相変化に関連するエンタルピーの大きさに正 図\(\PageIndex{3}\)では、水の蒸発エンタルピーが融合エンタルピーの数倍であるため、100°Cでの水平線は0°Cでの線よりもはるかに長い。
過熱液体は、それがガスであるべき温度と圧力で液体のサンプルです。
過熱液体は、それがガスであるべき温度と圧力で液体のサンプルです。
過熱された液体は安定していません;液体は最終的に、時々激しく沸騰します。 過熱の現象は、液体が実験室で加熱されると”ぶつかる”原因となる。 例えば、水を含む試験管をブンゼンバーナー上で加熱すると、液体の一部が容易に熱くなりすぎる可能性がある。 過熱された液体がガスに変えるとき、試験管から液体の残りを押すか、または”ぶつかる”ことができます。 攪拌棒またはセラミックの小片(「沸騰チップ」)を試験管に配置すると、蒸気の泡が物体の表面に形成され、液体が過熱するのではなく沸騰するように 過熱は、電子レンジで滑らかなカップで加熱された液体が、カップの動きが気泡を形成することを可能にするときに、カップが動くまで沸騰しない