イオンの電子配置を見つけなければならないときの良い出発点は、中性原子の電子配置です。 あなたの場合、フッ化物アニオンの電子配置#”F”^(-)#を見つけなければならないので、中性フッ素原子の電子配置#”F”#を書くことから始めてください。 フッ素は周期2、周期表の第17族に位置し、原子番号は#9#です。
フッ素は周期2、周期表の第17族に位置し、原子番号は#9#です。
フッ素は周期 これは、中性フッ素原子は、その核を囲む#9#電子の合計を持っていることを示しています。
その電子配置は次のようになります
#”F:”1s^2 2s^2 2p^5#
今、#”F”^(-)#陰イオンは#1#電子が中性フッ素原子に加 中性原子の2pサブシェルには5個の電子が含まれていることに注意してください。
中性原子の2pサブシェルには5個の電子が含まれています。 その最大容量は実際には#6#電子であり、各p軌道に2つの電子があります。 p>
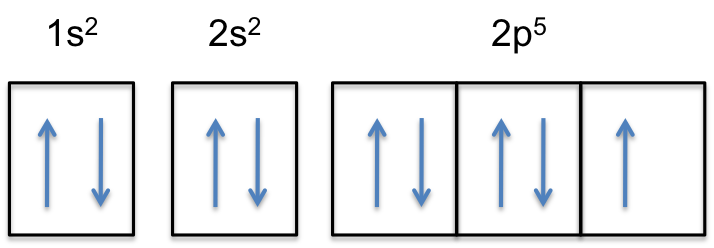
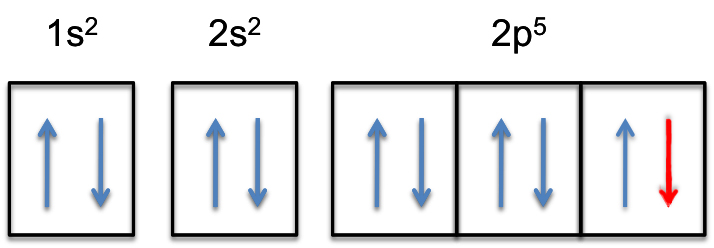
これは、#color(red)(“extra electron”)#が3つの2p軌道のいずれかに追加されることを意味します。#2p_y#としましょう。
 chemwiki.ucdavis.edu
chemwiki.ucdavis.edu
2p-subshellは完全に満たされます、つまり#6#電子を保持します。 したがって、フッ化物アニオンの電子配置は次のようになります。
#color(green)(|bar(ul(color(white)(a/a)color(black)(“F”^(-):color(white)(a)1s^2color(white)(a)2s^2color(white)(a)2p^6)color(white)(a/a)|)))#
フッ化物アニオンは、その第二の殻、最も外側の殻に合計8個の電子を有することに注意してください。 これは、アニオンが完全なオクテットを持っていることを示しています。
フッ化物アニオンはネオンと等電子であるため、#”Ne”#、あなたは希ガスの速記表記を使用してその電子配置を書くことができます
#”F”^(-):#
ここで
##-ネオンの電子配置
#”F”^(-):#
##-ネオンの電子配置