一般名:ヘパリンナトリウム
投与形態:注射
- Hep-Lock説明
- Hep-Lock-Clinical Pharmacology
- Hepロックのための徴候そして使用法
- 禁忌
- 警告
- 過敏症
- 出血
- 血小板減少症
- ヘパリン誘発性血小板減少症(HIT)およびヘパリン誘発性血小板減少症および血栓症(HITT)
- HITおよびHITTの遅延発症
- 新生児および乳児での使用
- 使用上の注意
- 一般
- 実験室試験
- 薬物相互作用
- 発癌、突然変異誘発、生殖能力の障害
- 妊娠
- 妊娠カテゴリー C
- 授乳中の母親
- 小児使用
- 高齢者の使用
- 副作用
- 出血
- 血小板減少症、ヘパリン誘発性血小板減少症(HIT)およびヘパリン誘発性血小板減少症および血栓症(HITT)およびHITおよびHITTの発症遅延
- 局所刺激
- 過敏症
- 過量投与
- 症状
- 治療–ヘパリン効果の中和
- Hep-Lock投与量および投与
- 静脈内デバイスの開存性の維持
- 血液サンプルの回収
- Hep-Lockはどのように供給されていますか
- ストレージ
Hep-Lock説明
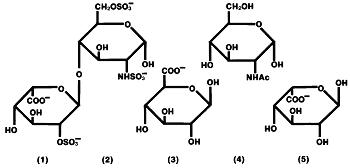
ヘパリンは、抗凝固特性を有するグリコサミノグリカンと呼ばれる直鎖アニオン性ムコ多糖類の異種群である。 他のものが存在してもよいが、ヘパリンに生じる主な糖は、(1)α-L-イデュロン酸2-硫酸、(2)2-デオキシ-2-スルファミノ-α-D-グルコース6-硫酸、(3)β-D-グルクロン酸、(4)2-アセトアミド-2-デオキシ-α-D-グルコースおよび(5)α-L-イデュロン酸である。 これらの糖は、通常、(2)>>>>(5)の順に減少量で存在し、グリコシド結合によって結合され、様々なサイズのポリマーを形成する。 ヘパリンは、共有結合した硫酸基とカルボン酸基の含有量のために強酸性である。 ヘパリンナトリウムでは、硫酸単位の酸性プロトンが部分的にナトリウムイオンに置換されている。
ヘパリンナトリウムの構造式(代表的なサブ単位):
Hep-Lock U/P(防腐剤フリーのヘパリンロックフラッシュ溶液、USP)は、静脈内フラッシュのみの滅菌溶液です。 それは抗凝固薬療法に使用されるべきではないです。 HepロックU/Pは防腐剤の使用が勧められない状態の使用のために特に作り出される。 各mLはブタの腸から得られ、注入のための水で抗凝固薬、塩化ナトリウム8mg、monobasicナトリウムの隣酸塩一水化物2.3mgおよびdibasicナトリウムの隣酸塩無水0.5mg pH5.0-7.5. 効力は、ミリグラム当たりのヘパリン活性の単位に基づいて、USP参照標準を使用する生物学的アッセイによって決定される。
Hep-Lock-Clinical Pharmacology
ヘパリンは、in vitroおよびin vivoの両方で血液の凝固およびフィブリン凝塊の形成につながる反応を阻害する。 ヘパリンは正常な凝固システムの多数の場所で機能します。 抗トロンビンIII(ヘパリン補因子)と組み合わせた少量のヘパリンは、活性化された第X因子を不活性化し、プロトロンビンのトロンビンへの変換を阻害することによって血栓症を阻害することができる。 活動的な血栓症が開発したら、ヘパリンの多量はトロンビンを不活性にし、フィブリノゲンのフィブリンへの転換を防ぐことによってそれ以上の凝固 ヘパリンはまた、フィブリン安定化因子の活性化を阻害することにより、安定したフィブリン凝塊の形成を防止する。
出血時間は通常ヘパリンの影響を受けません。 凝固時間はヘパリンの完全な治療上の線量によって延長されます;ほとんどの場合、それはヘパリンの低い線量によってmeasurably影響されません。 広範囲の用量レベルに対するヘパリン血漿濃度の時間との対数線形プロットは線形であり、ゼロ次プロセスが存在しないことを示唆している。 肝臓および網状内皮系は、生体内変換の部位である。 二相性排除曲線、急速に減少するアルファ相(t β=10分)、および40歳の後に遅いベータ相は、臓器における取り込みを示しています。 抗凝固剤半減期と濃度半減期との間に関係がないことは、ヘパリンのタンパク質結合などの因子を反映している可能性がある。
60歳以上の患者は、ヘパリンの同様の用量に続いて、60歳未満の患者と比較して、ヘパリンの血漿レベルが高く、活性化部分トロンボプラスチン時間(APTTs)が長
ヘパリンは線維素溶解活性を有さないため、既存の凝塊を溶解しない。
Hepロックのための徴候そして使用法
HepロックU/P(防腐剤なしのヘパリンロックの同じ高さの解決、USP)は断続的な注入か注入療法または血の見本抽出のために設計されている留置のvenipuncture装置の開存性を維持するように意図されている。 ヘパリンロックフラッシュ溶液は、薬物の各注射後、または実験室試験のための血液の回収後に、静脈内に装置を最初に配置した後に使用することが (使用方法については、投与量および投与、静脈内デバイスの開存性の維持を参照してください。Hep-Lock U/Pは抗凝固療法には使用しないでください。
禁忌
ヘパリンナトリウムは、以下の症状の患者には使用しないでください:重度の血小板減少症; これが播種性血管内凝固によるものである場合を除いて、制御不能な活動的な出血状態(警告を参照)。
警告
ヘパリンは筋肉内の使用のために意図されていません。
過敏症
ヘパリンに対する過敏症が文書化されている患者は、明らかに生命を脅かす状況でのみ薬物を投与すべきである。 (副作用、過敏症を参照してください。出血は、ヘパリンを投与されている患者のほぼすべての部位で起こり得る。
出血
出血は、ヘパリンを投与されている患者のほぼすべての部位で起こり得る。 ヘマトクリットの原因不明の落下、血圧の落下または他のどの原因不明の徴候も出血性のでき事の深刻な考察の原因となるべきです。
ヘパリンナトリウムは、出血の危険性が高い疾患状態では細心の注意を払って使用する必要があります。 出血の危険性の増加が存在する条件のいくつかは、
心血管
亜急性細菌性心内膜炎、重度の高血圧である。
外科的
(a)脊髄タップまたは脊髄麻酔、または(b)特に脳、脊髄、または眼を含む大手術中および直後。
外科的
特に脳、脊髄、または眼を含む大手術。
外科的
血液学的
血友病、血小板減少症およびいくつかの血管性紫斑病などの出血傾向の増加に関連する状態。
血液学的
血友病、血小板減少症およびいくつかの血管性紫斑病。
胃腸
潰瘍性病変および胃または小腸の連続的な管排液。
その他
月経、止血障害を伴う肝疾患。
血小板減少症
血小板減少症は、ヘパリンを投与された患者で発生することが報告されており、報告されている発生率は最大30%である。 血小板数は、ベースライン時およびヘパリン投与中に定期的に取得する必要があります。 軽度の血小板減少症(100,000/mm3を超える数)は、ヘパリンを継続しても安定しているか、逆になることがあります。 しかし、任意の程度の血小板減少症は密接に監視されるべきである。 カウントが100,000/mm3を下回った場合、または再発性血栓症が発症した場合(ヘパリン誘発性血小板減少症およびヘパリン誘発性血小板減少症および血栓症を参照)、ヘパリン製品を中止し、必要に応じて代替抗凝固剤を投与すべきである。
ヘパリン誘発性血小板減少症(HIT)およびヘパリン誘発性血小板減少症および血栓症(HITT)
ヘパリン誘発性血小板減少症(HIT)は、血小板の不可逆的な凝集に起因する重篤な抗体媒介反応である。 HITは静脈および幹線血栓症、ヘパリン誘発の血小板減少症および血栓症(HITT)と言われる条件の開発に進歩するかもしれません。 血栓イベントはまた、HITTのための最初の提示である可能性があります。 これらの重篤な血栓塞栓事象には、深部静脈血栓症、肺塞栓症、脳静脈血栓症、四肢虚血、脳卒中、心筋梗塞、腸間膜血栓症、腎動脈血栓症、皮膚壊死、切断につながる可能性のある四肢の壊疽、およびおそらく死が含まれる。 任意の程度の血小板減少症は密接に監視されるべきである。 血小板数が100,000/mm3を下回った場合、または再発性血栓症が発症した場合は、患者が継続的な抗凝固を必要とする場合は、ヘパリン製品を速やかに中止し、代替抗凝固剤を検討すべきである。
HITおよびHITTの遅延発症
ヘパリン誘発性血小板減少症およびヘパリン誘発性血小板減少症および血栓症は、ヘパリン療法の中止後数週間 ヘパリンの中止後に血小板減少症または血栓症を呈する患者は、HITおよびHITTについて評価されるべきである。
新生児および乳児での使用
100単位/mL濃度は、全身抗凝固のリスクのために新生児または体重が10kg未満の乳児では使用しないでくださ 治療上のヘパリンの線量が24時間の期間の幼児に与えられるかもしれないので頻繁なフラッシュを受け取っている1つのkgよりより少しの重
使用上の注意
一般
使用上の注意ヘパリンと相容れない薬物を、防腐剤を含まないヘパリンロックフラッシュ溶液を含む留置静脈内カテーテルを介して投与する場合には、注意が必要である。 (SeeDOSAGEおよび管理、静脈内装置の開存性の維持。 ヘパリン溶液中のリンの濃度は0.63mg/mLである。
血小板減少症、ヘパリン誘発性血小板減少症(HIT)およびヘパリン誘発性血小板減少症および血栓症(HITT)
SeeWARNINGS
高齢患者、特に女性へのリスクの増加
60歳以上の患者、特に女性では出血の発生率が高いことが報告されている。
実験室試験
投与経路にかかわらず、ヘパリン療法の全過程において、定期的な血小板数、血分泌、および便中の潜血検査が推奨される。 (SeeDOSAGEおよび管理。)
薬物相互作用
血小板阻害剤
アセチルサリチル酸、デキストラン、フェニルブタゾン、イブプロフェン、インドメタシン、ジピリダモール、ヒドロキシクロロキンなどの薬物は、血小板凝集反応(ヘパリン化患者の主な止血防御)を妨げる可能性があり、ヘパリンナトリウムを受けている患者には注意して使用すべきである。
他の相互作用
ジギタリス、テトラサイクリン、ニコチンまたは抗ヒスタミン薬は、ヘパリンナトリウムの抗凝固作用を部分的に打ち消す可能性がある。
発癌、突然変異誘発、生殖能力の障害
ヘパリンナトリウムの発癌性を評価するための動物における長期的な研究は行われていない。 また、突然変異誘発または生殖能力の障害に関する動物における生殖研究は行われていない。
妊娠
催奇形性効果
妊娠カテゴリー C
動物の生殖研究はヘパリンナトリウムを用いて行われていない。 また、ヘパリンナトリウムが妊娠中の女性に投与されたときに胎児の害を引き起こす可能性があるか、または再生能力に影響を与える可能性があ ヘパリンナトリウムは、明らかに必要な場合にのみ、妊娠中の女性に与えられるべきである。
非催奇形性効果
ヘパリンは胎盤障壁を通過しない。
授乳中の母親
ヘパリンはヒト乳中に排泄されない。
小児使用
小児患者における安全性および有効性は確立されていない(警告、新生児および乳児における使用を参照)。
高齢者の使用
60歳以上の患者、特に女性で出血の発生率が高いことが報告されている(臨床薬理学および注意事項、一般を参照)。
副作用
出血
出血は、ヘパリンの使用(seeWARNINGS、出血)に起因する可能性のある主な合併症です。 治療中の過度に延長された凝固時間または軽度の出血は、通常、薬物を撤回することによって制御することができる(過剰投与を参照)。
血小板減少症、ヘパリン誘発性血小板減少症(HIT)およびヘパリン誘発性血小板減少症および血栓症(HITT)およびHITおよびHITTの発症遅延
SeeWARNINGS。
局所刺激
ヘパリンロックフラッシュ溶液の使用により、局所刺激および紅斑が報告されている。
過敏症
一般化された過敏症反応が報告されており、悪寒、発熱、蕁麻疹が最も一般的な症状であり、喘息、鼻炎、流涙、頭痛、吐き気および嘔吐、ショックを含むアナフィラキシー様反応がよりまれに起こることが報告されている。 かゆみや灼熱感、特に足の足底側では、発生する可能性があります。
血小板減少症は、ヘパリンを投与された患者で発生することが報告されており、報告されている発生率は最大30%である。 しばしば軽度で明らかな臨床的意義はないが、このような血小板減少症は、皮膚壊死、四肢の壊疽などの重度の血栓塞栓性合併症を伴い、切断、心筋梗塞、肺塞栓症、脳卒中、およびおそらく死に至る可能性がある。 (警告および注意事項を参照してください。)
痛みを伴う、虚血性およびシアン化された四肢の特定のエピソードは、過去にアレルギー性血管攣縮反応に起因している。 これらが実際に血小板減少症に関連する合併症と同一であるかどうかは、依然として決定されていない。
過量投与
症状
出血はヘパリン過量投与の主な兆候です。 鼻血、尿中の血液またはタール便は、出血の最初の兆候として注目されることがあります。 容易なあざや点状の形成は、率直な出血に先行する可能性があります。
治療–ヘパリン効果の中和
臨床状況(出血)がヘパリン化の逆転を必要とする場合、遅い注入による硫酸プロタミン(1%溶液)はヘパリンナトリウム 任意の10分の期間に、50mg以下を非常にゆっくりと投与すべきである。 プロタミンの硫酸塩の各mgはおよそ100つのUSPのヘパリンの単位を中和します。 必要なプロタミンの量はヘパリンが新陳代謝すると同時にそのうちに減ります。 ヘパリンの代謝は複雑であるが、プロタミン用量を選択する目的で、静脈内注射後約1/2時間の半減期を有すると仮定することができる。
硫酸プロタミンの投与は、重度の低血圧およびアナフィラキシー様反応を引き起こす可能性がある。 しばしばアナフィラキシーに似た致命的な反応が報告されているため、蘇生技術とアナフィラキシー様ショックの治療が容易に利用可能な場合にのみ、薬剤を投与すべきである。
追加情報については、硫酸プロタミン注射、USP製品の標識を参照してください。
Hep-Lock投与量および投与
非経口医薬品は、溶液および容器が許可するときはいつでも、投与前に粒子状物質および変色について視覚的に検査 わずかな変色は効力を変えない。
100単位/mL濃度の防腐剤フリーのヘパリンロックフラッシュ溶液は、新生児および乳児での使用には推奨されません(警告、新生児および乳児での使
静脈内デバイスの開存性の維持
ヘパリンロックセットまたは中心静脈カテーテルにおける血餅形成を防止するために、ヘパリンロックフラッシュ溶液を適切に挿入した後、USPは、デバイス全体を満たすのに十分な量で注射ハブを介して注入される。 この解決策は、デバイスが使用されるたびに交換する必要があります。 針またはカテーテルの先端の開存性そして位置を確認するために装置によって解決を管理する前の吸引物。 管理されるべき薬剤がヘパリンと互換性がなければ薬物が管理される前後に全体の装置は正常な塩と洗い流されるべきです;第2塩のフラッシュの後で、ヘパリンロックの同じ高さの解決、USPは装置に再注入されるかもしれません。 装置製造業者の指示は使用に関する細目のために相談されるべきです。 通常この希薄なヘパリンの解決は4時間まで装置内の抗凝固を維持します。
注:ヘパリンの少量の繰り返し注射は、活性化部分トロンボプラスチン時間(APTT)の試験を変更することができるので、APTTのベースライン値は、静脈内装
血液サンプルの回収
防腐剤フリーのヘパリンロックフラッシュ溶液、USPはまた、実験室試験のための血液の各回収後に使用することがで ヘパリンが血液検査の結果と干渉するか、または変えるとき、ヘパリンの解決は血液サンプルを撤回する前にそれを吸い出し、捨てることによって装置
Hep-Lockはどのように供給されていますか
Hep-Lock U/P(防腐剤を含まないヘパリンロックフラッシュソリューション、USP)
10USPユニット/mL
1mL DOSETTEバイアル25s(NDC0641-0272-25)
100USPユニット/mL
1mL DOSETTEバイアル25s(NDC0641-0272-25)
100USPユニット/mL
1mL DOSETTEバイアル25s(NDC0641-0272-25)
100USPユニット/mL
1mL DOSETTEバイアル25s(NDC0641-0272-25)
(NDC0641-0273-25)
ストレージ
20°-25°C(68°-77°F)で保管してください。
- 田畑T,茂仁M,楠原K,上田Y,et al. ヘパリン誘発性血小板減少症の遅延発症-症例報告-J Jpn Assn Torca Surg.1992;40(3):110-111.
- Warkentin T,Kelton J. 遅延発症ヘパリン誘発性血小板減少症および血栓症。 内科の年表。 2001;135:502-506.
- Rice L,Attisha W,Drexler A,Francis J.遅延発症ヘパリンは血小板減少症を誘発した。 内科の年代記,2002;136:210-215.
- Dieck J.,C.Rizo-Patron,et al. (1990). “ヘパリン誘発性血栓症のための新しい症状と治療の選択肢。”胸。1990;98:1524-26.
- Smythe M,Stephens J,Mattson. 遅発性ヘパリンは血小板減少症を誘発した。 救急医療の年表, 2005;45(4):417-419.
- Divgi A.(Reprint),Thumma S.,Hari P.,Friedman K.,遅延発症ヘパリン誘発性血小板減少症(HIT)ポスト血管造影肺塞栓症として文書化されていない薬物曝露後に提示します。. 血だ 2003;102(11):127b.
ESIロゴ、Hep-LockおよびDosetteは、Baxter International,Inc.の登録商標です。 またはその子会社。
Baxter Healthcare Corporation製
Deerfield,IL60015USA
製品に関するお問い合わせは1 800ANA DRUG(1-800-262-3784)
MLT-00090/6。0
| Hep-Lock U/P heparin sodium injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
| Hep-Lock U/P heparin sodium injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Baxter Healthcare Corporation
Medical Disclaimer