多くの場合、ガルバニックセルとして知られているvoltaicセルは、電気エネルギーを提供します。 このエネルギー源は、自発的な化学反応、より具体的には自発的な酸化還元反応である。その反応物のほとんどまたはすべてが生成物に変換され、化学ポテンシャルエネルギーを電気エネルギーに変換すると、電池は平らになります。
ボルタセル-基本的なプロセス
化学ポテンシャルエネルギー→電気エネルギー
ボルタセルは、電気化学セルの二つの基本電解セルでは、電気エネルギーは、非自発的な化学反応を駆動するために使用されます。例えば、水は電解槽内で水素と酸素に分割することができる。 また、充電式電池が充電されると、それは電解質電池として動作する。
基本的な電圧セル回路図

電極での自発的な酸化還元反応は電圧を生成します。正しくセットアップされて、この電圧は示されている電球のような電気装置を通して電子を、運転できますhere.In この図では、種は電子を陽極に移動させ、そこから電球を通って陰極に流れ、そこで還元をもたらす。
基本電解セル回路図
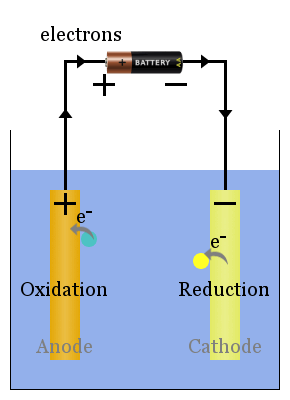
非自発的な酸化還元反応は、外部電圧によって駆動されます。電解セルのプロセスは、電源からの電流が電子を陰極に押し込み、そこで種の減少が起こる。
ボルタ対電解セルの陰極と陽極については、こちらをお読みください。
電圧セルの例
エジソン電池
エジソン電池は、トーマスによって発明された単純な、充電式セルですEdison.It 二つの金属電極、鉄、ニッケルの他の作られた一つで構成されています。最初の充満の間に、ニッケルの電極のニッケルの酸化物のコーティングは形作ります。
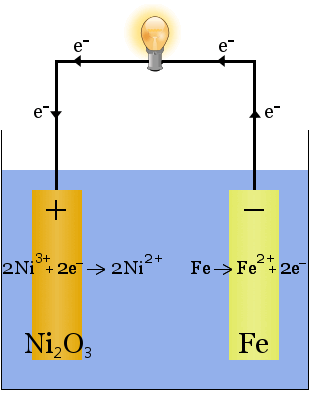
電解質(電極間のイオン液体)は、水中の水酸化カリウム20-30重量%である。この場合の水酸化カリウムの役割は、電気回路を完成させるためにイオン伝導性を高めることであり、水酸化カリウムは反応で消費されない。放電しているとき、エジソンセルはボルタセルとして動作します。
放電しているとき、エジソンセルはボルタセルとして動作します。
充電されているとき、セルは電解セルとして動作する。電極での反応の化学式は次のとおりです。
電極での反応の化学式は次のとおりです。
:
放電中、セルが電気エネルギーを供給しているとき、上記の反応は右→に進む。
充電中、セルが電気エネルギーを化学ポテンシャルエネルギーに変換しているとき、上記の反応は左πに進みます。
エジソンセルは、両方の電極が同じ電解質を共有しており、実用的な最も単純なボルタセルの一つです; ほとんどのvoltaic細胞はより複雑です。その大きい利点はほとんど無制限の充放電の循環の過充電および非常に長いワーキング-ライフのような間違いに対する驚くべき強さ、である。その最大の欠点は、そのエネルギー出力に比べて、それは非常に重い、ということです。
その最大の欠点は、そのエネルギー出力に比べて、それは非常に重
さらなる例
リチウム電池
電池技術の進歩により、電子デバイスの小型化が推進されています。これらの進歩がなければ、携帯電話やタブレットなどの最新のデバイスは、より大きく、より面倒になります。
これらの進歩の中心にリチウムイオン技術となっています。要素リチウムは非常に低密度の金属です:0.534g/cm3でリチウムは水半分密です;リチウムは水に浮かびます。これをエジソン電池の金属と比較して、ニッケルの密度は8.908g/cm3であり、鉄の密度は7.874g/cm3である:これらはリチウムの密度よりも10倍以上高い。
リチウムの高い酸化還元電位とその低密度を組み合わせることで、そのイオンは電池材料としての使用に最適です。
典型的なリチウムイオン電池は、Liイオンが細孔の内外を移動することを可能にする多孔質電極に基づいています。例えば、充電式リチウムイオン電池は、グラファイト電極と、塩Lipf6を含むポリオキシエチレン電解質を有するリチウムドープコバルト酸化物電極を有
このような電池がデバイスに電力を供給しているとき、グラファイトアノードの層構造内に保持されているリチウム原子が酸化されてイオンにな
陰極では、リチウムイオンはコバルト酸化物構造内で還元される。
These reactions are reversed when the cell is being charged.
