prawo wielu proporcji
Po pojawieniu się idei, że elementy połączone w określonych proporcjach tworzą związki, eksperymenty zaczęły również wykazywać, że te same pary pewnych elementów mogą łączyć się w więcej niż jeden związek. Rozważmy pierwiastki węgla i tlenu. Połączone w jeden sposób tworzą znany związek zwany dwutlenkiem węgla. W każdej próbce dwutlenku węgla jest \(32.0 \: \text{g}\) tlenu obecnego dla każdego \(12.0 \: \text{g}\) węgla. Dzieląc \(32,0\) przez \(12,0\), to upraszcza się do stosunku masy tlenu do węgla wynoszącego 2,66 do 1. Istnieje inny związek, który tworzy się z połączenia węgla i tlenu, zwany tlenkiem węgla. Każda próbka tlenku węgla zawiera \(16.0 \: \text{g}\) tlenu dla każdego \(12.0 \: \text{g}\) węgla. Jest to stosunek masy tlenu do węgla 1,33 do 1. W dwutlenku węgla jest dokładnie dwa razy więcej tlenu niż w tlenku węgla. Przykład ten ilustruje prawo wielorakich proporcji: gdy te same dwa pierwiastki tworzą więcej niż jeden związek, różne masy jednego pierwiastka, które łączą się z tą samą masą drugiego pierwiastka, są w stosunku małych liczb całkowitych.
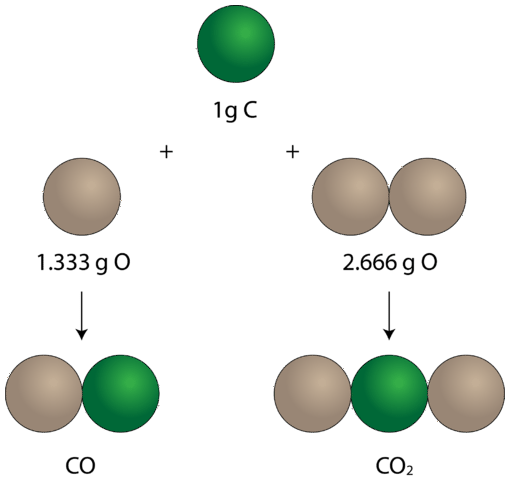
w tlenku węgla po lewej stronie znajduje się \(1.333 \: \text{g}\) tlenu dla każdego \(1 \: \text{g}\) węgla. W dwutlenku węgla, po prawej stronie, jest \(2.666\: \ text{g}\) tlenu na każdy gram węgla. Więc stosunek tlenu w tych dwóch związkach wynosi 1:2, mały stosunek liczby całkowitej.
różnica między tlenkiem węgla a dwutlenkiem węgla jest znacząca. Tlenek węgla jest śmiertelnym gazem, powstałym w wyniku niepełnego spalania niektórych materiałów zawierających węgiel (takich jak drewno i benzyna). Związek ten przyłącza się do hemoglobiny w krwinkach czerwonych i blokuje wiązanie tlenu z tymi komórkami. Jeśli tlen nie wiąże się, nie można go przenieść do komórek ciała, gdzie jest potrzebny, i może dojść do śmierci. Z drugiej strony dwutlenek węgla nie jest toksyczny jak tlenek węgla. Jednak może wyprzeć tlen w systemach, ponieważ jest cięższy. Gaśnice na dwutlenek węgla odcinają przepływ tlenu w pożarze, gasząc ogień.