większość infekcji bakteryjnych można leczyć antybiotykami, takimi jak penicylina, odkryta dziesiątki lat temu. Jednak takie leki są bezużyteczne przeciwko infekcjom wirusowym, w tym grypie, przeziębieniu i śmiertelnej gorączce krwotocznej, takiej jak Ebola.
teraz, w rozwoju, który może zmienić sposób leczenia infekcji wirusowych, zespół naukowców z laboratorium Lincolna mit zaprojektował lek, który może zidentyfikować komórki zainfekowane dowolnym typem wirusa, a następnie zabić te komórki, aby zakończyć infekcję.
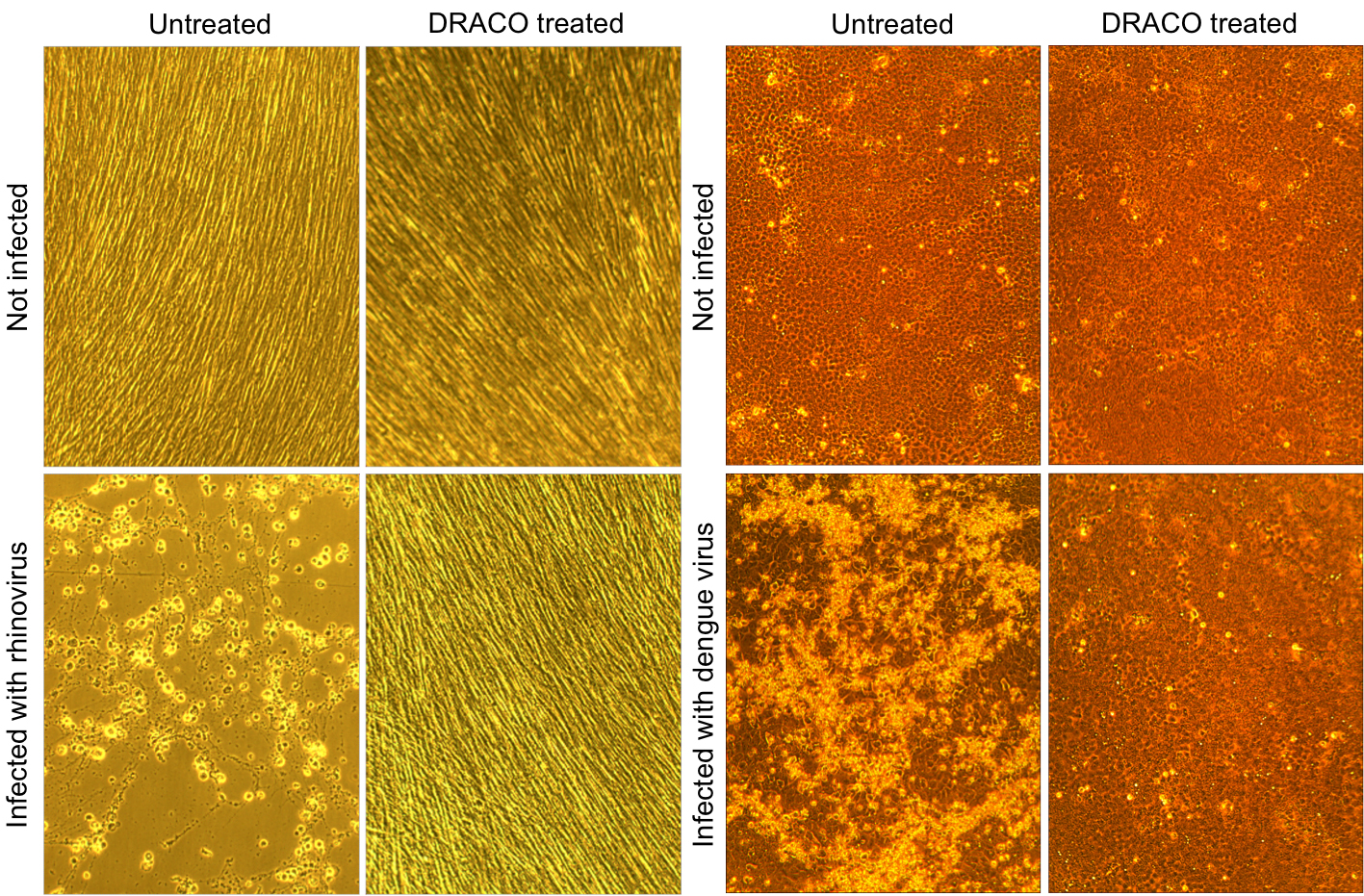
powyższe zdjęcia mikroskopowe pokazują, że DRACO skutecznie leczy infekcje wirusowe. W lewym zestawie czterech zdjęć, rhinovirus (wirus przeziębienia) zabija nieleczone komórki ludzkie (dolny lewy), podczas gdy DRACO nie ma toksyczności w niezakażonych komórkach (górny prawy) i leczy zakażoną populację komórek (dolny prawy). Podobnie, w prawym zestawie czterech zdjęć, denga wirus gorączki krwotocznej zabija nieleczone komórki małpy (lewy dolny), podczas gdy DRACO nie ma toksyczności w niezakażonych komórkach (prawy górny) i leczy zakażoną populację komórek (prawy dolny). / Powiększ zdjęcie
w artykule opublikowanym 27 lipca w czasopiśmie PLoS One naukowcy przetestowali swój lek przeciwko 15 wirusom i stwierdzili, że jest skuteczny przeciwko wszystkim z nich — w tym rinowirusom, które powodują przeziębienie, grypę H1N1, wirus żołądka, wirus polio, gorączkę dengi i kilka innych rodzajów gorączki krwotocznej.
lek działa poprzez celowanie w rodzaj RNA wytwarzanego tylko w komórkach zakażonych wirusami. „Teoretycznie powinna działać przeciwko wszystkim wirusom”, mówi Todd Rider, starszy pracownik naukowy w grupie technologii chemicznych, biologicznych i nanoskali w Lincoln Laboratory, który wynalazł nową technologię.
ponieważ technologia ma tak szerokie spektrum, potencjalnie może być również wykorzystana do zwalczania epidemii nowych wirusów, takich jak wybuch SARS (severe acute respiratory syndrome) z 2003 r., mówi Rider.
pozostali członkowie zespołu badawczego to Scott Wick, Christina Zook, Tara Boettcher, Jennifer Pancoast i Benjamin Zusman.
kilka dostępnych leków przeciwwirusowych
Rider wpadł na pomysł, aby spróbować opracować terapię przeciwwirusową o szerokim spektrum działania około 11 lat temu, po wynalezieniu CANARY (Analiza komórkowa i powiadamianie o ryzyku i plonach antygenu), biosensora, który może szybko identyfikować patogeny. „Jeśli wykryje się patogenną bakterię w środowisku, prawdopodobnie istnieje antybiotyk, który mógłby być użyty do leczenia kogoś narażonego na to, ale zdałem sobie sprawę, że istnieje bardzo niewiele metod leczenia wirusów”, mówi.
istnieje kilka leków, które zwalczają określone wirusy, takie jak inhibitory proteazy stosowane do kontrolowania zakażenia HIV, ale są one stosunkowo nieliczne i podatne na oporność wirusową.
Rider czerpał inspirację ze swoich środków terapeutycznych, nazywanych DRACOs (Dwuniciowymi aktywowanymi RNA Oligomeryzatorami kaspazy), pochodzących z systemów obronnych żywych komórek.
kiedy wirusy infekują komórkę, przejmują jej mechanizmy komórkowe dla własnego celu — czyli tworząc więcej kopii wirusa. Podczas tego procesu wirusy tworzą długie ciągi dwuniciowego RNA (dsRNA), który nie występuje w komórkach ludzkich ani innych zwierzęcych.
jako część ich naturalnej obrony przed infekcją wirusową, komórki ludzkie mają białka, które blokują się na dsRNA, uruchamiając kaskadę reakcji, która zapobiega replikacji wirusa. Jednak wiele wirusów może przechytrzyć ten system, blokując jeden z kroków dalej w dół kaskady.
Rider wpadł na pomysł połączenia białka wiążącego dsRNA z innym białkiem, które indukuje komórki do apoptozy (programmed cell suicide)-uruchamianego np. wtedy, gdy komórka stwierdza, że jest w drodze do stawania się nowotworową. Dlatego, gdy jeden koniec DRACO wiąże się z dsRNA, sygnalizuje drugi koniec DRACO, aby zainicjował samobójstwo komórkowe.
połączenie tych dwóch elementów to „świetny pomysł” i bardzo nowatorskie podejście, mówi Karla Kirkegaard, profesor mikrobiologii i immunologii na Uniwersytecie Stanforda. „Wirusy są całkiem dobre w rozwijaniu odporności na rzeczy, które staramy się przeciwko nim, ale w tym przypadku trudno jest wymyślić prostą drogę do lekooporności”, mówi.
każdy DRACO zawiera również „znacznik dostawy”, pobrany z naturalnie występujących białek, który umożliwia mu przenikanie przez błony komórkowe i przedostawanie się do dowolnej komórki ludzkiej lub zwierzęcej. Jeśli jednak nie ma dsRNA, Draco pozostawia komórkę bez szwanku.
większość testów zgłoszonych w tym badaniu przeprowadzono na komórkach ludzkich i zwierzęcych hodowanych w laboratorium, ale naukowcy testowali również DRACO na myszach zakażonych wirusem grypy H1N1. Kiedy myszy były leczone DRACO, zostały całkowicie wyleczone z infekcji. Testy wykazały również, że sam DRACO nie jest toksyczny dla myszy.
badacze testują teraz DRACO na więcej wirusów u myszy i zaczynają uzyskiwać obiecujące wyniki. Rider mówi, że ma nadzieję licencjonować technologię do badań na większych zwierzętach i do przyszłych badań klinicznych na ludziach.
praca ta jest finansowana z grantu Narodowego Instytutu Alergii i chorób zakaźnych oraz New England Regional Center Of Excellence for Biodefense and Emerging Infectious Diseases, z wcześniejszym finansowaniem Z Defense Advanced Research Projects Agency, Defense Threat Reduction Agency i dyrektora ds. badań obronnych & Engineering (obecnie asystent sekretarza obrony ds. badań i Inżynierii).