inlärningsmål
i slutet av detta avsnitt kommer du att kunna:
- förklara processerna för glykolys
- beskriv vägen för en pyruvatmolekyl genom Krebs-cykeln
- förklara transporten av elektroner genom elektrontransportkedjan
- beskriv processen för ATP-produktion genom oxidativ fosforylering
- sammanfatta processen för glukoneogenes
kolhydrater är organiska molekyler som består av kol -, väte-och syreatomer. Familjen kolhydrater innehåller både enkla och komplexa sockerarter. Glukos och fruktos är exempel på enkla sockerarter, och stärkelse, glykogen och cellulosa är alla exempel på komplexa sockerarter. De komplexa sockerarterna kallas också polysackarider och är gjorda av flera monosackaridmolekyler. Polysackarider fungerar som energilagring (t.ex. stärkelse och glykogen) och som strukturella komponenter (t. ex. kitin i insekter och cellulosa i växter).
under matsmältningen bryts kolhydrater ner i enkla, lösliga sockerarter som kan transporteras över tarmväggen in i cirkulationssystemet för att transporteras genom hela kroppen. Kolhydrat digestion börjar i munnen med verkan av salivamylas på stärkelse och slutar med att monosackarider absorberas över tunntarmens epitel. När de absorberade monosackariderna transporteras till vävnaderna börjar processen med cellulär andning (Figur 1). Detta avsnitt kommer att fokusera först på glykolys, en process där monosackaridglukosen oxideras och frigör den energi som lagras i dess bindningar för att producera ATP.
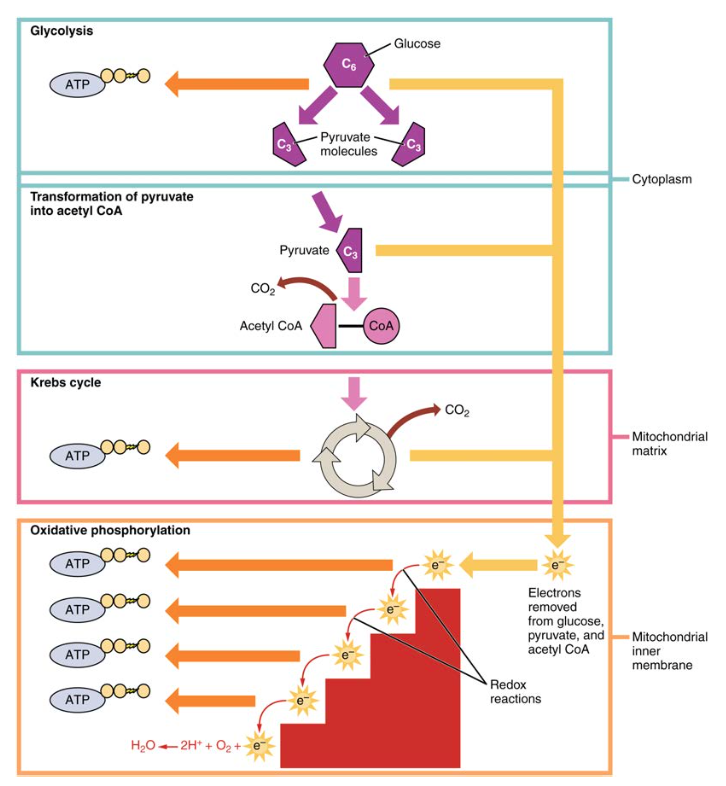
Figur 1. Cellulär andning oxiderar glukosmolekyler genom glykolys, Krebs-cykeln och oxidativ fosforylering för att producera ATP.
glykolys
glukos är kroppens mest tillgängliga energikälla. Efter matsmältningsprocesser bryter polysackarider ner i monosackarider, inklusive glukos, transporteras monosackariderna över tunntarmen och in i cirkulationssystemet, som transporterar dem till levern. I levern passerar hepatocyter antingen glukosen genom cirkulationssystemet eller lagrar överskott av glukos som glykogen. Celler i kroppen tar upp den cirkulerande glukosen som svar på insulin och överför genom en serie reaktioner som kallas glykolys en del av energin i glukos till ADP för att bilda ATP (Figur 2). Det sista steget i glykolys producerar produkten pyruvat.
glykolys börjar med fosforylering av glukos med hexokinas för att bilda glukos-6-fosfat. Detta steg använder en ATP, som är givaren av fosfatgruppen. Under verkan av fosfofruktokinas omvandlas glukos-6-fosfat till fruktos-6-fosfat. Vid denna tidpunkt donerar en andra ATP sin fosfatgrupp och bildar fruktos-1,6-bisfosfat. Detta sexkolsocker delas upp för att bilda två fosforylerade trekolmolekyler, glyceraldehyd-3-fosfat och dihydroxiacetonfosfat, som båda omvandlas till glyceraldehyd-3-fosfat. Glyceraldehyd-3-fosfatet fosforyleras ytterligare med grupper donerade av divätefosfat närvarande i cellen för att bilda trekolmolekylen 1,3-bisfosfoglycerat. Energin i denna reaktion kommer från oxidationen av (avlägsnande av elektroner från) glyceraldehyd-3-fosfat. I en serie reaktioner som leder till pyruvat överförs de två fosfatgrupperna sedan till två ADP för att bilda två ATP. Således använder glykolys två ATP men genererar fyra ATP, vilket ger en nettovinst på två ATP och två molekyler pyruvat. I närvaro av syre fortsätter pyruvat vidare till Krebs-cykeln (även kallad citronsyracykeln eller trikarboxylsyracykeln (TCA), där ytterligare energi extraheras och vidarebefordras.
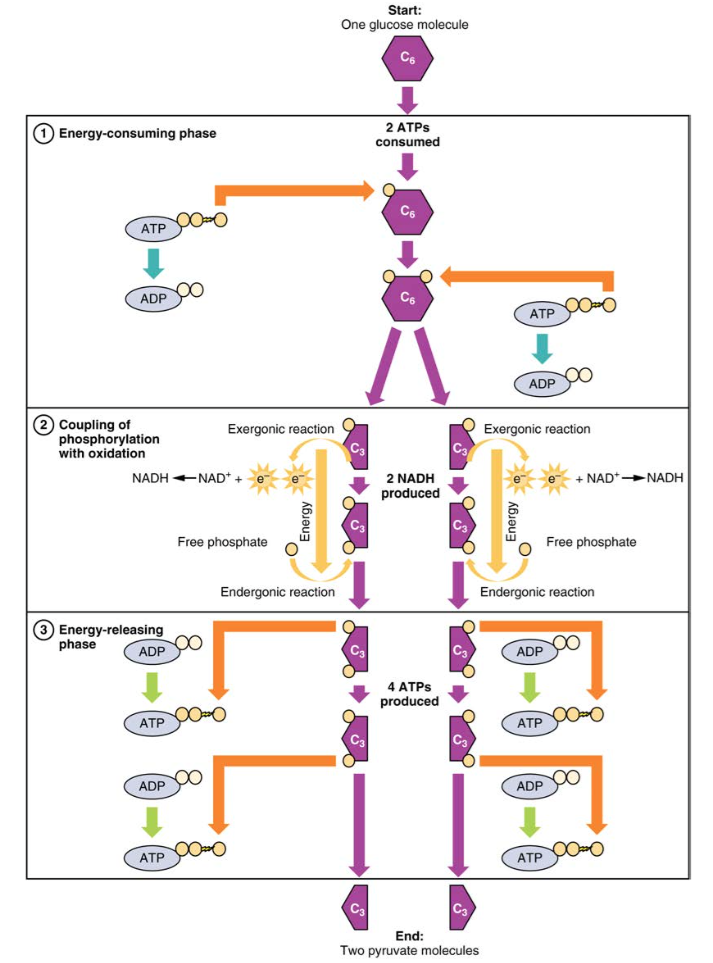
Figur 2. Under den energikrävande fasen av glykolys förbrukas två ATP, som överför två fosfater till glukosmolekylen. Glukosmolekylen delas sedan upp i två trekolföreningar, var och en innehållande ett fosfat. Under den andra fasen tillsätts ett ytterligare fosfat till var och en av trekolföreningarna. Energin för denna endergoniska reaktion tillhandahålls genom avlägsnande (oxidation) av två elektroner från varje trekolförening. Under den energifrisättande fasen avlägsnas fosfaterna från båda trekolföreningarna och används för att producera fyra ATP-molekyler.
titta på den här videon för att lära dig om glykolys:
glykolys kan delas in i två faser: energiförbrukande (även kallad kemisk priming) och energiavkastning. Den första fasen är den energikrävande fasen, så det kräver två ATP-molekyler för att starta reaktionen för varje glukosmolekyl. I slutet av reaktionen produceras emellertid fyra ATP, vilket resulterar i en nettovinst av två ATP-energimolekyler.
glykolys kan uttryckas som följande ekvation:
\text{Glucose}+2\text{ATP}+2\text{NAD}^{+}+4\text{ADP}+2\text{P}_{i}\to\text{Pyruvate}+4\text{ATP}+2\text{NADH}+2\text{H}^{+}
denna ekvation säger att glukos, i kombination med ATP (energikällan), NAD+ (ett koenzym som fungerar som en elektronacceptor) och oorganiskt fosfat, bryts ner i två pyruvatmolekyler och genererar fyra ATP—molekyler—för ett nettoutbyte av två ATP-och två ENERGIINNEHÅLLANDE NADH-koenzymer. NADH som produceras i denna process kommer att användas senare för att producera ATP i mitokondrier. Det är viktigt att i slutet av denna process genererar en glukosmolekyl två pyruvatmolekyler, två ATP-molekyler med hög energi och två elektronbärande NADH-molekyler.
följande diskussioner om glykolys inkluderar enzymerna som är ansvariga för reaktionerna. När glukos kommer in i en cell, lägger enzymet hexokinas (eller glukokinas i levern) snabbt ett fosfat för att omvandla det till glukos-6-fosfat. Ett kinas är en typ av enzym som lägger till en fosfatmolekyl i ett substrat (i detta fall glukos, men det kan också vara sant för andra molekyler). Detta omvandlingssteg kräver en ATP och fångar i huvudsak glukosen i cellen, vilket förhindrar att den passerar tillbaka genom plasmamembranet, vilket gör att glykolys kan fortsätta. Det fungerar också för att upprätthålla en koncentrationsgradient med högre glukosnivåer i blodet än i vävnaderna. Genom att fastställa denna koncentrationsgradient kommer glukosen i blodet att kunna strömma från ett område med hög koncentration (blodet) till ett område med låg koncentration (vävnaderna) som antingen ska användas eller lagras. Hexokinas finns i nästan alla vävnader i kroppen. Glukokinas uttrycks å andra sidan i vävnader som är aktiva när blodsockernivån är hög, såsom levern. Hexokinas har en högre affinitet för glukos än glukokinas och kan därför omvandla glukos i snabbare takt än glukokinas. Detta är viktigt när glukosnivåerna är mycket låga i kroppen, eftersom det tillåter glukos att resa företrädesvis till de vävnader som kräver det mer.
i nästa steg i den första fasen av glykolys omvandlar enzymet glukos-6-fosfatisomeras glukos-6-fosfat till fruktos-6-fosfat. Liksom glukos är fruktos också ett sex kolinnehållande socker. Enzymet fosfofruktokinas-1 lägger sedan till ytterligare ett fosfat för att omvandla fruktos-6-fosfat till fruktos-1-6-bisfosfat, ytterligare sexkolsocker, med en annan ATP-molekyl. Aldolas bryter sedan ner denna fruktos-1-6-bisfosfat i två trekolmolekyler, glyceraldehyd-3-fosfat och dihydroxiacetonfosfat. Triosefosfatisomerasenzymet omvandlar sedan dihydroxiacetonfosfat till en andra glyceraldehyd-3-fosfatmolekyl. Därför bryts en glukosmolekyl i slutet av denna kemiska priming eller energikrävande fas ned i två glyceraldehyd – 3-fosfatmolekyler.
den andra fasen av glykolys, den energigivande fasen, skapar den energi som är produkten av glykolys. Glyceraldehyd-3-fosfatdehydrogenas omvandlar varje tre-kol glyceraldehyd-3-fosfat som produceras under
energikrävande fas till 1,3-bisfosfoglycerat. Denna reaktion frigör en elektron som sedan plockas upp av NAD+ för att skapa en NADH-molekyl. NADH är en högenergimolekyl, som ATP, men till skillnad från ATP används den inte som energivaluta av cellen. Eftersom det finns två glyceraldehyd-3-fosfatmolekyler syntetiseras två NADH-molekyler under detta steg. Varje 1,3-bisfosfoglycerat defosforyleras därefter (dvs. ett fosfat avlägsnas) av Fosfoglyceratkinas till 3-fosfoglycerat. Varje fosfat som frigörs i denna reaktion kan omvandla en molekyl ADP till en ATP – molekyl med hög energi, vilket resulterar i en vinst på två ATP-molekyler.
enzymet fosfoglyceratmutas omvandlar sedan 3-fosfoglyceratmolekylerna till 2-fosfoglyceratmolekyler. Enolasenzymet verkar sedan på 2-fosfoglyceratmolekylerna för att omvandla dem till fosfoenolpyruvatmolekyler. Det sista steget av glykolys innefattar defosforylering av de två fosfoenolpyruvatmolekylerna med pyruvatkinas för att skapa två pyruvatmolekyler och två ATP-molekyler.
Sammanfattningsvis bryts en glukosmolekyl ner i två pyruvatmolekyler och skapar två netto ATP-molekyler och två NADH-molekyler genom glykolys. Därför genererar glykolys energi för cellen och skapar pyruvatmolekyler som kan bearbetas vidare genom den aeroba Krebs-cykeln (även kallad citronsyracykeln eller trikarboxylsyracykeln); omvandlas till mjölksyra eller alkohol (i jäst) genom jäsning; eller används senare för syntes av glukos genom glukoneogenes.
anaerob andning
när syre är begränsat eller frånvarande kommer pyruvat in i en anaerob väg. I dessa reaktioner kan pyruvat omvandlas till mjölksyra. Förutom att generera en ytterligare ATP, tjänar denna väg till att hålla pyruvatkoncentrationen låg så glykolys fortsätter, och den oxiderar NADH i NAD+ som behövs av glykolys. I denna reaktion ersätter mjölksyra syre som den slutliga elektronacceptorn. Anaerob andning förekommer i de flesta celler i kroppen när syre är begränsat eller mitokondrier är frånvarande eller icke-funktionella. Till exempel, eftersom erytrocyter (röda blodkroppar) saknar mitokondrier, måste de producera sin ATP från anaerob andning. Detta är en effektiv väg för ATP-produktion under korta perioder, allt från sekunder till några minuter. Den producerade mjölksyran diffunderar in i plasma och transporteras till levern, där den omvandlas tillbaka till pyruvat eller glukos via Cori-cykeln. På samma sätt, när en person övar, använder musklerna ATP snabbare än syre kan levereras till dem. De är beroende av glykolys och mjölksyraproduktion för snabb ATP-produktion.
aerob andning
i närvaro av syre kan pyruvat komma in i Krebs-cykeln där ytterligare energi extraheras när elektroner överförs från pyruvatet till receptorerna NAD+, BNP och FAD, med koldioxid som en ”avfallsprodukt” (Figur 3). NADH och FADH2 överför elektroner till elektrontransportkedjan, som använder den överförda energin för att producera ATP. Som terminalsteg i elektrontransportkedjan är syre den terminala elektronacceptorn och skapar vatten inuti mitokondrierna.
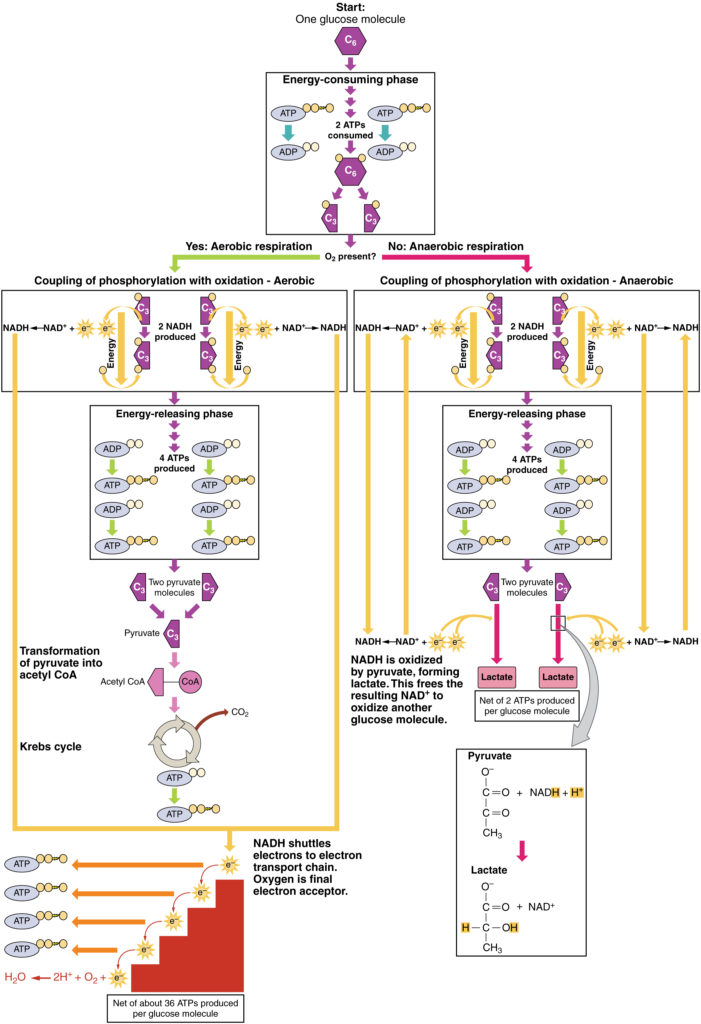
Figur 3. Klicka för att se en större bild. Processen med anaerob andning omvandlar glukos till två laktatmolekyler i frånvaro av syre eller inom erytrocyter som saknar mitokondrier. Under aerob andning oxideras glukos i två pyruvatmolekyler.
Krebs-cykel / citronsyracykel / Trikarboxylsyracykel
pyruvatmolekylerna som genereras under glykolys transporteras över mitokondriemembranet in i den inre mitokondriella matrisen, där de metaboliseras av enzymer i en väg som kallas Krebs-cykeln (Figur 4). Krebs-cykeln kallas också vanligtvis citronsyracykeln eller trikarboxylsyracykeln (TCA). Under Krebs-cykeln skapas högenergimolekyler, inklusive ATP, NADH och FADH2. NADH och FADH2 passerar sedan elektroner genom elektrontransportkedjan i mitokondrierna för att generera fler ATP-molekyler.
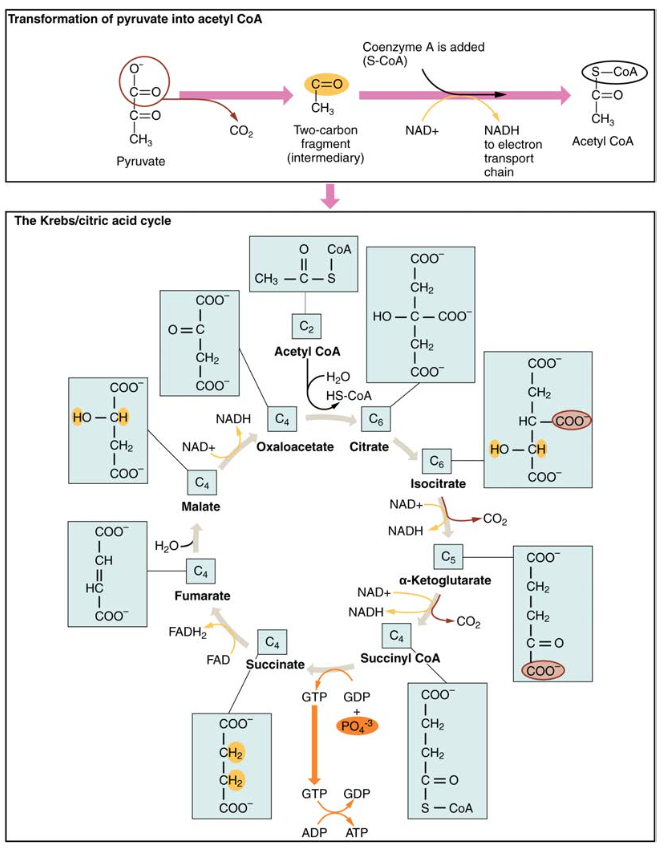
Figur 4. Under Krebs-cykeln omvandlas varje pyruvat som genereras genom glykolys till en två-kolacetyl-CoA-molekyl. Acetyl CoA bearbetas systematiskt genom cykeln och producerar NADH -, FADH2-och ATP-molekyler med hög energi.
titta på den här animationen för att observera Krebs-cykeln.
pyruvatmolekylen med tre kol som genereras under glykolys rör sig från cytoplasman till mitokondriell matris, där den omvandlas av enzymet pyruvatdehydrogenas till en två-kolacetylkoenzym a (acetyl CoA) molekyl. Denna reaktion är en oxidativ dekarboxyleringsreaktion. Den omvandlar pyruvatet med tre kol till en Coa-molekyl med två kol, frigör koldioxid och överför två elektroner som kombineras med NAD+ för att bilda NADH. Acetyl CoA går in i Krebs-cykeln genom att kombinera med en fyrkolsmolekyl, oxaloacetat, för att bilda sexkolmolekylcitrat eller citronsyra, samtidigt som koenzym A-molekylen frigörs.
sexkolcitratmolekylen omvandlas systematiskt till en femkolsmolekyl och sedan en fyrkolsmolekyl som slutar med oxaloacetat, början av cykeln. Längs vägen kommer varje citratmolekyl att producera en ATP, en FADH2 och tre NADH. FADH2 och NADH kommer in i det oxidativa fosforyleringssystemet beläget i det inre mitokondriella membranet. Dessutom levererar Krebs-cykeln utgångsmaterialen för att bearbeta och bryta ner proteiner och fetter.
för att starta Krebs-cykeln kombinerar citratsyntas acetyl-CoA och oxaloacetat för att bilda en sexkolcitratmolekyl; CoA frigörs därefter och kan kombineras med en annan pyruvatmolekyl för att börja cykeln igen. Aconitasenzymet omvandlar citrat till isocitrat. I två på varandra följande steg av oxidativ dekarboxylering produceras två molekyler av CO2 och två NADH-molekyler när isocitratdehydrogenas omvandlar isocitrat till fem-kol-Kubi-ketoglutarat, som sedan katalyseras och omvandlas till fyra-kolsuccinyl-CoA med hjälp av Kubi-ketoglutaratdehydrogenas. Enzymet succinyl CoA dehydrogenas omvandlar sedan succinyl CoA till succinat och bildar högenergimolekylen GTP, som överför sin energi till ADP för att producera ATP. Succinatdehydrogenas omvandlar sedan succinat till fumarat och bildar en molekyl av FADH2. Fumarase omvandlar sedan fumarat till malat, vilket malat dehydrogenas omvandlar sedan tillbaka till oxaloacetat samtidigt som nad+ reduceras till NADH. Oxaloacetat är sedan redo att kombineras med nästa acetyl CoA för att starta Krebs-cykeln igen (se Figur 4). För varje tur av cykeln skapas tre NADH, en ATP (genom GTP) och en FADH2. Varje kol av pyruvat omvandlas till CO2, som frigörs som en biprodukt av oxidativ (aerob) andning.
oxidativ fosforylering och elektrontransportkedjan
elektrontransportkedjan (ETC) använder NADH och FADH2 som produceras av Krebs-cykeln för att generera ATP. Elektroner från NADH och FADH2 överförs genom proteinkomplex inbäddade i det inre mitokondriella membranet genom en serie enzymatiska reaktioner. Elektrontransportkedjan består av en serie av fyra enzymkomplex (komplex i – komplex IV) och två koenzymer (ubiquinon och cytokrom c), som fungerar som elektronbärare och protonpumpar som används för att överföra H+ – joner till utrymmet mellan de inre och yttre mitokondriella membranen (Figur 5). ETC kopplar överföringen av elektroner mellan en givare (som NADH) och en elektronacceptor (som O2) med överföringen av protoner (H+ joner) över det inre mitokondriella membranet, vilket möjliggör processen för oxidativ fosforylering. I närvaro av syre passeras energi stegvis genom elektronbärarna för att gradvis samla in den energi som behövs för att fästa ett fosfat till ADP och producera ATP. Rollen av molekylärt syre, O2, är som den terminala elektronacceptorn för etc. Detta innebär att när elektronerna har passerat genom hela ETC, måste de överföras till en annan, separat molekyl. Dessa elektroner, O2 och H+ joner från matrisen kombineras för att bilda nya vattenmolekyler. Detta är grunden för ditt behov av att andas in syre. Utan syre upphör elektronflödet genom ETC.
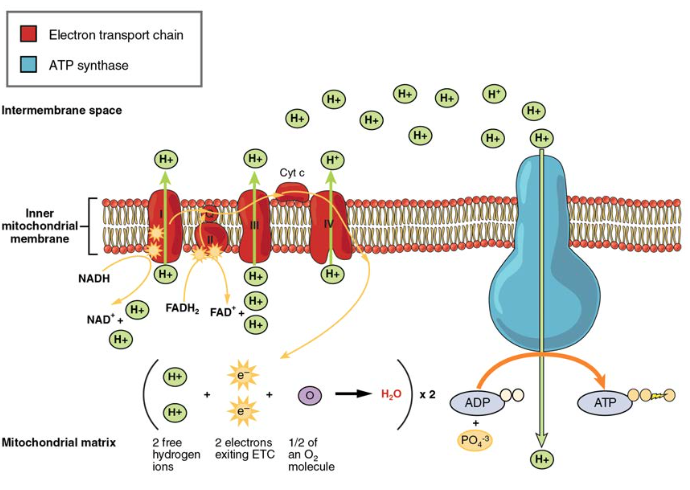
Figur 5. Elektrontransportkedjan är en serie elektronbärare och jonpumpar som används för att pumpa H+ – joner ur den inre mitokondriella matrisen.
titta på den här videon för att lära dig om elektrontransportkedjan.
elektronerna som frigörs från NADH och FADH2 passeras längs kedjan av var och en av bärarna, vilka reduceras när de tar emot elektronen och oxideras när de passerar vidare till nästa bärare. Var och en av dessa reaktioner frigör en liten mängd
energi, som används för att pumpa H+ joner över det inre membranet. Uppsamlingen av dessa protoner i utrymmet mellan membranen skapar en protongradient med avseende på mitokondriell matris.
även inbäddat i det inre mitokondriella membranet är ett fantastiskt proteinporkomplex som kallas ATP-syntas. Effektivt är det en turbin som drivs av flödet av H+ joner över det inre membranet nerför en gradient och in i mitokondriell matris. När h + – jonerna passerar komplexet roterar komplexets axel. Denna rotation gör det möjligt för andra delar av ATP-syntas att uppmuntra ADP och Pi att skapa ATP. Vid redovisning av det totala antalet ATP som produceras per glukosmolekyl genom aerob andning är det viktigt att komma ihåg följande punkter:
- ett nät av två ATP produceras genom glykolys (fyra producerade och två konsumeras under det energikrävande steget). Dessa två ATP används emellertid för att transportera NADH som produceras under glykolys från cytoplasman till mitokondrier. Därför är nettoproduktionen av ATP under glykolys noll.
- i alla faser efter glykolys måste antalet producerade ATP, NADH och FADH2 multipliceras med två för att återspegla hur varje glukosmolekyl producerar två pyruvatmolekyler.
- I ETC produceras cirka tre ATP för varje oxiderad NADH. Emellertid produceras endast omkring två ATP för varje oxiderad FADH2. Elektronerna från FADH2 producerar mindre ATP, eftersom de börjar vid en lägre punkt i ETC (komplex II) jämfört med elektronerna från NADH (komplex I) (Figur 5).
därför produceras för varje glukosmolekyl som går in i aerob andning en netto totalt 36 ATP (se Figur 6).
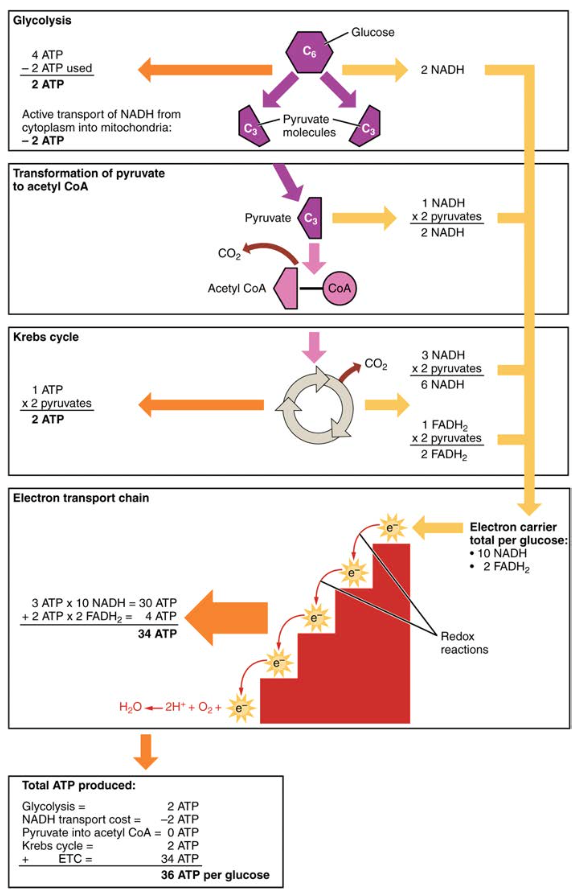
Figur 6. Kolhydratmetabolism innefattar glykolys, Krebs-cykeln och elektrontransportkedjan.
glukoneogenes
glukoneogenes är syntesen av nya glukosmolekyler från pyruvat, laktat, glycerol eller aminosyrorna alanin eller glutamin. Denna process sker främst i levern under perioder med låg glukos, det vill säga under förhållanden med fasta, svält och låga kolhydratdieter. Så frågan kan tas upp till varför kroppen skulle skapa något som den bara har spenderat en hel del ansträngningar för att bryta ner? Vissa nyckelorgan, inklusive hjärnan, kan bara använda glukos som energikälla; därför är det viktigt att kroppen upprätthåller en minimal blodglukoskoncentration. När blodglukoskoncentrationen faller under den specifika punkten syntetiseras ny glukos i levern för att höja blodkoncentrationen till det normala.
glukoneogenes är inte bara motsatsen till glykolys. Det finns några viktiga skillnader (Figur 7). Pyruvat är ett vanligt utgångsmaterial för glukoneogenes. Först omvandlas pyruvatet till oxaloacetat. Oxaloacetat tjänar sedan som ett substrat för enzymet fosfoenolpyruvatkarboxykinas (PEPCK), som omvandlar oxaloacetat till fosfoenolpyruvat (PEP). Från detta steg är glukoneogenes nästan motsatsen till glykolys. PEP omvandlas tillbaka till 2-fosfoglycerat, som omvandlas till 3-fosfoglycerat. Därefter omvandlas 3-fosfoglycerat till 1,3 bisfosfoglycerat och sedan till glyceraldehyd-3-fosfat. Två molekyler glyceraldehyd-3-fosfat kombineras sedan för att bilda fruktos-1-6-bisfosfat, som omvandlas till fruktos 6-fosfat och sedan till glukos-6-fosfat. Slutligen genererar en serie reaktioner glukos i sig. Vid glukoneogenes (jämfört med glykolys) ersätts enzymet hexokinas med glukos-6-fosfatas och enzymet fosfofruktokinas-1 ersätts med fruktos-1,6-bisfosfatas. Detta hjälper cellen att reglera glykolys och glukoneogenes oberoende av varandra.
som kommer att diskuteras som en del av lipolys kan fetter brytas ner i glycerol, som kan fosforyleras för att bilda dihydroxiacetonfosfat eller DHAP. DHAP kan antingen komma in i den glykolytiska vägen eller användas av levern som ett substrat för glukoneogenes.
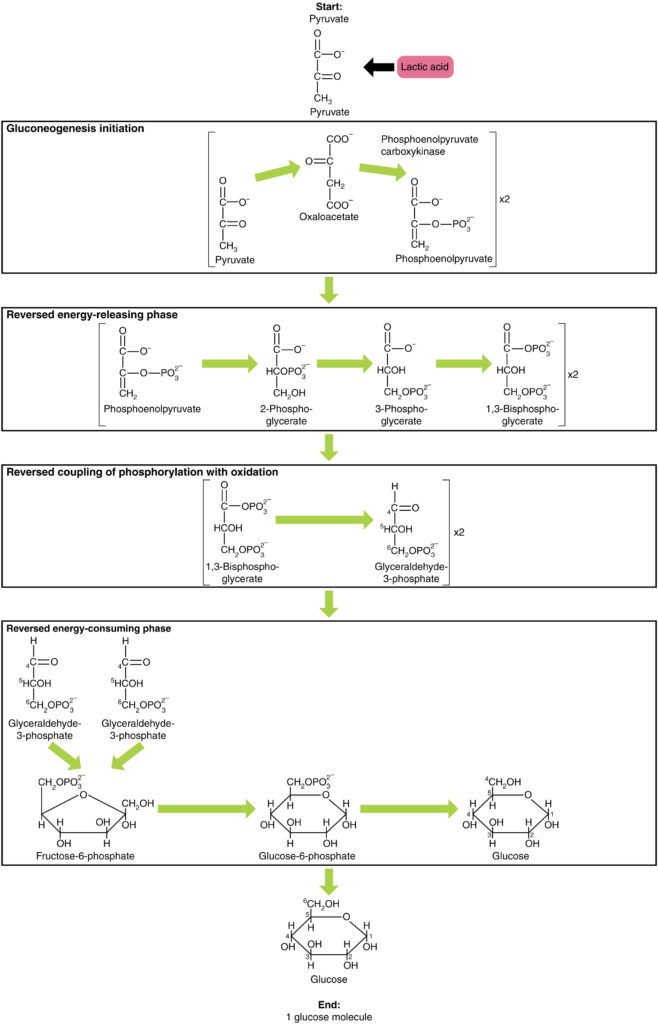
Figur 7. Klicka för att se en större bild. Glukoneogenes är syntesen av glukos från pyruvat, laktat, glycerol, alanin eller glutamat.
åldrande och kroppens ämnesomsättning
den mänskliga kroppens ämnesomsättning minskar nästan 2 procent per decennium efter 30 års ålder. Förändringar i kroppssammansättning, inklusive minskad mager muskelmassa, är mest ansvariga för denna minskning. Den mest dramatiska förlusten av muskelmassa och därmed minskad metabolisk hastighet uppträder mellan 50 och 70 år. Förlust av muskelmassa motsvarar minskad styrka, vilket tenderar att hämma seniorer från att delta i tillräcklig fysisk aktivitet. Detta resulterar i ett positivt återkopplingssystem där den minskade fysiska aktiviteten leder till ännu mer muskelförlust, vilket ytterligare minskar ämnesomsättningen.
det finns flera saker som kan göras för att förhindra allmänna nedgångar i ämnesomsättningen och att slå tillbaka mot den cykliska karaktären av dessa nedgångar. Dessa inkluderar att äta frukost, äta små måltider ofta, konsumera mycket magert protein, dricksvatten för att förbli hydratiserat, träna (inklusive styrketräning) och få tillräckligt med sömn. Dessa åtgärder kan hjälpa till att hålla energinivåerna från att släppa och begränsa uppmaningen till ökad kaloriförbrukning från överdriven snacking. Även om dessa strategier inte garanteras att upprätthålla ämnesomsättningen, hjälper de till att förhindra muskelförlust och kan öka energinivåerna. Vissa experter föreslår också att man undviker socker, vilket kan leda till överflödigt fettlagring. Kryddig mat och grönt te kan också vara fördelaktigt. Eftersom stress aktiverar kortisolfrisättning och kortisol saktar ämnesomsättningen, kan man undvika stress eller åtminstone öva avslappningstekniker.
kapitelöversikt
metaboliska enzymer katalyserar kataboliska reaktioner som bryter ner kolhydrater i maten. Den energi som frigörs används för att driva de celler och system som utgör din kropp. Överskott eller outnyttjad energi lagras som fett eller glykogen för senare användning. Kolhydratmetabolism börjar i munnen, där enzymet salivamylas börjar bryta ner komplexa sockerarter i monosackarider. Dessa kan sedan transporteras över tarmmembranet in i blodomloppet och sedan till kroppsvävnader. I cellerna bearbetas glukos, ett sexkolsocker, genom en sekvens av reaktioner till mindre sockerarter, och den energi som lagras inuti molekylen frigörs. Det första steget med kolhydratkatabolism är glykolys, som producerar pyruvat, NADH och ATP. Under anaeroba förhållanden kan pyruvatet omvandlas till laktat för att hålla glykolys fungerande. Under aeroba förhållanden går pyruvat in i Krebs-cykeln, även kallad citronsyracykeln eller trikarboxylsyracykeln. Förutom ATP producerar Krebs-cykeln högenergi – FADH2-och NADH-molekyler, som ger elektroner till den oxidativa fosforyleringsprocessen som genererar mer högenergi-ATP-molekyler. För varje glukosmolekyl som bearbetas i glykolys kan ett nät av 36 ATP skapas genom aerob andning.
under anaeroba förhållanden är ATP-produktionen begränsad till de som genereras av glykolys. Medan totalt fyra ATP produceras genom glykolys behövs två för att börja glykolys, så det finns ett nettoutbyte av två ATP-molekyler.
under förhållanden med låg glukos, såsom fastande, svält eller låga kolhydratdieter, kan glukos syntetiseras från laktat, pyruvat, glycerol, alanin eller glutamat. Denna process, kallad glukoneogenes, är nästan motsatsen till glykolys och tjänar till att skapa glukosmolekyler för glukosberoende organ, såsom hjärnan, när glukosnivåerna faller under normala.
självkontroll
svara på frågorna nedan för att se hur väl du förstår de ämnen som behandlas i föregående avsnitt.
kritiska tänkande frågor
- förklara hur glukos metaboliseras för att ge ATP.
- diskutera mekanismen celler använder för att skapa en koncentrationsgradient för att säkerställa kontinuerligt upptag av glukos från blodomloppet.
ordlista
polysackarider: komplexa kolhydrater som består av många monosackarider
monosackarid: minsta, monomer sockermolekyl
salivamylas: matsmältningsenzym som finns i saliven och börjar matsmältningen av kolhydrater i munnen
cellulär andning: produktion av ATP från glukosoxidation via glykolys, Krebs-cykeln och oxidativ fosforylering
glykolys: serie metaboliska reaktioner som bryter ner glukos till pyruvat och producerar ATP
pyruvat: slutprodukt med tre kol av glykolys och utgångsmaterial som omvandlas till acetyl CoA som går in i Krebs-cykeln
: även kallad citronsyracykeln eller trikarboxylsyracykeln, omvandlar pyruvat till CO2 och högenergi FADH2, NADH och ATP-molekyler
citronsyracykel eller trikarboxylsyracykel (TCA): även kallad Krebs-cykeln eller trikarboxylsyracykeln; omvandlar pyruvat till CO2 och högenergi FADH2, NADH och ATP-molekyler
energikrävande fas, första fas av glykolys, i vilken två molekyler av ATP är belägna i den första fasen nödvändigt att starta reaktionen
glukos-6-fosfat: fosforylerad glukos som produceras i det första steget av glykolys
hexokinas: cellulärt enzym, som finns i de flesta vävnader, som omvandlar glukos till glukos-6-fosfat vid upptag i cellen
glukokinas: cellularenzyme, som finns i levern, som omvandlar glukos till glukos-6-fosfat vid upptag i cellen
energiavkastande fas: andra fasen av glykolys, under vilken energi produceras
terminalelektronacceptor: ATP-produktionsväg där elektroner passerar genom en serie oxidationsreduceringsreaktioner som bildar vatten och producerar en protongradient
Krebs cykel: även kallad citronsyracykeln eller trikarboxylsyracykeln, omvandlar pyruvat till CO2 och högenergi FADH2, NADH och ATP-molekyler
elektrontransportkedja (ETC): ATP-produktionsväg där elektroner passerar genom en serie oxidationsreduceringsreaktioner som bildar vatten och producerar en protongradient
oxidativ fosforylering: process som omvandlar högenergi NADH och FADH2 till ATP
ATP-syntas protein: porkomplex som skapar ATP
glukoneogenes: process av glukossyntes från pyruvat eller andra molekyler