din rådgivare säger att han vill att du ska använda HPLC för att analysera din förening. Du vet att du har hört talas om den här tekniken tidigare, men du kommer inte ihåg vad HPLC står för, än mindre hur man gör det! Vi har alla varit där, och jag slår vad om att du önskar att du hade ägnat mer uppmärksamhet i den föreläsningen!
Frukta inte-i den här serien av artiklar kommer jag att påminna dig om kraften i HPLC-kolumnen bisexuell
i den här första artikeln tar jag dig igenom principen bakom HPLC och påminner dig om dess användning – du kommer att vara redo för labbet på nolltid!
hur fungerar HPLC?
högpresterande vätskekromatografi, eller HPLC, är ett långt namn för en kraftfull teknik baserad på det enkla faktum att enskilda föreningar beter sig annorlunda i vatten.
HPLC separerar och renar föreningar enligt deras polaritet, eller deras tendens att gilla eller ogillar vatten. För att sätta polaritet i sammanhang, anser att olja är en apolär vätska som inte blandas med vatten. Etanol, å andra sidan, är polär och som många av er vet, blandar mycket bra med vatten (Vodka och koks någon??).
Jag har försökt att förenkla hela processen i Figur 1 nedan, men först låt oss titta på de viktigaste komponenterna som är involverade i HPLC. Ursäkta i förväg för något oundvikligt jargong!
komponenterna
HPLC-kolumnen
detta kallas också den stationära fasen. Detta är arbetshästen för HPLC-maskinen, är tillverkad av en av olika ämnen (ofta kiseldioxid) och är mycket kompakt i naturen. Kiseldioxidpartiklarna funktionaliseras av långa kolkedjor. Kolkedjorna är apolära och ju längre kedjan desto mer apolär blir kolonnen. Kolumner som innehåller 18-kolkedjor används ofta och är kända som C18-kolumner.
HPLC-provet
Provtyper varierar mycket beroende på fältet och typen av föreningar i fråga. HPLC kan användas för att analysera föreningar i biologiska prover (urin, blod, saliv och muskler), miljöprover, läkemedelskemi (Läkemedel) och mikrobiologi (toxiner producerade av svampar och bakterier).
injektion av prov
prover injiceras i HPLC-kolumnen. Detta brukade utföras manuellt, vilket innebär att vissa fattiga själ var tvungen att sitta vid HPLC maskinen i timmar i sträck injicera varje prov med en spruta, ibland hela natten lång!
lyckligtvis har nyare modeller en automatisk injektor, vilket minskar manuell ingång och tillåter högre genomströmning. Moderna maskiner är utrustade med programvara som gör det möjligt för användaren att mata in en lista med prover, hur mycket och i vilken ordning de ska injiceras. Så du kan njuta av din lunch medan din HPLC kör själv!
den mobila fasen
detta är egentligen bara en blandning av vatten och ett organiskt lösningsmedel (vanligtvis acetonitril eller metanol). Den mobila fasen får det namn eftersom det rör sig genom kolonnen och samtidigt eluerar (eller spolar ut) föreningarna från kolonnen.
föreningar elueras ofta längs en koncentrationsgradient. Om du är något som jag, koncentration och lutning är två ord som du hatar att se komma ihop i en mening! Det betyder bara att andelen vatten i mobilfasen minskar med tiden, medan andelen apolärt lösningsmedel ökar samtidigt. Detta innebär att mobilfasen gradvis blir mer apolär. Oroa dig inte för mycket om gradienter för nu, eftersom de kommer att visas igen i en uppföljningsartikel.
HPLC-körningen
HPLC kan utföras i ett antal lägen. Den vanligaste metoden är känd som omvänd fas (RP-HPLC) och det här är vad jag beskriver här. I detta läge separeras föreningar som börjar med de mest polära och slutar med apolära föreningar. För alla lägen flyttar en högdriven pump provet och mobilfasen genom kolonnen. En typisk körning kan ta mellan 10-60 minuter.
principen bakom HPLC – en närmare titt
Nu när du har en uppfattning om de inblandade komponenterna, låt oss gå vidare till principen i lite mer detalj.
jag nämnde ovan att HPLC separerar föreningar på grundval av polaritet. Men hur fungerar det egentligen? Engelska snälla! När lutningen sparkar in ökar lösningsmedelskoncentrationen medan vattenkoncentrationen minskar. Detta gör mobilfasen mer och mer apolär. Föreningar som ingår i provet kommer att hålla fast vid kolkedjorna i kolonnen, med de mest apolära föreningarna som klibbar de starkaste och de mest polära föreningarna klibbar svagt.
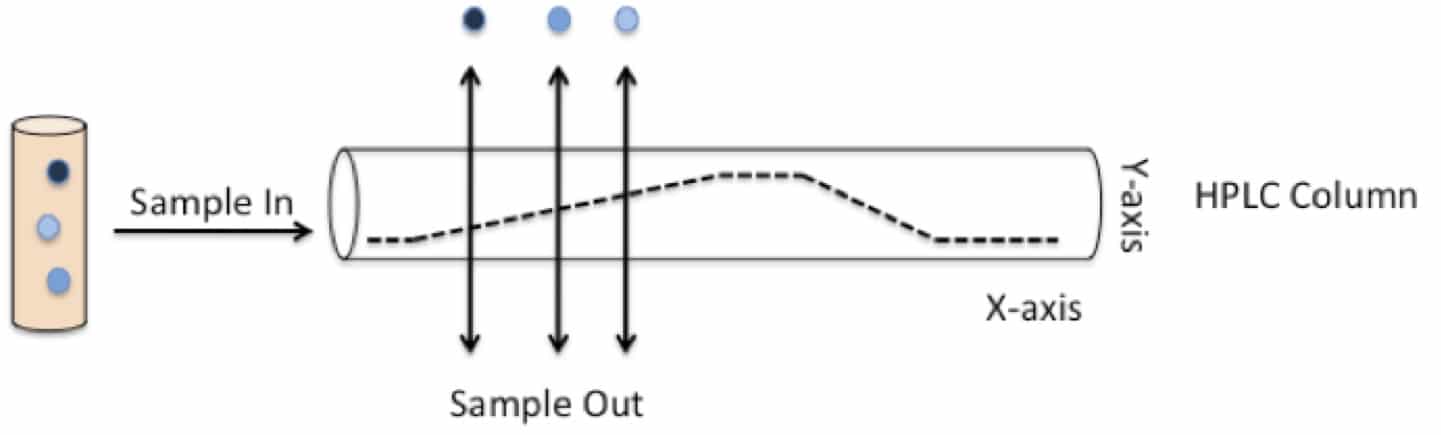
Figur 1 visar vad som händer med ett prov som innehåller en blandning av föreningar efter injektion i kolonnen. Föreningarna binder till kolonnen och spolas ut vid olika tidpunkter, beroende på om de är mer benägna att hålla sig till kolonnen eller mobilfasen när den pumpas igenom. Den tid som varje förening eluerar (eller spolar ut) från kolonnen är känd som den föreningens retentionstid (Rf).
Figur 1: principen bakom HPLC
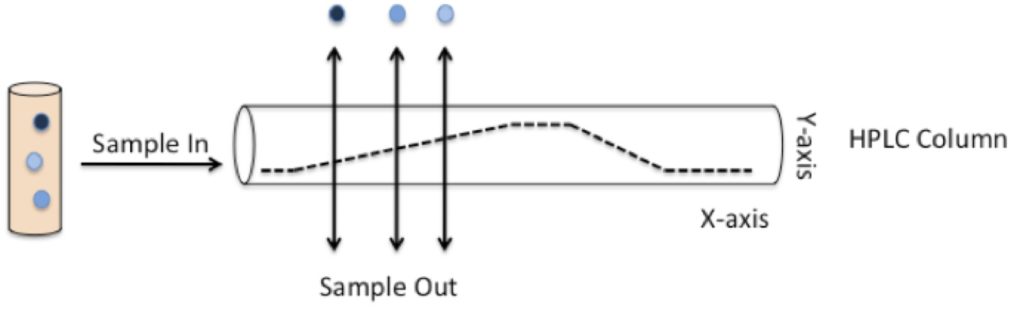
Figur 1: föreningar med olika polariteter (indikerade som mörkare nyanser av blått) injiceras i HPLC-kolonnen (hela cylindern). Den mobila fasen pumpas genom kolonnen, och tillsatsen av lösningsmedel längs en koncentrationsgradient (visas som en svart prickad linje) minskar kontinuerligt den totala polariteten hos den mobila fasen (Y-axeln). Föreningar kan hålla sig till antingen kolonnen eller mobilfasen, beroende på hur polära de är. Föreningar kommer så småningom att hålla sig till mobilfasen när deras polaritet matchar den för mobilfasen. De kommer sedan att dissociera från kolumnen och kommer att elueras vid en viss tidpunkt (X-axel) under körningen. Denna tid är känd som Rf för den föreningen.
förstå utgången
utgången eller resultaten av en HPLC-körning ses vanligtvis som ett kromatogram (Figur 2). Detta är en horisontell serie toppar som representerar föreningar eluerade från kolonnen med olika Rf-värden. Modern HPLC-utrustning kopplas ofta till en diodmatrisdetektor (DAD), så att användaren kan titta på det resulterande kromatogrammet av separerade föreningar i våglängder från 190 nm till 900 nm. Om de undersökta föreningarna är kända kan användaren välja att bara titta på 1 eller några valda våglängder. Till exempel kan kokain observeras vid 254 nm.
Figur 2: Ett typiskt HPLC-kromatogram

Figur 2: Detta kromatogram visar separationen av föreningar från en kemisk reaktion och kromatogrammet ses vid 254 nm. Två huvudtoppar uppträder vid 8,20 och 9 minuter, vilket representerar två föreningar med dessa retentionstider. Antalet absorbansenheter (AU) visas på Y-axeln medan tiden för körningen visas på X-axeln.
tillämpningar
inom biologi och medicin används HPLC ofta som ett analytiskt verktyg för att analysera biologiska och miljöprover för närvaro eller frånvaro av kända föreningar (till exempel metaboliter, läkemedel, toxiner, bekämpningsmedel) och kan hjälpa till vid identifiering av okända föreningar.
inom kemi används emellertid HPLC rutinmässigt för att övervaka kemiska reaktioner, liksom för att bestämma produktens renhet. Dessutom kan processen med HPLC modifieras till preparativ HPLC, varigenom föreningar av intresse kan renas för vidare användning.
HPLC kan komma över som mycket komplicerat till att börja med, men vara säker, precis som de flesta andra lab tekniker, det gör mycket mer meningsfullt när du faktiskt gör det.
Håll dig uppdaterad för mina uppföljningsartiklar under de kommande veckorna, där jag kommer att gå igenom några tips om hur du kan få det bästa av din HPLC-körning beroende på ditt forskningsmål, samt diskutera objektivt hur HPLC kan användas inom din forskning.
finns det några andra aspekter av denna teknik som du vill ha mer detaljerat? Om så är fallet, vi skulle gärna höra från dig!
Happy HPLC-ing Portugals
har detta hjälpt dig? Vänligen dela med ditt nätverk.