Generischer Name: Heparin-Natrium
Darreichungsform: Injektion
- Hep-Lock Beschreibung
- Hep-Lock – Klinische Pharmakologie
- Indikationen und Verwendung für Hep-Lock
- Kontraindikationen
- Warnhinweise
- Überempfindlichkeit
- Blutung
- Thrombozytopenie
- Heparin-induzierte Thrombozytopenie (HIT) und Heparin-induzierte Thrombozytopenie und Thrombose (HITT)
- Verzögertes Einsetzen von HIT und HITT
- Anwendung bei Neugeborenen und Säuglingen
- Vorsichtsmaßnahmen
- Allgemeines
- Labortests
- Arzneimittelwechselwirkungen
- Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
- Schwangerschaft
- Schwangerschaftskategorie C
- Stillende Mütter
- Pädiatrische Anwendung
- Geriatrische Anwendung
- Nebenwirkungen
- Blutungen
- Thrombozytopenie, Heparin-induzierte Thrombozytopenie (HIT) und Heparin-induzierte Thrombozytopenie und Thrombose (HITT) und verzögertes Einsetzen von HIT und HITT
- Lokale Reizung
- Überempfindlichkeit
- Überdosierung
- Symptome
- Behandlung – Neutralisierung der Heparinwirkung
- Hep-Lock Dosierung und Verabreichung
- Aufrechterhaltung der Durchgängigkeit von intravenösen Geräten
- Entnahme von Blutproben
- Wie wird Hep-Lock geliefert?
- Lagerung
Hep-Lock Beschreibung
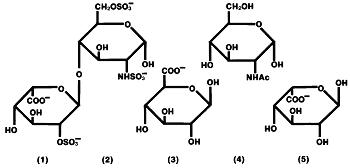
Heparin ist eine heterogene Gruppe von geradkettigen anionischen Mucopolysacchariden, Glykosaminoglykanen genannt, mit gerinnungshemmenden Eigenschaften. Obwohl andere vorhanden sein können, sind die in Heparin vorkommenden Hauptzucker: (1) α-L-iduronsäure-2-sulfat, (2) 2-Desoxy-2-sulfamino-α-D-glucose-6-sulfat, (3) β-D-Glucuronsäure, (4) 2-Acetamido-2-Desoxy-α-D-glucose und (5) α-L-iduronsäure. Diese Zucker sind in abnehmenden Mengen vorhanden, normalerweise in der Reihenfolge (2)>>>>(5), und sind durch glykosidische Verknüpfungen verbunden, wobei Polymere unterschiedlicher Größe gebildet werden. Heparin ist aufgrund seines Gehalts an kovalent verknüpften Sulfat- und Carbonsäuregruppen stark sauer. In Heparin-Natrium werden die sauren Protonen der Sulfateinheiten teilweise durch Natriumionen ersetzt.
Strukturformel von Heparin-Natrium (repräsentative Untereinheiten):
Hep-Lock U/ P (konservierungsmittelfreie Heparin-Lock-Spüllösung, USP) ist eine sterile Lösung nur zur intravenösen Spülung. Es darf nicht zur gerinnungshemmenden Therapie verwendet werden. Hep-Lock U / P wurde speziell für den Einsatz in Situationen entwickelt, in denen die Verwendung von Konservierungsmitteln nicht ratsam ist. Jeder ml enthält Heparin-Natrium 10 oder 100 USP-Einheiten, abgeleitet von Schweinedärmen und standardisiert für die Verwendung als Antikoagulans, Natriumchlorid 8 mg, einbasisches Natriumphosphat-Monohydrat 2,3 mg und zweibasisches Natriumphosphat wasserfrei 0,5 mg in Wasser zur Injektion. pH 5,0-7.5. Die Wirksamkeit wird durch biologischen Assay unter Verwendung eines USP-Referenzstandards basierend auf Einheiten der Heparinaktivität pro Milligramm bestimmt.
Hep-Lock – Klinische Pharmakologie
Heparin hemmt Reaktionen, die sowohl in vitro als auch in vivo zur Blutgerinnung und zur Bildung von Fibringerinnseln führen. Heparin wirkt an mehreren Stellen im normalen Gerinnungssystem. Kleine Mengen Heparin in Kombination mit Antithrombin III (Heparin-Cofaktor) können die Thrombose hemmen, indem sie den aktivierten Faktor X inaktivieren und die Umwandlung von Prothrombin in Thrombin hemmen. Sobald sich eine aktive Thrombose entwickelt hat, können größere Mengen Heparin die weitere Gerinnung hemmen, indem sie Thrombin inaktivieren und die Umwandlung von Fibrinogen in Fibrin verhindern. Heparin verhindert auch die Bildung eines stabilen Fibringerinnsels, indem es die Aktivierung des Fibrinstabilisierungsfaktors hemmt.
Die Blutungszeit wird normalerweise nicht durch Heparin beeinflusst. Die Gerinnungszeit wird durch volle therapeutische Heparindosen verlängert; In den meisten Fällen wird es durch niedrige Heparindosen nicht messbar beeinflusst. Loglineare Diagramme der Heparin-Plasmakonzentrationen mit der Zeit sind für einen weiten Bereich von Dosisstufen linear, was auf das Fehlen von Prozessen nullter Ordnung hindeutet. Leber und das retikulo-endotheliale System sind die Orte der Biotransformation. Die biphasische Eliminationskurve, eine schnell abnehmende Alpha-Phase (t½ = 10 min) und nach dem 40. Lebensjahr eine langsamere Beta-Phase, zeigt die Aufnahme in die Organe an. Das Fehlen einer Beziehung zwischen der gerinnungshemmenden Halbwertszeit und der Konzentrationshalbwertszeit kann Faktoren wie die Proteinbindung von Heparin widerspiegeln.
Patienten über 60 Jahre können nach ähnlichen Heparin-Dosen höhere Heparin-Plasmaspiegel und längere aktivierte partielle Thromboplastinzeiten (APTTs) aufweisen als Patienten unter 60 Jahren.
Heparin hat keine fibrinolytische Aktivität; Daher wird es vorhandene Gerinnsel nicht lysieren.
Indikationen und Verwendung für Hep-Lock
Hep-Lock U / P (konservierungsmittelfreie Heparin-Lock-Spüllösung, USP) soll die Durchgängigkeit eines verweilenden Venenpunktionsgeräts aufrechterhalten, das für die intermittierende Injektions- oder Infusionstherapie oder Blutentnahme ausgelegt ist. Heparin Lock Flush Solution kann nach der ersten Platzierung des Geräts in der Vene, nach jeder Injektion eines Medikaments oder nach Entnahme von Blut für Labortests verwendet werden. (Siehe DOSIERUNG UND VERABREICHUNG, Aufrechterhaltung der Durchgängigkeit von intravenösen Geräten für Gebrauchsanweisungen.)
Hep-Lock U/P darf nicht zur gerinnungshemmenden Therapie angewendet werden.
Kontraindikationen
Heparin-Natrium sollte NICHT bei Patienten mit folgenden Erkrankungen angewendet werden: schwere Thrombozytopenie; ein unkontrollierbarer aktiver Blutungszustand (siehe WARNHINWEISE), außer wenn dies auf eine disseminierte intravaskuläre Koagulation zurückzuführen ist.
Warnhinweise
Heparin ist nicht zur intramuskulären Anwendung bestimmt.
Überempfindlichkeit
Patienten mit dokumentierter Überempfindlichkeit gegen Heparin sollten das Arzneimittel nur in eindeutig lebensbedrohlichen Situationen erhalten. (Siehe NEBENWIRKUNGEN, Überempfindlichkeit.)
Blutung
Blutungen können bei Patienten, die Heparin erhalten, an praktisch jeder Stelle auftreten. Ein ungeklärter Abfall des Hämatokrits, ein Blutdruckabfall oder ein anderes ungeklärtes Symptom sollte zu einer ernsthaften Prüfung eines hämorrhagischen Ereignisses führen.
Heparin-Natrium sollte in Krankheitszuständen, in denen eine erhöhte Blutungsgefahr besteht, mit äußerster Vorsicht angewendet werden. Einige der Zustände, bei denen eine erhöhte Blutungsgefahr besteht, sind:
Kardiovaskulär
Subakute bakterielle Endokarditis, schwere Hypertonie.Chirurgisch Während und unmittelbar nach (a) Spinal Tap oder Spinalanästhesie oder (b) größeren Operationen, insbesondere am Gehirn, Rückenmark oder Auge.Hämatologische Zustände, die mit erhöhten Blutungstendenzen verbunden sind, wie Hämophilie, Thrombozytopenie und einige vaskuläre Purpuras.
Gastrointestinal
Ulzerative Läsionen und kontinuierliche Schlauchdrainage des Magens oder Dünndarms.
Andere
Menstruation, Lebererkrankung mit gestörter Hämostase.
Thrombozytopenie
Es wurde berichtet, dass Thrombozytopenie bei Patienten, die Heparin erhielten, mit einer berichteten Inzidenz von bis zu 30% auftrat. Die Thrombozytenzahl sollte zu Studienbeginn und in regelmäßigen Abständen während der Heparin-Verabreichung ermittelt werden. Eine leichte Thrombozytopenie (Anzahl größer als 100.000 / mm3) kann stabil bleiben oder sich umkehren, selbst wenn Heparin fortgesetzt wird. Thrombozytopenie jeden Grades sollte jedoch engmaschig überwacht werden. Wenn die Zahl unter 100.000 / mm3 fällt oder sich eine wiederkehrende Thrombose entwickelt (siehe Heparin-induzierte Thrombozytopenie und Heparin-induzierte Thrombozytopenie und Thrombose), sollte das Heparin-Produkt abgesetzt und erforderlichenfalls ein alternatives Antikoagulans verabreicht werden.
Heparin-induzierte Thrombozytopenie (HIT) und Heparin-induzierte Thrombozytopenie und Thrombose (HITT)
Heparin-induzierte Thrombozytopenie (HIT) ist eine schwerwiegende antikörpervermittelte Reaktion, die aus einer irreversiblen Aggregation von Thrombozyten resultiert. HIT kann zur Entwicklung von venösen und arteriellen Thrombosen führen, einem Zustand, der als Heparin-induzierte Thrombozytopenie und Thrombose (HITT) bezeichnet wird. Thrombotische Ereignisse können auch die erste Präsentation für HITT sein. Diese schwerwiegenden thromboembolischen Ereignisse umfassen tiefe Venenthrombose, Lungenembolie, zerebrale Venenthrombose, Extremitätenischämie, Schlaganfall, Myokardinfarkt, Mesenterialthrombose, Nierenarterienthrombose, Hautnekrose, Gangrän der Extremitäten, die zur Amputation und möglicherweise zum Tod führen können. Thrombozytopenie jeden Grades sollte engmaschig überwacht werden. Wenn die Thrombozytenzahl unter 100.000 / mm3 fällt oder sich eine rezidivierende Thrombose entwickelt, sollte das Heparinpräparat unverzüglich abgesetzt und alternative Antikoagulanzien in Betracht gezogen werden, wenn Patienten eine weitere Antikoagulation benötigen.
Verzögertes Einsetzen von HIT und HITT
Heparin-induzierte Thrombozytopenie und Heparin-induzierte Thrombozytopenie und Thrombose können bis zu mehreren Wochen nach Absetzen der Heparin-Therapie auftreten. Patienten mit Thrombozytopenie oder Thrombose nach Absetzen von Heparin sollten auf HIT und HITT untersucht werden.
Anwendung bei Neugeborenen und Säuglingen
Die Konzentration von 100 Einheiten/ml sollte wegen des Risikos einer systemischen Antikoagulation nicht bei Neugeborenen oder bei Säuglingen mit einem Gewicht von weniger als 10 kg angewendet werden. Vorsicht ist geboten, wenn die Konzentration von 10 Einheiten / ml bei Frühgeborenen angewendet wird, die weniger als 1 kg wiegen und häufige Spülungen erhalten, da dem Säugling innerhalb von 24 Stunden eine therapeutische Heparin-Dosis verabreicht werden kann.
Vorsichtsmaßnahmen
Allgemeines
Vorsichtsmaßnahmen müssen getroffen werden, wenn Arzneimittel, die mit Heparin nicht kompatibel sind, über einen intravenösen Verweilkatheter verabreicht werden, der eine konservierungsmittelfreie Heparin-Lock-Spüllösung enthält. (Überdosierung UND VERABREICHUNG, Aufrechterhaltung der Durchgängigkeit von intravenösen Geräten.) Die Konzentration von Phosphor in der Heparinlösung beträgt 0,63 mg/ml.
Thrombozytopenie, Heparin-induzierte Thrombozytopenie (HIT) und Heparin-induzierte Thrombozytopenie und Thrombose (HITT)
SeeWARNINGS
Erhöhtes Risiko für ältere Patienten, insbesondere Frauen
Eine höhere Inzidenz von Blutungen wurde bei Patienten, insbesondere Frauen, über 60 Jahre berichtet.
Labortests
Während des gesamten Verlaufs der Heparintherapie werden unabhängig vom Verabreichungsweg periodische Thrombozytenzahlen, Hämatokritwerte und Tests auf okkultes Blut im Stuhl empfohlen. (DosIERUNG UND VERABREICHUNG.)
Arzneimittelwechselwirkungen
Thrombozytenhemmer
Arzneimittel wie Acetylsalicylsäure, Dextran, Phenylbutazon, Ibuprofen, Indomethacin, Dipyridamol, Hydroxychloroquin und andere, die Thrombozytenaggregationsreaktionen (die wichtigste hämostatische Abwehr von heparinisierten Patienten) stören, können Blutungen auslösen und sollten bei Patienten, die Heparin-Natrium erhalten, mit Vorsicht angewendet werden.
Andere Wechselwirkungen
Digitalis, Tetracycline, Nikotin oder Antihistaminika können der gerinnungshemmenden Wirkung von Heparin-Natrium teilweise entgegenwirken.
Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
Es wurden keine Langzeitstudien an Tieren durchgeführt, um das karzinogene Potenzial von Heparin-Natrium zu bewerten. Es wurden auch keine Reproduktionsstudien an Tieren zur Mutagenese oder Beeinträchtigung der Fertilität durchgeführt.
Schwangerschaft
Teratogene Wirkungen
Schwangerschaftskategorie C
Tierexperimentelle Reproduktionsstudien mit Heparin-Natrium wurden nicht durchgeführt. Es ist auch nicht bekannt, ob Heparin-Natrium bei Verabreichung an eine schwangere Frau fetale Schäden verursachen oder die Fortpflanzungsfähigkeit beeinträchtigen kann. Heparin-Natrium sollte einer schwangeren Frau nur verabreicht werden, wenn dies eindeutig erforderlich ist.
Nichtteratogene Wirkungen
Heparin überschreitet nicht die Plazentaschranke.
Stillende Mütter
Heparin wird nicht in die Muttermilch ausgeschieden.
Pädiatrische Anwendung
Sicherheit und Wirksamkeit bei pädiatrischen Patienten wurden nicht nachgewiesen (siehe WARNHINWEISE, Anwendung bei Neugeborenen und Säuglingen).
Geriatrische Anwendung
Bei Patienten über 60 Jahren, insbesondere bei Frauen, wurde über eine höhere Inzidenz von Blutungen berichtet (siehe KLINISCHE PHARMAKOLOGIE und VORSICHTSMAßNAHMEN, Allgemein).
Nebenwirkungen
Blutungen
Blutungen sind die Hauptkomplikation, die sich aus der Anwendung von Heparin ergeben kann (siehe Warnhinweise, Blutungen). Eine übermäßig verlängerte Gerinnungszeit oder geringfügige Blutungen während der Therapie können normalerweise durch Absetzen des Arzneimittels kontrolliert werden (siehe ÜBERDOSIERUNG).
Thrombozytopenie, Heparin-induzierte Thrombozytopenie (HIT) und Heparin-induzierte Thrombozytopenie und Thrombose (HITT) und verzögertes Einsetzen von HIT und HITT
Seewarnungen.
Lokale Reizung
Bei der Anwendung von Heparin Lock Flush Solution wurden lokale Reizungen und Erytheme berichtet.
Überempfindlichkeit
Es wurde über generalisierte Überempfindlichkeitsreaktionen berichtet, wobei Schüttelfrost, Fieber und Urtikaria die häufigsten Manifestationen waren und Asthma, Rhinitis, Tränenfluss, Kopfschmerzen, Übelkeit und Erbrechen sowie anaphylaktoide Reaktionen, einschließlich Schock, seltener auftraten. Juckreiz und Brennen, insbesondere auf der Plantarseite der Füße, können auftreten.
Es wurde berichtet, dass Thrombozytopenie bei Patienten, die Heparin erhielten, mit einer berichteten Inzidenz von bis zu 30% auftrat. Obwohl eine solche Thrombozytopenie häufig mild und ohne offensichtliche klinische Bedeutung ist, kann sie von schweren thromboembolischen Komplikationen wie Hautnekrose, Gangrän der Extremitäten begleitet sein, die zu Amputation, Myokardinfarkt, Lungenembolie, Schlaganfall und möglicherweise zum Tod führen können. (Siehe WARNHINWEISE und VORSICHTSMAßNAHMEN.)
Bestimmte Episoden von schmerzhaften, ischämischen und zyanosierten Gliedmaßen wurden in der Vergangenheit auf allergische vasospastische Reaktionen zurückgeführt. Ob diese tatsächlich mit den Thrombozytopenie-assoziierten Komplikationen identisch sind, bleibt abzuwarten.
Überdosierung
Symptome
Blutungen sind das Hauptzeichen einer Heparin-Überdosierung. Nasenbluten, Blut im Urin oder teeriger Stuhl können als erstes Anzeichen von Blutungen festgestellt werden. Leichte Blutergüsse oder petechiale Formationen können offenen Blutungen vorausgehen.
Behandlung – Neutralisierung der Heparinwirkung
Wenn klinische Umstände (Blutungen) eine Umkehrung der Heparinisierung erfordern, neutralisiert Protaminsulfat (1% ige Lösung) durch langsame Infusion Heparin-Natrium. In einem Zeitraum von 10 Minuten sollten nicht mehr als 50 mg sehr langsam verabreicht werden. Jedes mg Protaminsulfat neutralisiert ungefähr 100 USP-Heparin-Einheiten. Die erforderliche Menge an Protamin nimmt mit der Zeit ab, wenn Heparin metabolisiert wird. Obwohl der Metabolismus von Heparin komplex ist, kann für die Wahl einer Protamindosis von einer Halbwertszeit von etwa 1/2 Stunde nach intravenöser Injektion ausgegangen werden.
Die Verabreichung von Protaminsulfat kann schwere blutdrucksenkende und anaphylaktoide Reaktionen verursachen. Da tödliche Reaktionen, die häufig einer Anaphylaxie ähneln, berichtet wurden, sollte das Arzneimittel nur verabreicht werden, wenn Wiederbelebungstechniken und die Behandlung eines anaphylaktoiden Schocks leicht verfügbar sind.
Für weitere Informationen konsultieren Sie die Kennzeichnung von Protaminsulfat-Injektion, USP-Produkte.
Hep-Lock Dosierung und Verabreichung
Parenterale Arzneimittel sollten vor der Verabreichung visuell auf Partikel und Verfärbungen untersucht werden, wann immer Lösung und Behälter dies zulassen. Leichte Verfärbungen verändern die Wirksamkeit nicht.
Konservierungsmittelfreie Heparin-Lock-Spüllösung in einer Konzentration von 100 Einheiten/ml wird nicht für die Anwendung bei Neugeborenen und Säuglingen empfohlen (siehe WARNHINWEISE, Anwendung bei Neugeborenen und Säuglingen).
Aufrechterhaltung der Durchgängigkeit von intravenösen Geräten
Um die Gerinnselbildung in einem Heparin-Lock-Set oder Zentralvenenkatheter nach ordnungsgemäßem Einführen zu verhindern, wird Heparin Lock Flush Solution, USP, über die Injektionsnabe in einer Menge injiziert, die ausreicht, um das gesamte Gerät zu füllen. Diese Lösung sollte bei jeder Verwendung des Geräts ausgetauscht werden. Aspirieren Sie, bevor Sie eine Lösung über das Gerät verabreichen, um die Durchgängigkeit und Position der Nadel oder Katheterspitze zu bestätigen. Wenn das zu verabreichende Medikament nicht mit Heparin kompatibel ist, sollte das gesamte Gerät vor und nach der Verabreichung des Medikaments mit normaler Kochsalzlösung gespült werden. Die Anweisungen des Geräteherstellers sollten zu Einzelheiten seiner Verwendung konsultiert werden. Normalerweise hält diese verdünnte Heparinlösung die Antikoagulation innerhalb des Geräts für bis zu 4 Stunden aufrecht.
HINWEIS: Da wiederholte Injektionen kleiner Heparindosen die Tests auf aktivierte partielle Thromboplastinzeit (APTT) verändern können, sollte vor dem Einsetzen eines intravenösen Geräts ein Ausgangswert für die APTT ermittelt werden.
Entnahme von Blutproben
Konservierungsmittelfreie Heparin-Lock-Spüllösung, USP, kann auch nach jeder Blutentnahme für Labortests verwendet werden. Wenn Heparin die Ergebnisse von Blutuntersuchungen beeinträchtigen oder verändern würde, sollte die Heparinlösung aus dem Gerät entfernt werden, indem sie abgesaugt und verworfen wird, bevor die Blutprobe entnommen wird.
Wie wird Hep-Lock geliefert?
Hep-Lock U/P (konservierungsmittelfreie Heparin-Lock-Spüllösung, USP)
10 USP-Einheiten/ml
1 ml Dosettenfläschchen verpackt in 25s (NDC 0641-0272-25)
100 USP-Einheiten/ml
1 ml Dosettenfläschchen verpackt in 25s (NDC 0641-0273-25)
Lagerung
Bei 20°-25°C (68°-77°F) lagern.
- Tahata T, Shigehito M, Kusuhara K, Ueda Y, et al. Verzögertes Einsetzen der Heparin-induzierten Thrombozytopenie – Ein Fallbericht – J Jpn Assn Torca Surg.1992; 40 (3): 110-111.
- Warkentin T., Kelton J. Verzögert einsetzende Heparin-induzierte Thrombozytopenie und Thrombose. Annalen der Inneren Medizin. 2001;135:502-506.
- Rice L, Attisha W, Drexler A, Francis J. Heparin-induzierte Thrombozytopenie mit verzögertem Beginn. Annalen der Inneren Medizin, 2002; 136: 210-215.
- Dieck J., C. Rizo-Patron, et al. (1990). „Eine neue Manifestations- und Behandlungsalternative für Heparin-induzierte Thrombosen.” Brust.1990;98:1524-26.
- Smythe M, Stephens J, Mattson. Verzögert einsetzende Heparin-induzierte Thrombozytopenie. Annalen der Notfallmedizin, 2005;45(4):417-419.
- Divgi A. (Nachdruck), Thumma S., Hari P., Friedman K., Verzögerte Heparin-induzierte Thrombozytopenie (HIT) nach undokumentierter Arzneimittelexposition als Lungenembolie nach Angiographie. Blut. 2003;102(11):127b.
Das ESI-Logo, Hep-Lock und Dosette sind eingetragene Marken von Baxter International, Inc. oder deren Tochtergesellschaften.
Hergestellt von
Baxter Healthcare Corporation
Deerfield, IL 60015 USA
Für Produktanfrage 1 800 ANA DRUG (1-800-262-3784)
MLT-00090/6.0
| Hep-Lock U/P heparin sodium injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
| Hep-Lock U/P heparin sodium injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Baxter Healthcare Corporation
Medical Disclaimer