neuvonantajasi kertoo, että hän haluaa sinun käyttävän HPLC: tä yhdisteesi analysointiin. Tiedät, että olet kuullut tästä tekniikasta aiemmin, mutta et muista, mitä HPLC tarkoittaa, saati miten tehdä se! Olemme kaikki olleet siellä, ja toivot varmasti, että olisit kiinnittänyt enemmän huomiota luennolla!
pelko pois – tässä artikkelisarjassa muistutan HPLC – palstan voimasta 🙂
tässä ensimmäisessä artikkelissa käyn läpi HPLC: n taustalla olevaa periaatetta ja muistutan sen käyttötarkoituksista-olet valmis laboratorioon hetkessä!
miten HPLC vaikuttaa?
korkean erotuskyvyn nestekromatografia eli HPLC on pitkä nimitys tehokkaalle tekniikalle, joka perustuu siihen, että yksittäiset yhdisteet käyttäytyvät vedessä eri tavoin.
HPLC erottaa ja puhdistaa yhdisteitä niiden polaarisuuden tai taipumuksen pitää tai olla pitämättä vedestä. Jos haluat laittaa napaisuuden asiayhteyteen, ota huomioon, että öljy on apolaarinen neste, joka ei sekoitu veteen. Etanoli taas on polaarinen ja kuten monet teistä tietävät, sekoittuu erittäin hyvin veteen(Vodka ja coke ketään??).
olen yrittänyt yksinkertaistaa koko prosessia alla olevassa kuvassa 1, mutta Tarkastellaanpa ensin HPLC: hen liittyviä pääkomponentteja. Pahoittelut etukäteen jostain väistämättömästä jargonista!
komponentit
HPLC-sarake
tätä kutsutaan myös stationäärifaasiksi. Tämä on HPLC-koneen työjuhta, joka on valmistettu yhdestä eri aineista (usein piidioksidista) ja on luonteeltaan hyvin kompakti. Piihiukkaset funktionalisoituvat pitkillä hiiliketjuilla. Hiiliketjut ovat apolaarisia, joten mitä pidempi ketju, sitä apolaarisempi kolonnista tulee. 18-hiilisiä ketjuja sisältäviä pylväitä käytetään yleisesti, ja niitä kutsutaan C18-sarakkeiksi.
HPLC-näytteen
Näytetyypit vaihtelevat suuresti kentän ja kyseessä olevien yhdisteiden tyypin mukaan. HPLC: tä voidaan käyttää biologisten näytteiden (virtsa, veri, sylki ja lihas), ympäristönäytteiden, lääkekemian (lääkkeet) ja mikrobiologian (sienten ja bakteerien tuottamat toksiinit) analysointiin.
näytteet injektoidaan HPLC-kolonniin. Tämä tehtiin ennen käsin, mikä tarkoitti sitä, että jonkun köyhän täytyi istua HPLC-koneen ääressä tuntikausia ruiskuttaen jokaista näytettä ruiskulla, joskus koko yön!
onneksi uudemmissa malleissa on automaattisuutin, joka vähentää manuaalista syöttöä ja mahdollistaa suuremman läpimenon. Nykyaikaiset koneet on varustettu ohjelmistolla, jonka avulla käyttäjä voi syöttää luettelon näytteistä, kuinka paljon ja missä järjestyksessä niitä tulee ruiskuttaa. Joten voit nauttia lounaan, kun HPLC toimii itse!
liikkuva faasi
Tämä on oikeastaan vain veden ja orgaanisen liuottimen (yleensä asetonitriilin tai metanolin) seos. Liikkuva faasi saa nimensä, koska se liikkuu kolonnin läpi ja samalla eluoi (tai huuhtoo) kolonnista yhdisteitä.
yhdisteet eluoidaan usein konsentraatiogradienttia pitkin. Jos olet yhtään kaltaiseni, keskittyminen ja kaltevuus ovat kaksi sanaa, joita Inhoat nähdä yhdessä lauseessa! Se tarkoittaa vain sitä, että veden osuus liikkuvassa faasissa pienenee ajan myötä, kun taas apolaarisen liuottimen osuus kasvaa samanaikaisesti. Tämä tarkoittaa, että liikkuva faasi muuttuu vähitellen apolaarisemmaksi. Älä murehdi liikaa liukuvärejä toistaiseksi, sillä ne näkyvät jälleen jatkoartikkelissa.
HPLC-ajo
HPLC voidaan suorittaa useissa moodeissa. Yleisimmin käytetty menetelmä tunnetaan käänteisfaasina (RP-HPLC) ja tämä on mitä kuvailen tässä. Tässä tilassa yhdisteet erotetaan toisistaan alkaen polaarisimmasta ja päättyen apolaarisiin yhdisteisiin. Kaikissa tiloissa suuritehoinen pumppu siirtää näytteen ja liikkuvan vaiheen kolonnin läpi. Tyypillinen juoksu voi kestää 10-60 minuuttia.
HPLC: n taustalla oleva periaate – lähempi katsaus
nyt kun sinulla on käsitys mukana olevista komponenteista, siirrytään periaatteeseen hieman yksityiskohtaisemmin.
i edellä mainittiin, että HPLC erottaa yhdisteet napaisuuden perusteella. Mutta miten tämä oikeastaan toimii? Englantia, kiitos! Gradientin käynnistyessä liuotinpitoisuus kasvaa samalla kun vesipitoisuus laskee. Tämä tekee liikkuvasta vaiheesta yhä apolaarisemman. Näytteen sisältämät yhdisteet tarttuvat kolonnin hiiliketjuihin, joista apolaarisimmat yhdisteet tarttuvat vahvimpiin ja polaarisimmat yhdisteet heikosti.
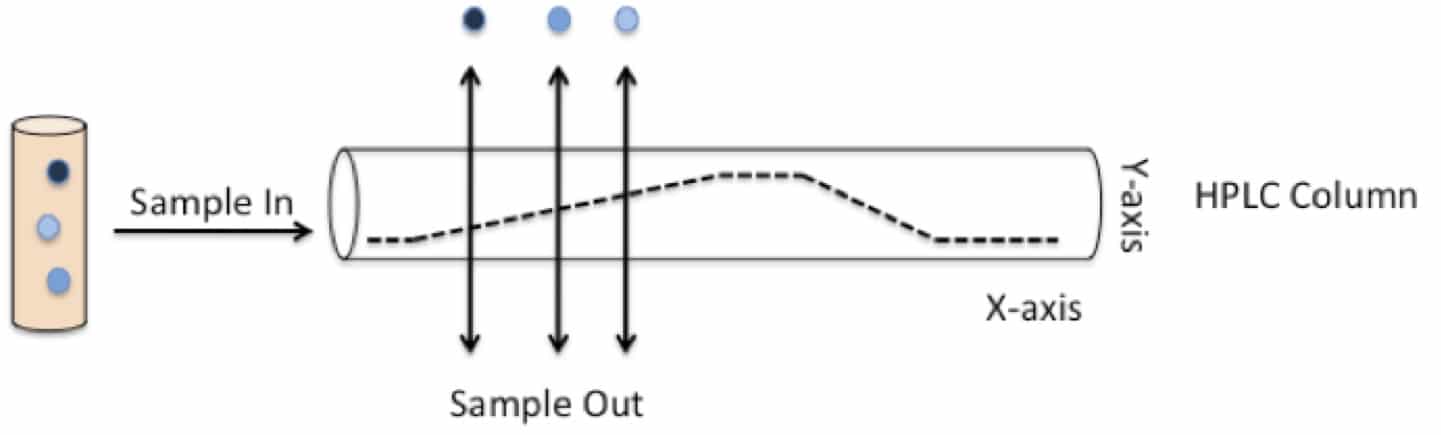
kuva 1 osoittaa, mitä tapahtuu yhdisteseosta sisältävälle näytteelle kolonniin injisoinnin jälkeen. Yhdisteet sitoutuvat kolonniin ja huuhtoutuvat ulos eri aikoina riippuen siitä, tarttuvatko ne todennäköisemmin kolonniin vai liikkuvaan faasiin, kun se pumpataan läpi. Aikaa, jonka kukin yhdiste eluoituu (tai huuhtoutuu) kolonnista, kutsutaan yhdisteen retentioajaksi (RF).
kuva 1: HPLC: n taustalla oleva periaate
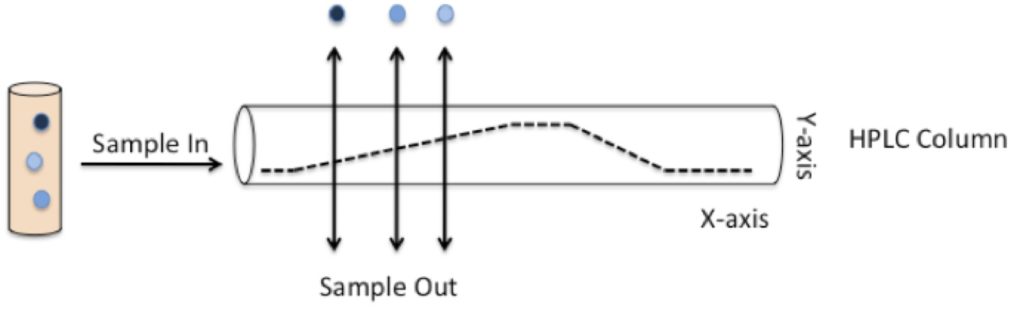
kuva 1: HPLC-kolonniin (koko sylinteri) ruiskutetaan erilaisia polariteettiyhdisteitä (merkitty sinisen tummuvina sävyinä). Liikkuva faasi pumpataan kolonnin läpi, ja liuottimen lisääminen konsentraatiogradienttia pitkin (mustana katkoviivana) vähentää jatkuvasti liikkuvan faasin (Y-akselin) yleistä napaisuutta. Yhdisteet pystyvät tarttumaan joko kolonniin tai liikkuvaan faasiin riippuen siitä, kuinka polaarisia ne ovat. Yhdisteet tarttuvat lopulta liikkuvaan faasiin, kun niiden napaisuus vastaa liikkuvan faasin napaisuutta. Tämän jälkeen ne irtoavat pylväästä ja eluoituvat tiettyyn aikaan (X-akseli) ajon aikana. Tämä aika tunnetaan kyseisen yhdisteen RF: nä.
Lähtö
HPLC-ajon tulosta tai tuloksia tarkastellaan yleensä kromatogrammina (kuva 2). Tämä on vaakasuora sarja huippuja, jotka edustavat kolonnista eluoituja yhdisteitä, joilla on erilaiset Rf-arvot. Nykyaikaiset HPLC-laitteet on usein kytketty diodirividetektoriin (DAD), jolloin käyttäjä voi tarkastella erotettujen yhdisteiden muodostamaa kromatogrammia aallonpituuksilla 190-900 nm. Jos tutkittavat yhdisteet tunnetaan, käyttäjä voi halutessaan katsoa vain 1: tä tai muutamaa valittua aallonpituutta. Esimerkiksi kokaiinia voidaan havaita 254 nm: ssä.
kuva 2: tyypillinen HPLC-kromatogrammi

kuva 2: Tämä kromatogrammi näyttää yhdisteiden erottumisen kemiallisesta reaktiosta, ja kromatogrammia tarkastellaan aallonpituudella 254 nm. Kaksi päähuippua esiintyvät 8.20 ja 9 minuutin kohdalla, mikä edustaa kahta yhdistettä, joilla on nämä retentioajat. Absorbanssiyksiköiden määrä (AU) esitetään Y-akselilla, kun taas ajonaika esitetään X-akselilla.
Sovellukset
biologiassa ja lääketieteessä HPLC: tä käytetään usein analyyttisenä välineenä biologisten ja ympäristönäytteiden määrityksessä tunnettujen yhdisteiden (esimerkiksi aineenvaihduntatuotteiden, lääkkeiden, toksiinien ja torjunta-aineiden) esiintymisen tai puuttumisen varalta, ja se voi auttaa tuntemattomien yhdisteiden tunnistamisessa.
kemiassa HPLC: tä käytetään kuitenkin rutiininomaisesti kemiallisten reaktioiden seuraamiseen sekä tuotteiden puhtauden määrittämiseen. Lisäksi HPLC: n prosessi voidaan muuttaa preparatiiviseksi HPLC: ksi, jolloin kiinnostavia yhdisteitä voidaan puhdistaa jatkokäyttöä varten.
HPLC voi tuntua aluksi hyvin monimutkaiselta, mutta voit olla varma, kuten useimmat muutkin laboratoriotekniikat, se on paljon järkevämpää, kun todella teet sen.
Stay tuned for my follow-up articles in the coming weeks, in which I will go through some pointers on how you can get the best from your HPLC run depending on your research goal, as well as discuss objectively how HPLC can be used within your research.
Onko tekniikassa muita näkökohtia, joita haluaisit käsitellä yksityiskohtaisemmin? Jos on, haluaisimme kuulla sinusta!
onnellinen HPLC-ing 🙂
onko tämä auttanut sinua? Jaa sitten verkkosi kanssa.