L’expansion réversible d’un gaz idéal peut être utilisée comme exemple de procédé isobare. Un intérêt particulier est la façon dont la chaleur est convertie au travail lorsque l’expansion est effectuée à différentes pressions de gaz de travail / gaz environnant.
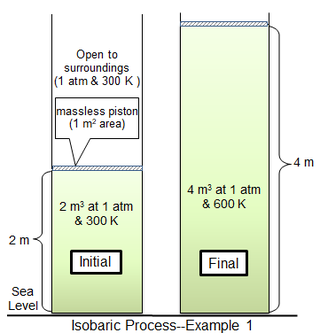
Dans le premier example de procédé, une chambre cylindrique de 1 m2 de surface renferme 81,2438 moles d’un gaz diatomique idéal de masse moléculaire 29 g mol-1 à 300 K. Le gaz environnant est à 1 atm et 300 K, et séparé du gaz de cylindre par un piston mince. Pour le cas limite d’un piston sans masse, le gaz du cylindre est également à une pression de 1 atm, avec un volume initial de 2 m3. La chaleur est ajoutée lentement jusqu’à ce que la température du gaz soit uniformément de 600 K, après quoi le volume de gaz est de 4 m3 et le piston est à 2 m au-dessus de sa position initiale. Si le mouvement du piston est suffisamment lent, la pression du gaz à chaque instant aura pratiquement la même valeur (psys = 1 atm) tout au long.
Pour un gaz diatomique thermiquement parfait, la capacité thermique spécifique molaire à pression constante (cp) est de 7/2R ou 29,1006 J mol−1 deg−1. La capacité calorifique molaire à volume constant (cv) est de 5 / 2R ou 20,7862 J mol−1 deg−1. Le rapport γ{\displaystyle\gamma}

des deux capacités thermiques est de 1,4.
La chaleur Q nécessaire pour amener le gaz de 300 à 600 K est
Q= Δ H = n c p Δ T = 81.2438 × 29.1006 × 300 = 709 , 274 J {\displaystyle Q = {\Delta\mathrm{H}} = n\, c_{p}\, \Delta\mathrm{T} = 81,2438\fois 29.1006\fois 300 = 709,274 {\text {J}}}

.
L’augmentation de l’énergie interne est
Δ U = n c v Δ T = 81.2438 × 20.7862 × 300 = 506 , 625 J {\displaystyle\Delta\U = n \, c_{v}\,\Delta\mathrm{T} = 81,2438\fois 20,7862\fois 300 = 506,625 {\text{J}}}

Par conséquent, W = Q−Δ U = 202, 649 J = N R δ T {\displaystyle W = Q-\Delta U = 202,649 {\text {J}} = nR\Delta\mathrm {T}}

Aussi
W= p δ ν = 1 atm × 2 m3 × 101325 Pa = 202, 650 J {\displaystyle W = {p\Delta\nu} = 1 ~ {\text {atm}} \ times 2 {\text {m3}} \times 101325 {\text{Pa}} = 202,650 {\text{J}}}

, qui est bien sûr identique à la différence entre ΔH et ΔU.
Ici, le travail est entièrement consumé par l’expansion contre l’environnement. De la chaleur totale appliquée (709,3 kJ), le travail effectué (202,7 kJ) représente environ 28,6% de la chaleur fournie.

Le deuxième exemple de procédé est similaire au premier, sauf que le piston sans masse est remplacé par un piston ayant une masse de 10 332.2 kg, ce qui double la pression du gaz de la bouteille à 2 atm. Le volume de gaz de la bouteille est alors de 1 m3 à la température initiale de 300 K. La chaleur est ajoutée lentement jusqu’à ce que la température du gaz soit uniformément de 600 K, après quoi le volume de gaz est de 2 m3 et le piston est à 1 m au-dessus de sa position initiale. Si le mouvement du piston est suffisamment lent, la pression du gaz à chaque instant aura pratiquement la même valeur (psys = 2 atm) tout au long.
Puisque l’enthalpie et l’énergie interne sont indépendantes de la pression,
Q= Δ H = 709,274 J {\displaystyle Q= {\Delta\mathrm{H}} = 709,274 {\text {J}}}

et Δ U = 506,625 J {\displaystyle\Delta U= 506,625 {\text {J}}}

. W = p Δ V = 2 atm × 1 m3 × 101325 Pa = 202,650 J {\displaystyle W = {p\Delta V} = 2 ~ {\text {atm}} \fois 1 ~{\text{m3}} \fois 101325 {\text{Pa}} = 202,650 {\text{J}}}

Comme dans le premier exemple, environ 28,6% de la chaleur fournie est convertie en travail. Mais ici, le travail est appliqué de deux manières différentes: en partie en élargissant l’atmosphère environnante et en partie en soulevant 10 332,2 kg sur une distance h de 1 m.
W l i f t = 10 332,2 kg × 9.80665 m /s2 × 1 m = 101,324 J {\displaystyle W_ {\rm{ascenseur}}=10\,332.2~{\ text {kg}} \times 9.80665 ~{\text{m/s2}} \times 1 {\text{m}} = 101,324 {\text{J}}}

Ainsi, la moitié du travail soulève la masse du piston (travail de gravité, ou travail ”utilisable »), tandis que l’autre moitié élargit l’environnement.
Les résultats de ces deux exemples de processus illustrent la différence entre la fraction de chaleur convertie en travail utilisable (mgΔh) et la fraction de chaleur convertie en travail utilisable (mgΔh). la fraction convertie en travail pression-volume effectué contre l’atmosphère environnante. Le travail utilisable se rapproche de zéro lorsque la pression de gaz de travail se rapproche de celle de l’environnement, tandis que le travail utilisable maximal est obtenu lorsqu’il n’y a pas de pression de gaz environnante. Le rapport de tout le travail effectué à l’apport de chaleur pour une expansion idéale du gaz isobare est
W Q = n R Δ T n c p δ T =2 5 {\displaystyle {\frac {W}{Q}}= {\frac {NR\Delta\mathrm{T}} {nc_ {p}\Delta\mathrm {T}}}= {\frac {2}{5}}}
