următor: 3.4 Frigidere și încălzire: 3. Prima lege anterioară: 3.2 reprezentarea generalizată a conținutului Index
un ciclu Carnot este prezentat în figura 3.4. Are patru procese. Există două picioare reversibile adiabatice și douăpicioare reversibile izoterme. Putem construi un ciclu Carnot cu multe sisteme diferite, dar conceptele pot fi arătate folosind un fluid de lucru familiar, gazul ideal. Sistemul poate fi privit cao cameră închisă de un piston și umplută cu acest gaz ideal.
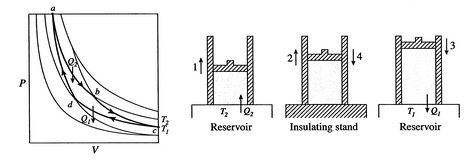
cele patru procese din ciclul Carnot sunt:
- sistemul este la temperatura
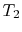 la starea
la starea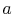 . Este adus în contact cu un rezervor de căldură, care este doar o masă lichidă sau solidă de o măsură suficient de mare, astfel încât temperatura sa să nu se schimbe în mod apreciabil atunci când o anumită cantitate de căldură este transferată în sistem. Cu alte cuvinte, rezervorul de căldură este o temperatură constantăsursă (sau receptor) de căldură. Sistemul suferă apoi o expansiune anizotermică de la
. Este adus în contact cu un rezervor de căldură, care este doar o masă lichidă sau solidă de o măsură suficient de mare, astfel încât temperatura sa să nu se schimbe în mod apreciabil atunci când o anumită cantitate de căldură este transferată în sistem. Cu alte cuvinte, rezervorul de căldură este o temperatură constantăsursă (sau receptor) de căldură. Sistemul suferă apoi o expansiune anizotermică de la 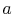 la
la 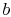 , cu căldură absorbită
, cu căldură absorbită 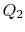 .
. - Atstate
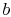 , sistemul este izolat termic (scos din contactwith rezervorul de căldură) și apoi lăsați să se extindă la
, sistemul este izolat termic (scos din contactwith rezervorul de căldură) și apoi lăsați să se extindă la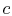 . În timpul thisexpansion temperatura scade la
. În timpul thisexpansion temperatura scade la 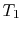 . Schimb de căldurăîn această parte a ciclului,
. Schimb de căldurăîn această parte a ciclului, 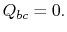 )
) - la starea
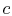 sistemul este adus în contact cu un rezervor de căldură la temperatura
sistemul este adus în contact cu un rezervor de căldură la temperatura 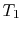 . Este apoi comprimat la starea
. Este apoi comprimat la starea 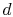 , respingând căldura
, respingând căldura 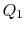 în proces.
în proces. - în cele din urmă, sistemul este comprimat adiabatic înapoi la starea inițială
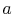 . Schimbul de căldură
. Schimbul de căldură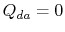 .
.
eficiența termică a ciclului este dată de definiția
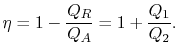 |
(3..4) |
în această ecuație, există o convenție semn implicit. Cantitățile ![]()
![]() așa cum sunt definite sunt mărimile căldurii absorbite șijectate. Cantitățile
așa cum sunt definite sunt mărimile căldurii absorbite șijectate. Cantitățile ![]()
![]() pe de altă parte sunt definitecu referire la căldura primită de sistem. În acest exemplu, fostul este negativ, iar acesta din urmă este pozitiv. Căldura absorbită șirejectată de sistem are loc în timpul proceselor izoterme șiștim deja care sunt valorile lor din Eq.(3.1):
pe de altă parte sunt definitecu referire la căldura primită de sistem. În acest exemplu, fostul este negativ, iar acesta din urmă este pozitiv. Căldura absorbită șirejectată de sistem are loc în timpul proceselor izoterme șiștim deja care sunt valorile lor din Eq.(3.1):
eficiența poate fi acum scrisă în termeni de volume la diferite stări ca
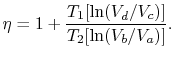 |
(3..5) |
The path from states ![]() to
to ![]() and from
and from ![]() to
to ![]() are bothadiabatic and reversible. For a reversible adiabatic process we knowthat
are bothadiabatic and reversible. For a reversible adiabatic process we knowthat ![]() . Using the ideal gas equation ofstate, we have
. Using the ideal gas equation ofstate, we have ![]() . Along curve
. Along curve![]()
![]() , therefore,
, therefore, ![]() . Alongthe curve
. Alongthe curve ![]()
![]()
![]() . Thus,
. Thus,

Comparing the expression for thermal efficiencyEq. (3.4) with Eq. (3.5) arată două consecințe. În primul rând, încălzirile primite și respinse sunt legate de temperaturile părților izoterme ale ciclului de
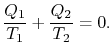 |
(3..6) |
în al doilea rând, eficiența unui ciclu Carnot este dată compact de
 |
(3..7) |
eficiența poate fi de 100% numai dacă temperatura la care este respinsă căldura este zero. Transferurile de căldură și de lucru către și dinspre sistem sunt prezentate schematic în figura 3.5.
ă>
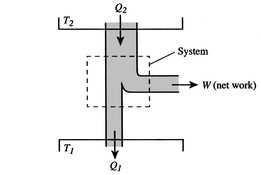
puncte noroioase
Din ![]() , uita la
, uita la![]()
![]() grafic, doeaceasta înseamnă mai departe în afară
grafic, doeaceasta înseamnă mai departe în afară![]()
![]() izoterme sunt mai eficiente? Și dacă ar fi foarte apropiați, ar fifoarte ineficient? (MP 3.2)
izoterme sunt mai eficiente? Și dacă ar fi foarte apropiați, ar fifoarte ineficient? (MP 3.2)
în ciclul Carnot, de ce avem de-a face doar cu modificări de volum șinu cu modificări de presiune asupra adiabatelor și izotermelor?(MP 3.3)
există o aplicație fizică pentru ciclul Carnot? Putem proiecta un motor Carnot pentru un dispozitiv de propulsie?(MP 3.4)
cum știm ce cicluri să folosim ca modele pentru procese reale?(MP 3.5)
următor: 3.4 Frigidere și încălzire: 3. Prima Lege Anterioară: 3.2 reprezentarea generalizată a conținutului Index
UnifiedTP