Legea proporțiilor Multiple
odată stabilită ideea că elementele combinate în proporții definite pentru a forma compuși, experimentele au început, de asemenea, să demonstreze că aceleași perechi de anumite elemente se pot combina pentru a forma mai mult de un compus. Luați în considerare elementele carbon și oxigen. Combinate într-un fel, ele formează compusul familiar numit dioxid de carbon. În fiecare probă de dioxid de carbon, există \(32,0 \: \text{g}\) de oxigen prezent pentru fiecare \(12,0 \: \text{g}\) de carbon. Prin împărțirea \(32,0\) la \(12,0\), acest lucru simplifică la un raport de masă de oxigen la carbon de 2,66 la 1. Există un alt compus care se formează din combinația de carbon și oxigen numită monoxid de carbon. Fiecare probă de monoxid de carbon conține \(16,0 \: \text{g}\) de oxigen pentru fiecare \(12,0 \: \text{g}\) de carbon. Acesta este un raport de masă de oxigen la carbon de 1,33 la 1. În dioxidul de carbon, există exact de două ori mai mult oxigen decât în monoxidul de carbon. Acest exemplu ilustrează Legea proporțiilor multiple: ori de câte ori aceleași două elemente formează mai mult de un compus, diferitele mase ale unui element care se combină cu aceeași masă a celuilalt element sunt în raportul numerelor întregi mici.
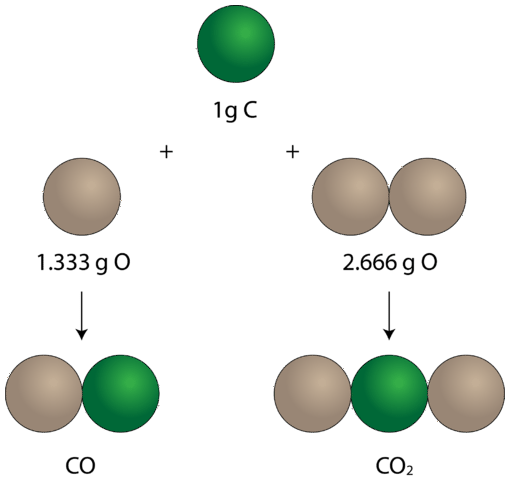
în monoxidul de carbon, în stânga, există \(1.333 \: \text{g}\) de oxigen pentru fiecare \(1 \: \text{g}\) de carbon. În dioxidul de carbon, în dreapta, există \(2.666 \: \text{g}\) de oxigen pentru fiecare gram de carbon. Deci raportul dintre oxigen în cei doi compuși este 1: 2, un raport mic al numărului întreg.
diferența dintre monoxidul de carbon și dioxidul de carbon este semnificativă. Monoxidul de Carbon este un gaz mortal, format din arderea incompletă a unor materiale care conțin carbon (cum ar fi lemnul și benzina). Acest compus se va atașa de hemoglobină în celulele roșii din sânge și va bloca legarea oxigenului de acele celule. Dacă oxigenul nu se leagă, acesta nu poate fi transportat în celulele corpului acolo unde este necesar și poate apărea moartea. Dioxidul de Carbon, pe de altă parte, nu este toxic ca monoxidul de carbon. Cu toate acestea, poate deplasa oxigenul în sisteme, deoarece este mai greu. Stingătoarele cu dioxid de Carbon taie fluxul de oxigen într-un incendiu, stingând focul.