delocalizarea are loc atunci când sarcina electrică este răspândită pe mai mult de un atom. De exemplu, electronii de legătură pot fi distribuiți între mai mulți atomi care sunt legați împreună.

Exemplul 1:
unul dintre cele mai cunoscute exemple ale unei molecule în care electronii de legătură sunt delocalizați este benzenul, prezentat mai jos:
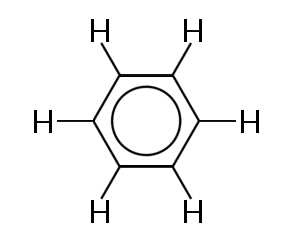
benzenul constă dintr-un inel de șase atomi de carbon. Atomii de carbon sunt toți hibridizați sp2 cu un orbital p nehidridizat.
orbitalii hibrizi sp2 produc legături covalente normale, uneori numite legături de tip inqq: acestea sunt legăturile C-C simple și legăturile C-H simple.
Acest lucru lasă fiecare carbon cu un electron într-un orbital p la un unghi drept față de planul inelului.
în diagrama de mai jos, în stânga puteți vedea orbitalii sp2 formând legături covalente. În dreapta, puteți vedea orbitalii p, fiecare conținând un electron.
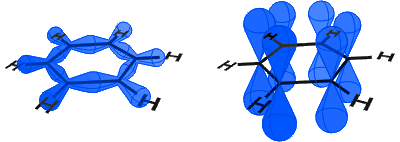
orbitalii p se combină lateral și electronii din orbitalii p sunt descriși ca fiind electroni de la un nivel la altul.
în diagrama de mai jos, orbitalii p s-au combinat, iar electronii-inqc sunt delocalizați. În medie, toate legăturile inelare sunt identice.
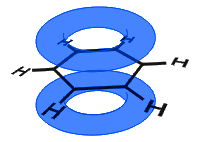
spre deosebire de următorul exemplu de mai jos, electronii delocalizați din benzen sunt ținuți în moleculă și nu sunt liberi să se deplaseze prin materialul în vrac.
Exemplul 2: metalele au o conductivitate termică și electrică ridicată, deoarece electronii exteriori din atomii lor sunt delocalizați. Acești electroni nu sunt asociați cu un anumit nucleu metalic și, prin urmare, sunt liberi să se miște în tot metalul.
recunoaștere: imaginile colorate în albastru ale orbitalilor benzenului sunt curtoazie de Sansculotte. Aceste imagini sunt licențiate sub Creative Commons Attribution-Share Alike 1.0 Generic license.