o celulă voltaică, adesea cunoscută sub numele de celulă galvanică, furnizează energie electrică. Sursa acestei energii este o reacție chimică spontană, mai precis o reacție spontană redox.
de exemplu, toate bateriile sunt fabricate din una sau mai multe celule voltaice;bateriile se opresc atunci când majoritatea sau toți reactanții lor au fost transformați în produse, transformând energia lor potențială chimică în energie electrică.
celule voltaice – procesul de bază
energie potențială chimică energie electrică
celula voltaică este unul dintre cele două tipuri de bază de celule electrochimice.Celălalt tip este celula electrolitică; într-o celulă electrolitică, energia electrică este utilizată pentru a conduce o reacție chimică non-spontană.De exemplu, apa poate fi împărțită în hidrogen și oxigen într-o celulă electrolitică. De asemenea, atunci când o baterie reîncărcabilă este reîncărcată, aceasta funcționează ca o celulă electrolitică.
schema celulei voltaice de bază

reacțiile redox spontane la electrozi produc o tensiune.Configurat corect, această tensiune poate conduce electronii prin dispozitive electrice, cum ar fi becul prezentat here.In această diagramă, speciile transferă electroni către anod de unde curg prin bec către catod, unde produc reducere.
schema celulară electrolitică de bază
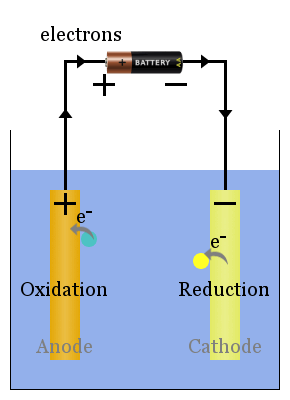
non-spontană reacțiile redox sunt conduse de o tensiune externă.Procesele celulei electrolitice sunt opuse celulelor voltaice. curentul de la sursa de energie împinge electronii spre catod, unde provoacă reducerea speciilor.
citiți mai multe aici despre catozi și anozi în celulele voltaice vs electrolitice.
exemplu de celulă voltaică
bateria Edison
bateria Edison este o celulă simplă, reîncărcabilă, inventată de Thomas Edison.It constă din doi electrozi metalici, unul din fier, celălalt din nichel.În timpul încărcării inițiale, se formează un strat de oxid de nichel pe electrodul de nichel.
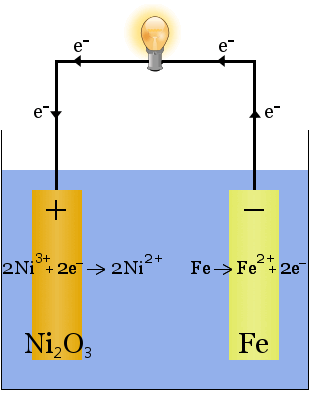
electrolitul (lichidul ionic dintre electrozi) este de 20-30% în greutate hidroxid de potasiu în apă.Rolul hidroxidului de potasiu în acest caz este de a crește conductivitatea ionică pentru a finaliza circuitul electric – hidroxidul de potasiu nu este consumat în reacție.
când se descarcă, celula Edison funcționează ca o celulă voltaică.Când este încărcată, celula funcționează ca o celulă electrolitică.
ecuațiile chimice pentru reacțiile la electrozi sunt:
în timpul descărcării, atunci când celula furnizează energie electrică, reacțiile de mai sus se îndreaptă spre dreapta.
în timpul încărcării, când celula transformă energia electrică în energie potențială chimică, reacțiile de mai sus se îndreaptă spre stânga.
celula Edison, cu ambii electrozi care împart același electrolit, este una dintre cele mai simple celule voltaice în utilizare practică; majoritatea celulelor voltaice sunt mai complicate.Marile sale avantaje sunt robustețea sa remarcabilă împotriva erorilor, cum ar fi supraîncărcarea și durata sa de viață foarte lungă, cu ciclism de încărcare-descărcare aproape nelimitat.
cel mai mare dezavantaj al său este că, în raport cu producția sa de energie, este foarte grea.
exemplu suplimentar
Baterii cu litiu
progresele în tehnologia bateriei au condus miniaturizarea dispozitivelor electronice.Fără aceste progrese, dispozitivele moderne, cum ar fi telefoanele mobile și tabletele, ar fi mai mari și mai greoaie.
în centrul acestor progrese a fost tehnologia litiu-ion.Elementul litiu este un metal cu densitate foarte mică: la 0,534 g/cm3 litiul este pe jumătate la fel de dens ca apa; litiul plutește pe apă.Comparați acest lucru cu metalele din celula Edison, densitatea nichelului este de 8,908 g/cm3, iar fierul este de 7,874 g/cm3: acestea sunt cu peste 10 ori mai mari decât densitatea litiului.
potențialul redox ridicat al litiului, combinat cu densitatea scăzută, face ca ionii săi să fie perfecți pentru utilizarea ca material pentru baterii.
o baterie tipică litiu-ion se bazează pe electrozi poroși care permit ionilor Li să se deplaseze în și din porii lor.De exemplu, o baterie reîncărcabilă Litiu-ion ar putea avea un electrod de grafit și un electrod de oxid de cobalt dopat cu litiu cu un electrolit de polioxietilenă care conține sarea LiPF6.
când o astfel de baterie alimentează un dispozitiv, atomii de litiu ținuți în structura stratului de anod de grafit sunt oxidați pentru a deveni ioni.
la catod, ionii de litiu sunt reduși în structura oxidului de cobalt.
These reactions are reversed when the cell is being charged.
