The chemical element krypton is classed as a noble gas and a nonmetal. It was discovered in 1898 by William Ramsay and his assistant Morris Travers.

Data Zone
| Classification: | Krypton is a noble gas and a nonmetal |
| Color: | colorless |
| Atomic weight: | 83.80 |
| State: | gas |
| Melting point: | -157.3 oC, 115.9 K |
| Boiling point: | -153.2 oC, 119.4 K |
| Electrons: | 36 |
| Protons: | 36 |
| Neutrons in most abundant isotope: | 48 |
| Electron shells: | 2,8,18,8 |
| Electron configuration: | 3d10 4s2 4p6 |
| Density @ 20oC: | 0.003708 g/cm3 |
Show more, including: Heats, Energies, Oxidation,
Reactions, Compounds, Radii, Conductivities
| Atomic volume: | 38.9 cm3/mol |
| Structure: | fcc: face-centered cubic |
| Hardness: | – |
| Specific heat capacity | 0.248 J g-1 K-1 |
| Heat of fusion | 1.638 kJ mol-1 |
| Heat of atomization | 0 kJ mol-1 |
| Heat of vaporization | 9.029 kJ mol-1 |
| 1st ionization energy | 1350.7 kJ mol-1 |
| 2nd ionization energy | 2350.3 kJ mol-1 |
| 3rd ionization energy | 3565.1 kJ mol-1 |
| Electron affinity | – kJ mol-1 |
| Minimum oxidation number | 0 |
| Min. common oxidation no. | 0 |
| Maximum oxidation number | 2 |
| Max. common oxidation no. | 2 |
| Electronegativity (Pauling Scale) | 3 |
| Polarizability volume | 2.5 Å3 |
| Reaction with air | none |
| Reaction with 15 M HNO3 | none |
| Reaction with 6 M HCl | none |
| Reaction with 6 M NaOH | none |
| Oxide(s) | none |
| Hydride(s) | none |
| Chloride(s) | none |
| Atomic radius | 88 pm |
| Ionic radius (1+ ion) | – |
| Ionic radius (2+ ion) | – |
| Ionic radius (3+ ion) | – |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | 0.01 W m-1 K-1 |
| Electrical conductivity | – |
| Freezing/Melting point: | -157.3 oC, 115.9 K |
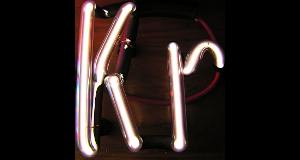
Krypton gas glows with the help of a few thousand volts. Image: Pslawinski.

Kryptons Spektrum.

William Ramsay zeigt auf die letzte Spalte des Periodensystems, die die edlen (oder inerten) Gase enthält. Ramsay erhielt den Nobelpreis für Chemie im Jahr 1904 für seine Arbeit in der Entdeckung der Inertgase. Bild: Vanity Fair

>Ein Kryptonionen-568-nm-Tertiärlaser, der in der Proteinforschung eingesetzt wird. Foto: Zentrum für Krebsforschung
Entdeckung von Krypton
Der schottische Chemiker William Ramsay und sein Assistent englischer Chemiker Morris Travers entdeckten Krypton 1898 in London.
Ramsay hatte zuvor Helium und Argon entdeckt. Er war sich bewusst, dass mehr neue Elemente in derselben Gruppe des Periodensystems liegen müssen.
Ramsay und Travers betrachteten die Lücke im Periodensystem zwischen Helium und Argon. Sie argumentierten, dass ein neues Element (es heißt jetzt Neon) existieren muss, um diese Lücke zu füllen; Sie waren entschlossen, es zu finden. Und sie fanden es, aber erst nachdem ihre Suche ein weiteres neues Element enthüllt hatte: Krypton. (1)
Ramsay war sich der Geschichte der Chemie bewusst und wusste, dass manchmal ein neues Element ein anderes verbergen kann. Zum Beispiel hatte Johan Gadolin Yttrium in dem Mineral entdeckt, das wir jetzt Gadolinit nennen. Einige Jahre später entdeckte Carl Gustaf Mosander die neuen Elemente Erbium und Terbium in Gadolinit; Sie waren die ganze Zeit dort gewesen, aber Gadolin hatte sie nicht gefunden. Ramsay wunderte sich über die Möglichkeit, kleine Mengen des schwer fassbaren neuen Elements zu finden, das sich in einer seiner früheren Entdeckungen, Argon, versteckt.
Ramsay und Travers beschlossen, eine große Menge Argon aus der Luft zu extrahieren. Sie verflüssigten das Argon und destillierten es dann in separate Fraktionen, um zu sehen, ob die leichtesten Fraktionen das neue Gas enthielten. (2)
Mit wenig Erfahrung im Umgang mit Flüssiggasen erhielten sie einen Liter flüssige Luft, um herauszufinden, wie man damit arbeitet. In ihrer praktischen Arbeit verdampften sie das meiste davon und ließen nur 100 ml übrig. Ramsay wusste, dass es höchst unwahrscheinlich war, dass das neue Gas, leichter als Argon, in dieser Restprobe vorhanden sein könnte, Aber die aufregende Idee kam ihm, dass ein neues, schwereres Gas nur vorhanden sein könnte.
In diesem Sinne entfernte Travers Sauerstoff und Stickstoff aus dem Gas mit glühendem Kupfer und Magnesium. Er legte eine Probe des verbleibenden Gases in eine Vakuumröhre und legte eine Hochspannung an, um das Spektrum des Gases zu messen.
Er stellte fest, dass Argon wie erwartet vorhanden war, aber auch zwei neue brillante Linien, eine gelbe und eine grüne, die noch nie zuvor gesehen worden waren. Ramsay und Travers maßen das Verhältnis der spezifischen Wärme des Gases bei konstantem Druck zu seiner spezifischen Wärme bei konstantem Volumen und fanden heraus, dass es 1,66 betrug. Dieser Wert konnte nur erhalten werden, wenn das neue Gas aus einzelnen Atomen bestand, was beweist, dass es sich nicht um eine Verbindung handeln konnte. Wenn es keine Verbindung war, musste es ein neues Element sein.
Krypton wurde entdeckt. Ramsay wählte den Namen des Elements aus dem griechischen Wort ‚kryptos‘ Bedeutung ‚versteckt.Viele Jahre nach der Entdeckung der Edelgase glaubten die meisten Wissenschaftler, dass sie keine Verbindungen bilden würden. Dies stellte sich als falsch heraus. William Ramsay (William Ramsay) glaubte wirklich, dass Zusammensetzungen möglich sein würden, 1902 schreibend: „Ich habe seit langem die Idee gehabt, dass Krypton und Xenon in Kombinationen viel leichter eingehen können als die anderen Gase; aber wie man es herbeiführt?“ (3)
Es dauerte weitere 60 Jahre, bis seine Frage beantwortet war. (Siehe interessante Fakten unten.William Ramsay erhielt 1904 den Nobelpreis für Chemie, „in Anerkennung seiner Verdienste um die Entdeckung der inerten gasförmigen Elemente in der Luft und seiner Bestimmung ihres Platzes im Periodensystem.“ Er war dafür verantwortlich, dem Periodensystem eine ganz neue Gruppe hinzuzufügen. Radon war das einzige Edelgas, das er nicht entdeckte.
Interessante Fakten über Krypton
- Zwischen 1960 und 1983 wurde die wissenschaftliche Längeneinheit, der Meter, als 1 650 763 definiert.73 Wellenlängen der orange-roten Spektrallinie von Krypton-86. (Das Messgerät ist jetzt definiert als die Entfernung, die Licht in einem Vakuum während eines Zeitintervalls von
1/299 792 458 einer Sekunde zurücklegt.) - Von seiner Entdeckung im Jahr 1898 bis in die 1960er Jahre glaubten die meisten Wissenschaftler, dass es unmöglich sei, Verbindungen aus Krypton oder einem anderen Edelgas herzustellen – obwohl siehe William Ramsay, oben. Kryptondifluorid wurde 1963 hergestellt. Es ist ein weißer, kristalliner Feststoff, stabil bei Temperaturen unter -30 oC. (4)
- Krypton kommt in der Atmosphäre unseres Planeten nicht sehr häufig vor: Für jedes Kryptonatom gibt es etwa 8200 Argonatome, 184 000 Sauerstoffmoleküle und 685 000 Stickstoffmoleküle.Krypton-85 in der Atmosphäre kann verwendet werden, um das Vorhandensein von ansonsten geheimen Forschungs- und Produktionsanlagen für Atomwaffen nachzuweisen. (5)
- Krypton-Fluor-Laser erzeugen Pulse mit der 500-fachen Leistung des gesamten US-Stromnetzes. Es überrascht nicht, dass diese Impulse von kurzer Dauer sind: vier Milliardstel Sekunden. (6)


Krypton leuchtet bei hoher Spannung in einer elektrischen Entladungsröhre. Foto: Alchemist-hp
Aussehen und Eigenschaften
Schädliche Wirkungen:
Krypton gilt als ungiftig.
Eigenschaften:
Krypton ist ein farbloses, geruchloses Inertgas.
Obwohl es extrem unreaktiv ist, kann Krypton mit dem sehr reaktiven Gas Fluor reagieren. Einige Verbindungen von Krypton wurden hergestellt, einschließlich Krypton (II) fluorid und Krypton Clathrate.
Festes Krypton ist weiß und kristallin.
Verwendung von Krypton
Krypton wird in Beleuchtungsprodukten verwendet:
Eine wichtige Verwendung findet sich in leistungsstarken, blinkenden Start- und Landebahnlichtern.
Ionisiertes Kryptongas erscheint weißlich – siehe Foto links – was Krypton-basierte Glühbirnen als brillante weiße Lichtquelle in der Hochgeschwindigkeitsfotografie nützlich macht.
Krypton wird zusammen mit anderen Gasen verwendet, um leuchtende Neonlicht-Schilder herzustellen, die mit einem grünlich-gelben Licht leuchten.
Krypton wird als Füllgas für energiesparende Leuchtstofflampen und als inertes Füllgas in Glühlampen verwendet.Die relative Häufigkeit von Krypton im Vergleich zu Wasserstoff kann von Astronomen verwendet werden, um zu messen, wie viel Nukleosynthese (Elementbildung) in einer Region des interstellaren Raums stattgefunden hat. (7)
Zwischen 1960 und 1983 definierte ein internationales Abkommen die Meterlänge in Bezug auf die Wellenlänge des vom Kryptonisotop 86Kr emittierten Lichts. (Das Messgerät ist jetzt definiert als die Entfernung, die Licht im Vakuum während einer Zeit von 1/299.792.458 einer Sekunde zurücklegt. Die Zeit wird mit einer Cäsium-Atomuhr gemessen.)
Abundanz und Isotope
Abundanz Erdkruste: 100 Teile pro Billion nach Gewicht, 30 Teile pro Billion nach Mol
Abundanz Sonnensystem: Teile pro Million nach Gewicht, Teile pro Million nach Mol
Kosten, rein: $ 33 pro 100g
Kosten, Bulk: $ pro 100g
Quelle: Krypton wird kommerziell durch fraktionierte Destillation von flüssiger Luft gewonnen.
Isotope: Krypton hat 25 Isotope, deren Halbwertszeiten bekannt sind, mit Massenzahlen 71 bis 95. Natürlich vorkommendes Krypton ist eine Mischung aus sechs Isotopen und sie werden in den angegebenen Prozentsätzen gefunden: 78Kr (0,4%), 80Kr (2,3%), 82kr (11,6%), 83Kr (11,5%), 84Kr (57,0%) und 86Kr (17,3%). Das am häufigsten vorkommende Isotop ist 84Kr bei 57,0%.

- William Ramsay, Nobelpreisvorlesung., 12. Dezember 1904.William Ramsay, Die kürzlich entdeckten Gase und ihre Beziehung zum periodischen Gesetz., Wissenschaft, 1898, Vol. IX, S. 273-280.Leonello Paoloni, Die Edelgasverbindungen: die Ansichten von William Ramsay und Giuseppe Oddo im Jahr 1902. In : J. Chem. Educ., 1983, 60 (9), S. 758.
- D. R. MacKenzie, Kryptondifluorid: Vorbereitung und Handhabung., Wissenschaft 20 September 1963, Vol. 141 Nr. 3586 p1171.BBC Report, New N Korea nuclear plant suspected Sunday, 20 July, 2003.
- Marineforschungslabor, Krypton-Fluor-Laser.Stefan I. B. Cartledge et al., Interstellar Krypton Abundances: The Detection of Kiloparsec-scale Differences in Galactic Nucleosynthetic History. 2008: Astrophysical Journal., 687, S. 1043.
Diese Seite zitieren
Für Online-Links kopieren Sie bitte einen der folgenden Links und fügen Sie ihn ein:
<a href="https://www.chemicool.com/elements/krypton.html">Krypton</a>
oder
<a href="https://www.chemicool.com/elements/krypton.html">Krypton Element Facts</a>
Um diese Seite in einem wissenschaftlichen Dokument zu zitieren, verwenden Sie bitte das folgende MLA-konforme Zitat:
"Krypton." Chemicool Periodic Table. Chemicool.com. 17 Oct. 2012. Web. <https://www.chemicool.com/elements/krypton.html>.