The chemical element krypton is classed as a noble gas and a nonmetal. It was discovered in 1898 by William Ramsay and his assistant Morris Travers.

Data Zone
| Classification: | Krypton is a noble gas and a nonmetal |
| Color: | colorless |
| Atomic weight: | 83.80 |
| State: | gas |
| Melting point: | -157.3 oC, 115.9 K |
| Boiling point: | -153.2 oC, 119.4 K |
| Electrons: | 36 |
| Protons: | 36 |
| Neutrons in most abundant isotope: | 48 |
| Electron shells: | 2,8,18,8 |
| Electron configuration: | 3d10 4s2 4p6 |
| Density @ 20oC: | 0.003708 g/cm3 |
Show more, including: Heats, Energies, Oxidation,
Reactions, Compounds, Radii, Conductivities
| Atomic volume: | 38.9 cm3/mol |
| Structure: | fcc: face-centered cubic |
| Hardness: | – |
| Specific heat capacity | 0.248 J g-1 K-1 |
| Heat of fusion | 1.638 kJ mol-1 |
| Heat of atomization | 0 kJ mol-1 |
| Heat of vaporization | 9.029 kJ mol-1 |
| 1st ionization energy | 1350.7 kJ mol-1 |
| 2nd ionization energy | 2350.3 kJ mol-1 |
| 3rd ionization energy | 3565.1 kJ mol-1 |
| Electron affinity | – kJ mol-1 |
| Minimum oxidation number | 0 |
| Min. common oxidation no. | 0 |
| Maximum oxidation number | 2 |
| Max. common oxidation no. | 2 |
| Electronegativity (Pauling Scale) | 3 |
| Polarizability volume | 2.5 Å3 |
| Reaction with air | none |
| Reaction with 15 M HNO3 | none |
| Reaction with 6 M HCl | none |
| Reaction with 6 M NaOH | none |
| Oxide(s) | none |
| Hydride(s) | none |
| Chloride(s) | none |
| Atomic radius | 88 pm |
| Ionic radius (1+ ion) | – |
| Ionic radius (2+ ion) | – |
| Ionic radius (3+ ion) | – |
| Ionic radius (1- ion) | – |
| Ionic radius (2- ion) | – |
| Ionic radius (3- ion) | – |
| Thermal conductivity | 0.01 W m-1 K-1 |
| Electrical conductivity | – |
| Freezing/Melting point: | -157.3 oC, 115.9 K |
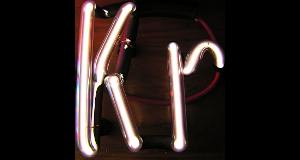
Krypton gas glows with the help of a few thousand volts. Image: Pslawinski.

Spectrul lui Krypton.

William Ramsay arătând spre coloana finală a tabelului periodic care conține gazele nobile (sau inerte). Ramsay a primit Premiul Nobel pentru Chimie în 1904 pentru munca sa în descoperirea gazelor inerte. Imagine: Vanity Fair

>un laser terțiar cu ioni kripton 568 nm utilizat în cercetarea proteinelor. Foto: Centrul de cercetare a cancerului
descoperirea Kriptonului
chimistul scoțian William Ramsay și asistentul său chimist englez Morris Travers au descoperit kriptonul în 1898 la Londra. Ramsay descoperise anterior heliu și argon. El era conștient de faptul că mai multe elemente noi trebuie să se afle în același grup al tabelului periodic.Ramsay și Travers au luat în considerare decalajul din tabelul periodic dintre heliu și argon. Ei au argumentat că un element nou (acum se numește neon) trebuie să existe pentru a umple acest gol; erau hotărâți să-l găsească. Și au găsit – o, dar numai după ce căutarea lor a dezvăluit pentru prima dată un alt element nou: krypton. (1)
conștient de istoria chimiei, Ramsay știa că uneori un element nou poate ascunde altul. De exemplu, Johan Gadolin descoperise ytriul în mineralul pe care îl numim acum gadolinit. Câțiva ani mai târziu, Carl Gustaf Mosander a descoperit noile elemente erbiu și terbiu în gadolinit; au fost acolo tot timpul, dar Gadolin nu le-a găsit. Ramsay s-a întrebat despre posibilitatea de a găsi cantități mici din noul element evaziv ascuns într-una din descoperirile sale anterioare, argon. Ramsay și Travers au decis să extragă un volum mare de argon din aer. Ar lichefia argonul și apoi l-ar distila în fracții separate pentru a vedea dacă cele mai ușoare fracții conțin noul gaz. (2)
cu puțină experiență în manipularea gazelor lichide, au obținut un litru de aer lichid pentru a afla cum să lucreze cu acesta. În activitatea lor de practică, au evaporat cea mai mare parte, lăsând doar 100 ml. Ramsay știa că este foarte improbabil ca noul gaz, mai ușor decât argonul, să poată fi prezent în această probă reziduală, dar ideea interesantă i-a venit că un gaz nou, mai greu, ar putea fi prezent.având în vedere acest lucru, Travers a eliminat oxigenul și azotul din gaz folosind cupru și magneziu roșu-fierbinte. El a plasat o mostră din gazul rămas într-un tub de vid și a aplicat o tensiune înaltă pentru a măsura spectrul gazului.
el a descoperit că argonul era prezent, așa cum era de așteptat, dar și două noi linii strălucitoare, una galbenă și una verde, care nu au mai fost văzute până acum. Ramsay și Travers au măsurat raportul dintre căldura specifică a gazului la presiune constantă și căldura specifică la volum constant și au constatat că este de 1,66. Această valoare ar putea fi obținută numai dacă noul gaz ar consta din atomi unici, dovedind că nu poate fi un compus. Dacă nu era un compus, trebuia să fie un element nou.
Krypton a fost descoperit. Ramsay a ales numele elementului din cuvântul grecesc ‘kryptos’ care înseamnă ‘ ascuns.timp de mulți ani după descoperirea gazelor nobile, majoritatea oamenilor de știință au crezut că nu vor forma compuși. Acest lucru sa dovedit a fi incorect.
William Ramsay credea de fapt că compușii ar fi posibili, scriind în 1902: „am avut de mult timp ideea că kriptonul și xenonul pot intra în combinații mult mai ușor decât celelalte gaze; dar cum să o producem?”(3)
a durat încă 60 de ani înainte ca întrebarea lui să primească răspuns. (A se vedea Fapte interesante de mai jos.William Ramsay a primit Premiul Nobel pentru Chimie în 1904, „ca recunoaștere a serviciilor sale în descoperirea elementelor gazoase inerte din aer și determinarea locului lor în sistemul periodic.”El a fost responsabil pentru adăugarea unui întreg grup nou la tabelul periodic. Radonul a fost singurul gaz nobil pe care nu l-a descoperit.
fapte interesante despre Krypton
- între 1960 și 1983, unitatea științifică de lungime, contorul, a fost definită ca 1 650 763.73 lungimi de undă ale liniei spectrale portocaliu-roșu krypton-86. (Contorul este acum definit ca distanța parcursă de lumină în vid într-un interval de timp de
1/299 792 458 de secundă.) - de la descoperirea sa în 1898 până în anii 1960, majoritatea oamenilor de știință au crezut că este imposibil să se facă compuși de kripton sau orice alt gaz nobil – deși vezi William Ramsay, mai sus. Difluorura de kripton a fost făcută în 1963. Este un solid alb, cristalin, stabil la temperaturi sub -30 oC. (4)
- Krypton nu este foarte abundent în atmosfera planetei noastre: Pentru fiecare atom de kripton, există aproximativ 8200 de atomi de argon, 184 000 de molecule de oxigen și 685 000 de molecule de azot.
- Krypton-85 în atmosferă poate fi folosit pentru a detecta prezența instalațiilor de cercetare și producție a armelor nucleare altfel secrete. (5)
- laserele Krypton-fluor produc impulsuri cu o putere de 500 de ori mai mare decât întreaga rețea electrică din SUA. Nu este surprinzător că aceste impulsuri au o durată scurtă: patru miliarde de secunde. (6)


Krypton strălucind la tensiune înaltă într-un tub de descărcare electrică. Foto: Alchemist-hp
aspect și caracteristici
efecte nocive:
Krypton este considerat a fi non-toxic.
caracteristici:
Krypton este un gaz inert incolor, inodor.
deși este extrem de neractiv krypton poate reacționa cu fluor gaz foarte reactiv. Au fost preparați câțiva compuși de kripton, inclusiv fluorură de kripton (II) și clatrați de kripton.
kriptonul Solid este alb și cristalin.
utilizări ale Kriptonului
Kriptonul este utilizat în produsele de iluminat:
o utilizare importantă este în luminile de pistă intermitente de mare putere ale aeroportului.
gazul kripton ionizat apare albicios – vezi fotografia din stânga – ceea ce face ca becurile pe bază de kripton să fie utile ca sursă de lumină albă strălucitoare în fotografia de mare viteză.
Kriptonul este folosit alături de alte gaze pentru a face semne luminoase de stil neon care strălucesc cu o lumină galben-verzuie.
Kriptonul este utilizat ca gaz de umplere pentru luminile fluorescente care economisesc energie și ca gaz de umplere inert în becurile incandescente.abundența relativă a kriptonului față de hidrogen poate fi folosită de astronomi pentru a măsura cât de multă nucleosinteză (formarea elementelor) a avut loc în orice regiune a spațiului interstelar. (7)
între 1960 și 1983, un acord internațional a definit lungimea contorului în ceea ce privește lungimea de undă a luminii emise de izotopul krypton, 86Kr. (Contorul este acum definit ca distanța parcursă de lumină în vid într-un timp de 1/299,792,458 de secundă. Timpul este măsurat folosind un ceas atomic de cesiu.)
abundență și izotopi
abundență crusta pământului: 100 părți pe trilion în greutate, 30 părți pe trilion de alunițe
abundență sistemul solar: părți pe milion în greutate, părți pe milion de alunițe
cost, pur: 33 USD pe 100g
Cost, în vrac: $ per 100g
Sursa: Krypton se obține comercial prin distilarea fracționată a aerului lichid.
izotopi: kryptonul are 25 de izotopi ale căror timpi de înjumătățire sunt cunoscuți, cu numere de masă de la 71 la 95. Kriptonul natural este un amestec de șase izotopi și se găsesc în procentele prezentate: 78Kr (0,4%), 80kr (2,3%), 82kr (11,6%), 83kr (11,5%), 84kr (57,0%) și 86kr (17,3%). Cel mai abundent izotop este 84kr la 57,0%.

citează această pagină
pentru conectarea online, copiați și lipiți una dintre următoarele:
<a href="https://www.chemicool.com/elements/krypton.html">Krypton</a>
sau
<a href="https://www.chemicool.com/elements/krypton.html">Krypton Element Facts</a>
pentru a cita această pagină într-un document academic, vă rugăm să folosiți următoarea citare conformă MLA:
"Krypton." Chemicool Periodic Table. Chemicool.com. 17 Oct. 2012. Web. <https://www.chemicool.com/elements/krypton.html>.