- Iluminacióneditar
- Termometría de fosforeditar
- Juguetes que brillan en la oscuraeditar
- Estampillas de franqueaeditar
- radioluminiscencia Edit
- Electroluminiscenciaeditar
- Led blancoseditar
- rayos Catódicos tubesEdit
- CRTS de televisión en blanco y negroeditar
- CRTS de color de paleta reducida Edit
- CRTS de televisión en coloreditar
- Televisores de proyectacióneditar
Iluminacióneditar
Las capas de fósforo proporcionan la mayor parte de la luz producida por las lámparas fluorescentes, y también se utilizan para mejorar el equilibrio de la luz producida por las lámparas de halogenuros metálicos. Varios letreros de neón usan capas de fósforo para producir diferentes colores de luz. Las pantallas electroluminiscentes que se encuentran, por ejemplo, en los paneles de instrumentos de los aviones, utilizan una capa de fósforo para producir iluminación sin deslumbramiento o como dispositivos de visualización numérica y gráfica. Las lámparas LED blancas consisten en un emisor azul o ultravioleta con un revestimiento de fósforo que emite a longitudes de onda más largas, lo que proporciona un espectro completo de luz visible. Los tubos de rayos catódicos desenfocados y no filtrados se utilizaron como lámparas estroboscópicas desde 1958.
Termometría de fosforeditar
La termometría de fósforo es un enfoque de medición de temperatura que utiliza la dependencia de la temperatura de ciertos fósforos. Para ello, se aplica un revestimiento de fósforo a una superficie de interés y, por lo general, el tiempo de descomposición es el parámetro de emisión que indica la temperatura. Debido a que la iluminación y la óptica de detección se pueden ubicar de forma remota, el método se puede usar para superficies móviles, como superficies de motores de alta velocidad. Además, el fósforo se puede aplicar al extremo de una fibra óptica como un análogo óptico de un termopar.
Juguetes que brillan en la oscuraeditar
En estas aplicaciones, el fósforo se agrega directamente al plástico utilizado para moldear los juguetes, o se mezcla con un aglutinante para su uso como pinturas.
ZnS: El fósforo Cu se utiliza en cremas cosméticas que brillan en la oscuridad que se usan con frecuencia para maquillajes de Halloween.Generalmente, la persistencia del fósforo aumenta a medida que aumenta la longitud de onda. Consulte también la barra de luz para artículos brillantes a base de quimioluminiscencia.
Estampillas de franqueaeditar
Los sellos con bandas de fósforo aparecieron por primera vez en 1959 como guías para máquinas para ordenar el correo. En todo el mundo existen muchas variedades con diferentes cantidades de bandas. Los sellos postales a veces se recogen por si están o no» marcados » con fósforo (o impresos en papel luminiscente).
radioluminiscencia Edit
Los fósforos de sulfuro de zinc se utilizan con materiales radiactivos, donde el fósforo fue excitado por los isótopos en descomposición alfa y beta, para crear pintura luminiscente para esferas de relojes e instrumentos (esferas de radio). Entre 1913 y 1950, el radio-228 y el radio-226 se utilizaron para activar un fósforo hecho de sulfuro de zinc dopado con plata (ZnS:Ag), que daba un brillo verdoso. El fósforo no es adecuado para ser utilizado en capas de más de 25 mg/cm2, ya que la autoabsorción de la luz se convierte en un problema. Además, el sulfuro de zinc sufre una degradación de su estructura de celosía cristalina, lo que conduce a una pérdida gradual de brillo significativamente más rápida que el agotamiento del radio. Las pantallas de espintariscopio recubiertas de ZnS:Ag fueron utilizadas por Ernest Rutherford en sus experimentos descubriendo el núcleo atómico.
El sulfuro de zinc dopado con cobre (ZnS: Cu) es el fósforo más común utilizado y produce luz azul verdosa. El sulfuro de zinc dopado con cobre y magnesio (ZnS:Cu,Mg) produce luz amarillo-naranja.
El tritio también se utiliza como fuente de radiación en varios productos que utilizan iluminación de tritio.
Electroluminiscenciaeditar
La electroluminiscencia se puede explotar en fuentes de luz. Tales fuentes normalmente emiten desde un área grande, lo que las hace adecuadas para retroiluminación de pantallas LCD. La excitación del fósforo se logra generalmente mediante la aplicación de un campo eléctrico de alta intensidad, generalmente con la frecuencia adecuada. Las fuentes de luz electroluminiscente de corriente tienden a degradarse con el uso, lo que resulta en una vida útil relativamente corta.
ZnS:Cu fue la primera formulación que mostró electroluminiscencia con éxito, probada en 1936 por Georges Destriau en los laboratorios Madame Marie Curie de París.
La electroluminiscencia en polvo o CA se encuentra en una variedad de aplicaciones de retroiluminación y luz nocturna. Varios grupos ofrecen ofertas de marca EL (por ejemplo, IndiGlo utilizado en algunos relojes Timex) o «Lighttape», otro nombre comercial de un material electroluminiscente, utilizado en tiras de luz electroluminiscentes. El programa espacial Apolo es a menudo acreditado como el primer uso significativo de EL para retroiluminación e iluminación.
Led blancoseditar
Los diodos emisores de luz blancos suelen ser LED InGaN azules con un revestimiento de un material adecuado. El YAG dopado con cerio(III) (YAG:Ce3+, o Y3Al5O12: Ce3+) se usa a menudo; absorbe la luz del LED azul y emite en un amplio rango de verdor a rojizo, con la mayor parte de su salida en amarillo. Esta emisión amarilla combinada con la emisión azul restante da la luz «blanca», que se puede ajustar a la temperatura de color como blanco cálido (amarillento) o frío (azulado). La emisión de amarillo pálido del Ce3+:El YAG se puede ajustar sustituyendo el cerio por otros elementos de tierras raras, como terbio y gadolinio, e incluso se puede ajustar aún más sustituyendo parte o la totalidad del aluminio del YAG por galio. Sin embargo, este proceso no es de fosforescencia. La luz amarilla se produce mediante un proceso conocido como centelleo, siendo la ausencia completa de un resplandor posterior una de las características del proceso.
Algunos sialones dopados con tierras raras son fotoluminiscentes y pueden servir como fósforos. El β-SiAlÓN dopado con europio(II) absorbe el espectro de luz ultravioleta y visible y emite una intensa emisión visible de banda ancha. Su luminancia y color no cambian significativamente con la temperatura, debido a la estructura cristalina estable a la temperatura. Tiene un gran potencial como fósforo de conversión descendente verde para ledes blancos; también existe una variante amarilla (α-SiAlON). Para los LED blancos, se utiliza un LED azul con un fósforo amarillo, o con un fósforo de SiAlÓN verde y amarillo y un fósforo rojo a base de CaAlSiN3 (CASN).
Los LED blancos también se pueden fabricar recubriendo los LED emisores de ultravioleta cercano(NUV) con una mezcla de fósforos emisores de rojo y azul a base de europio de alta eficiencia y sulfuro de zinc dopado con cobre y aluminio de emisión verde (ZnS:Cu,Al). Este es un método análogo a la forma en que funcionan las lámparas fluorescentes.
Algunos LED blancos más nuevos utilizan un emisor amarillo y azul en serie, para aproximarse al blanco; esta tecnología se utiliza en algunos teléfonos Motorola, como el Blackberry, así como en la iluminación LED y los emisores apilados de la versión original mediante el uso de GaN en SiC en InGaP, pero más tarde se descubrió que se fracturaba a corrientes de transmisión más altas.
Muchos led blancos utilizados en sistemas de iluminación general se pueden utilizar para la transferencia de datos, como, por ejemplo, en sistemas que modulan el LED para actuar como una baliza.
También es común que los led blancos usen fósforos que no sean Ce: YAG, o que usen dos o tres fósforos para lograr un CRI más alto, a menudo a costa de la eficiencia. Ejemplos de fósforos adicionales son R9, que produce un rojo saturado, nitruros que producen rojo, y aluminatos como el granate de aluminio lutecio que produce verde. Los fósforos de silicato son más brillantes pero se desvanecen más rápidamente, y se utilizan en retroiluminación LED LCD en dispositivos móviles. Los fósforos LED se pueden colocar directamente sobre el dado o convertirlos en una cúpula y colocarlos encima del LED: este enfoque se conoce como fósforo remoto. Algunos LED de colores, en lugar de usar un LED de color, usan un LED azul con un fósforo de color porque tal disposición es más eficiente que un LED de color. Los fósforos de oxinitruro también se pueden usar en leds. Los percursores utilizados para fabricar los fósforos pueden degradarse cuando se exponen al aire.
rayos Catódicos tubesEdit
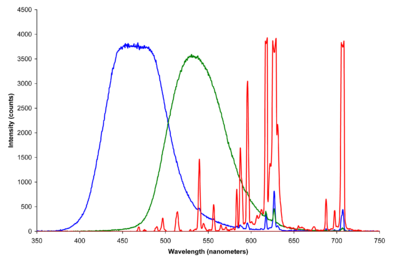
Los tubos de rayos catódicos producen patrones de luz generados por señales en un formato (típicamente) redondo o rectangular. Los CRT voluminosos se utilizaron en los televisores domésticos en blanco y negro («TV») que se hicieron populares en la década de 1950, así como en los televisores a color de primera generación basados en tubos y en la mayoría de los monitores de computadora anteriores. Los TRC también se han utilizado ampliamente en instrumentación científica y de ingeniería, como osciloscopios, generalmente con un solo color de fósforo, típicamente verde. Los fósforos para tales aplicaciones pueden tener un brillo posterior prolongado, para una mayor persistencia de la imagen.
Los fósforos pueden depositarse como película delgada o como partículas discretas, un polvo unido a la superficie. Las películas delgadas tienen mejor vida útil y mejor resolución, pero proporcionan una imagen menos brillante y menos eficiente que las en polvo. Esto es causado por múltiples reflejos internos en la película delgada, dispersando la luz emitida.
Blanco (en blanco y negro): La mezcla de sulfuro de zinc y cadmio y sulfuro de zinc plateado, el ZnS:Ag+(Zn,Cd) S: Ag es el fósforo P4 blanco utilizado en CRT de televisión en blanco y negro. Las mezclas de fósforos amarillos y azules son habituales. También se pueden encontrar mezclas de rojo, verde y azul, o un solo fósforo blanco.
Rojo: El sulfuro de óxido de itrio activado con europio se utiliza como fósforo rojo en los TRC de color. El desarrollo de la televisión en color tomó mucho tiempo debido a la búsqueda de un fósforo rojo. El primer fósforo de tierras raras emisor de rojo, YVO4:Eu3+, fue introducido por Levine y Palilla como color primario en la televisión en 1964. En forma de cristal único, se utilizó como un excelente polarizador y material láser.
Amarillo: Cuando se mezcla con sulfuro de cadmio, el sulfuro de cadmio de zinc (Zn, Cd) S: Ag resultante proporciona una fuerte luz amarilla.
Verde: Combinación de sulfuro de zinc con cobre, el fósforo P31 o ZnS:Cu, proporciona luz verde con un pico de 531 nm, con un brillo largo.Azul: Combinación de sulfuro de zinc con pocas ppm de plata, el ZnS: Ag, cuando es excitado por electrones, proporciona un fuerte brillo azul con un máximo de 450 nm, con un brillo posterior corto con una duración de 200 nanosegundos. Se conoce como fósforo P22B. Este material, sulfuro de zinc plateado, sigue siendo uno de los fósforos más eficientes en tubos de rayos catódicos. Se utiliza como fósforo azul en CRTs de color.
Los fósforos son generalmente conductores eléctricos pobres. Esto puede llevar a la deposición de carga residual en la pantalla, disminuyendo efectivamente la energía de los electrones impactantes debido a la repulsión electrostática (un efecto conocido como «adherencia»). Para eliminar esto, se deposita una fina capa de aluminio (aproximadamente 100 nm) sobre los fósforos, generalmente por evaporación al vacío, y se conecta a la capa conductora dentro del tubo. Esta capa también refleja la luz de fósforo en la dirección deseada, y protege el fósforo del bombardeo iónico resultante de un vacío imperfecto.
Para reducir la degradación de la imagen por reflexión de la luz ambiental, el contraste se puede aumentar mediante varios métodos. Además del enmascaramiento negro de las áreas no utilizadas de la pantalla, las partículas de fósforo en las pantallas a color están recubiertas con pigmentos de color a juego. Por ejemplo,los fósforos rojos están recubiertos con óxido férrico (reemplazando a los anteriores Cd(S, Se) debido a la toxicidad por cadmio), los fósforos azules pueden estar recubiertos con azul marino (CoO·nAl
2O
3) o azul ultramar (Na
8Al
6Si
6O
24S
2). Los fósforos verdes basados en ZnS: Cu no tienen que estar recubiertos debido a su propio color amarillento.
CRTS de televisión en blanco y negroeditar
Las pantallas de televisión en blanco y negro requieren un color de emisión cercano al blanco. Por lo general, se emplea una combinación de fósforos.
La combinación más común es ZnS: Ag+(Zn, Cd) S:Cu,Al (azul+amarillo). Otros son ZnS:Ag+(Zn,Cd)S:Ag (azul+amarillo), y ZnS:Ag+ZnS:Cu,Al+Y2O2S:Eu3+ (azul + verde + rojo – no contienen cadmio y tiene baja eficiencia). El tono de color se puede ajustar por las proporciones de los componentes.
Como las composiciones contienen granos discretos de diferentes fósforos, producen una imagen que puede no ser completamente lisa. Un solo fósforo emisor de blancos, (Zn,Cd)S:Ag,Au, Al supera este obstáculo. Debido a su baja eficiencia, se utiliza solo en pantallas muy pequeñas.
Las pantallas se cubren típicamente con fósforo usando un revestimiento de sedimentación, donde las partículas suspendidas en una solución se dejan sedimentar en la superficie.
CRTS de color de paleta reducida Edit
Para mostrar una paleta de colores limitada, hay algunas opciones.
En los tubos de penetración de haz, los fósforos de diferentes colores se superponen y se separan con material dieléctrico. El voltaje de aceleración se utiliza para determinar la energía de los electrones; los de menor energía se absorben en la capa superior del fósforo, mientras que algunos de los de mayor energía se disparan y se absorben en la capa inferior. Por lo tanto, se muestra el primer color o una mezcla del primer y segundo color. Con una pantalla con capa exterior roja y capa interior verde, la manipulación del voltaje de aceleración puede producir un continuo de colores desde el rojo hasta el naranja y el amarillo hasta el verde.
Otro método es usar una mezcla de dos fósforos con características diferentes. El brillo de uno depende linealmente del flujo de electrones, mientras que el brillo del otro se satura en flujos más altos: el fósforo no emite más luz, independientemente de cuántos electrones más lo impacten. Con un flujo de electrones bajo, ambos fósforos emiten juntos; en flujos más altos, prevalece la contribución luminosa del fósforo no saturante, cambiando el color combinado.
Tales pantallas pueden tener alta resolución, debido a la ausencia de estructuración bidimensional de los fósforos RGB CRT. Su paleta de colores es, sin embargo, muy limitada. Se utilizaron, por ejemplo, en algunas pantallas de radar militares más antiguas.
CRTS de televisión en coloreditar
Los fósforos en CRT de color necesitan un mayor contraste y resolución que los de blanco y negro. La densidad de energía del haz de electrones es aproximadamente 100 veces mayor que en los CRT en blanco y negro; el punto de electrones está enfocado a aproximadamente 0.2 mm de diámetro en lugar de aproximadamente 0,6 mm de diámetro de los TRC en blanco y negro. Por lo tanto, los efectos relacionados con la degradación por irradiación de electrones son más pronunciados.
Los CRT de color requieren tres fósforos diferentes, que emiten en rojo, verde y azul, con dibujos en la pantalla. Se utilizan tres pistolas de electrones separadas para la producción de color (excepto para pantallas que usan tecnología de tubo de índice de haz, que es rara).
La composición de los fósforos cambió con el tiempo, a medida que se desarrollaron mejores fósforos y que las preocupaciones ambientales llevaron a reducir el contenido de cadmio y luego abandonarlo por completo. El (Zn,Cd)S:Ag,Cl fue reemplazado por (Zn,Cd)S:Cu,Al con una relación cadmio/zinc más baja, y luego con ZnS:Cu,Al sin cadmio.
El fósforo azul se mantuvo generalmente sin cambios, un sulfuro de zinc dopado con plata. El fósforo verde utilizó inicialmente silicato de zinc dopado con manganeso, luego evolucionó a través de sulfuro de cadmio-zinc activado con plata, a una fórmula activada con cobre-aluminio de bajo cadmio, y luego a una versión libre de cadmio de la misma. El fósforo rojo vio la mayoría de los cambios; originalmente era fosfato de zinc activado por manganeso, luego un sulfuro de cadmio y zinc activado por plata, luego aparecieron los fósforos activados por europio(III); primero en una matriz de vanadato de itrio, luego en óxido de itrio y actualmente en oxisulfuro de itrio. La evolución de los fósforos, por tanto, era (ordenado por B-G-R):
- ZnS:Ag – Zn2SiO4:Mn – Zn3(PO4)2:Mn
- ZnS:Ag – (Zn,Cd)S:Ag – (Zn,Cd)S:Ag
- ZnS:Ag – (Zn,Cd)S:Ag – YVO4:Eu3+ (1964–?)
- ZnS:Ag – (Zn,Cd)S:Cu,Al – Y2O2S:Eu3+ o Y2O3:Eu3+
- ZnS:Ag – ZnS:Cu,Al, o ZnS:Au,Cu,Al – Y2O2S:Eu3 +
Televisores de proyectacióneditar
Para televisores de proyección, donde la densidad de potencia del haz puede ser dos órdenes de magnitud mayor que en los CRT convencionales, se deben usar algunos fósforos diferentes.
Para el color azul,se emplea ZnS:Ag, Cl. Sin embargo, se satura. (La,Gd)OBr:Ce,Tb3+ se puede utilizar como una alternativa que es más lineal a altas densidades de energía.
Para verde, un Gd2O2Tb3 + activado por terbio; su pureza de color y brillo a bajas densidades de excitación es peor que la alternativa de sulfuro de zinc, pero se comporta de forma lineal a altas densidades de energía de excitación, mientras que el sulfuro de zinc se satura. Sin embargo, también se satura, por lo que Y3Al5O12:Tb3+ o Y2SiO5:Tb3+ pueden sustituirse. LaOBr: Tb3 + es brillante pero sensible al agua, propenso a la degradación, y la morfología en forma de placa de sus cristales dificulta su uso; estos problemas se resuelven ahora, por lo que está ganando uso debido a su mayor linealidad.
Y2O2S: Eu3 + se utiliza para la emisión de rojo.