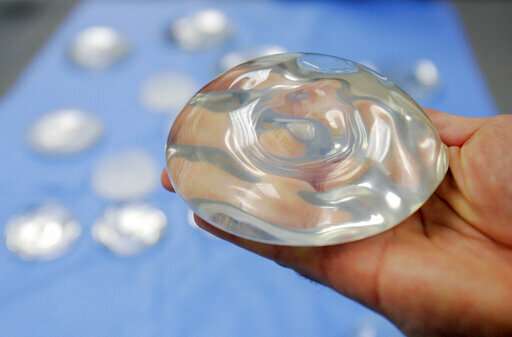
amerikanske medicinske myndigheder gennemgår sikkerheden ved brystimplantater, der bruges af millioner af amerikanske kvinder, den seneste gennemgang i en løbende debat om deres potentielle sundhedseffekter.
et ekspertpanel samlet af Food and Drug Administration åbnede et to-dages møde mandag for at diskutere de seneste beviser om risikoen for sygdom og komplikationer med enhederne, som er blevet solgt siden midten af 1960 ‘ erne.
brystforstørrelse er den mest populære form for kosmetisk kirurgi i USA, hvor omkring 300.000 kvinder gennemgår proceduren hvert år. Yderligere 100.000 kvinder modtager implantater til brystrekonstruktion efter kræftoperation.
panelet vil høre fra forskere, plastikkirurger, patienter og producenter og derefter anbefale de næste trin. FDA er ikke forpligtet til at følge gruppens råd, selvom det ofte gør det.
for nu foreslår FDA ikke nye begrænsninger eller advarsler. Agenturets mangeårige position er, at implantater i det væsentlige er sikre, så længe kvinder forstår, at de har komplikationer, herunder ardannelse, smerte, hævelse og implantatbrud.FDA og andre regulatorer rundt om i verden har kæmpet med, hvordan man håndterer et nyligt bekræftet link til en sjælden kræft og tusindvis af ubekræftede påstande om, at implantaterne kan bidrage til andre kroniske lidelser.
“det er vigtigt, at vi prøver at forstå brystimplantatsygdom,” sagde Stephanie Manson brun, en direktør med implantatproducent Allergan. Men hun tilføjede, at der ikke er nogen medicinsk anerkendt definition af problemet eller standardiseret måde at diagnosticere det på.
de fleste bekræftede tilfælde af kræft, kendt som brystimplantatassocieret anaplastisk storcellelymfom, har involveret en bestemt implantatstil med en struktureret overflade, designet til at reducere arvæv og glidning.sidste år afviste EU-tilsynsmyndighederne at forny godkendelsen af teksturerede implantater, der blev solgt af Allergan, med henvisning til links til kræften. Det fik virksomheden til at trække produkterne fra Det Europæiske marked.men FDA har sagt, at det er uklart, om kræften udelukkende er knyttet til teksturerede implantater eller også involverer glatte implantater, der udgør det meste af det amerikanske marked. Manglende data om det samlede antal implantater i brug gør det næsten umuligt at bestemme, hvor ofte kræften opstår, bemærker agenturet.
sygdommen er ikke brystkræft, men en form for kræft, der angriber immunsystemet og normalt dannes i arvævet omkring implantater. Det vokser langsomt og kan normalt behandles med succes ved at fjerne implantaterne.
tusindvis af kvinder har også skylden deres implantater for en lang række kroniske lidelser, herunder reumatoid arthritis, kronisk træthed og muskelsmerter. Panelet vil høre fra snesevis af kvinder; mange af dem har opfordret agenturet til at placere nye advarsler og begrænsninger på implantaterne.
” Ignorer os ikke. Vi er virkelige, ” sagde Holly Davis fra Charleston, South Carolina.Davis, 60, sagde, at hun oplevede kroniske smerter, hårtab, udslæt og hukommelsestab efter at have modtaget silikone gelfyldte implantater efter en dobbelt mastektomi i 2002. Davis sagde, at hun lærte, at hendes implantater var brudt, da de blev fjernet i 2017; hendes symptomer er siden løst.hun og andre patienter ønsker, at FDA skal kræve, at producenterne giver standardiserede oplysninger om risikooplysning til alle kvinder, der overvejer implantater.”vi er nødt til at vide, hvad vi tilmelder os—det kan ikke være en overraskelse nede ad vejen,” sagde Davis.
i USA vælger de fleste kvinder silikoneimplantater, der betragtes som mere naturlige end saltvandsimplantater. Begge typer har en silikone ydre skal.paneldeltagerne hørte også fra forskere, der teoretiserer, delvis baseret på dyreforsøg, at silikone, der lækker fra implantater, kan udløse eller forværre immunsystemforstyrrelser hos visse patienter.i 1992 trak FDA midlertidigt silikongelimplantater fra markedet på grund af frygt for, at de kan forårsage brystkræft, lupus og andre lidelser. Men da undersøgelser syntes at udelukke det meste af sygdomsproblemet, returnerede regulatorer dem til markedet i 2006.
men kritikere af denne forskning bemærkede sine mangler på mandagens møde.”undersøgelserne på det tidspunkt var ikke særlig gode og havde ikke den statistiske magt til at bestemme sjældne sygdomme,” sagde Diana Usuckerman, præsident for nonprofit, National Center for Health Research, der offentliggjorde en analyse af mere end 20 brystimplantatundersøgelser sidste år. Gruppen konkluderede, at stort set alle var for små eller for korte eller ikke fokuserede på patienter, der havde deres implantater længe nok til at udvikle problemer.FDA siger på sin hjemmeside, at der ikke er nogen” tilsyneladende sammenhæng ” mellem brystimplantater og kroniske, svækkende sygdomme, såsom bindevævssygdom.
men tidligere i denne måned syntes FDA at signalere et skift i sin tænkning.agenturet sagde, at det ville begynde at undersøge, om visse materialer, der anvendes i brystimplantater, metal hofter og andre enheder, kan udløse sundhedsmæssige problemer hos patienter.”vi mener, at de nuværende beviser, selvom de er begrænsede, antyder, at nogle individer kan være disponeret for at udvikle en immuninflammatorisk reaktion, når de udsættes for udvalgte materialer,” sagde agenturet i en erklæring.
Udforsk yderligere
FDA tager op årtier lang debat om brystimplantatsikkerhed
kar 2019 Associated Press. Alle rettigheder forbeholdes.