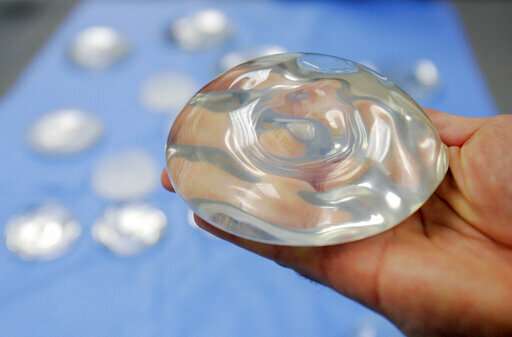
az amerikai egészségügyi hatóságok felülvizsgálják az amerikai nők milliói által használt mellimplantátumok biztonságosságát, a legújabb felülvizsgálat egy folyamatban lévő vitában a lehetséges egészségügyi hatásokról.
a Food and Drug Administration által összeállított szakértői testület kétnapos ülést nyitott hétfőn, hogy megvitassák a legújabb bizonyítékokat a betegségek és szövődmények kockázatairól az eszközökkel, amelyeket az 1960-as évek közepe óta értékesítettek.
a mellnagyobbítás a kozmetikai sebészet legnépszerűbb formája az Egyesült Államokban, évente nagyjából 300 000 nő vesz részt az eljárásban. További 100 000 nő kap implantátumot a mell rekonstrukciójára a rákműtét után.
a testület meghallgatja a kutatókat, a plasztikai sebészeket, a betegeket és a gyártókat, majd javasolja a következő lépéseket. Az FDA-nak nem kell követnie a csoport tanácsát, bár gyakran megteszi.
jelenleg az FDA nem javasol új korlátozásokat vagy figyelmeztetéseket. Az ügynökség hosszú távú álláspontja az, hogy az implantátumok lényegében biztonságosak, mindaddig, amíg a nők megértik, hogy komplikációik vannak, beleértve a hegesedést, fájdalmat, duzzanatot és az implantátum repedését.
az FDA és más szabályozók szerte a világon küzdenek azzal, hogyan lehet kezelni egy nemrégiben megerősített kapcsolatot egy ritka rákkal és több ezer meg nem erősített állítással, hogy az implantátumok hozzájárulhatnak más krónikus betegségekhez.
“elengedhetetlen, hogy megpróbáljuk megérteni a mellimplantátum betegségét” – mondta Stephanie Manson Brown, az Allergan implantátumgyártó ügyvezető igazgatója. De hozzátette, hogy nincs orvosilag elismert meghatározása a problémának vagy szabványosított módja annak diagnosztizálására.
a legtöbb megerősített rákos eset, az úgynevezett emlő implantátummal társult anaplasztikus nagysejtes limfóma, egy bizonyos stílusú, texturált felületű implantátumot érintett, amelynek célja a hegszövet és a csúszás csökkentése.
tavaly az Európai Unió szabályozói elutasították az Allergan által értékesített texturált implantátumok jóváhagyásának megújítását, hivatkozva a rákra. Ez arra késztette a vállalatot, hogy kivonja a termékeket az európai piacról.
de az FDA azt mondta, hogy nem világos, hogy a rák kizárólag a texturált implantátumokhoz kapcsolódik-e, vagy sima implantátumokkal is jár, amelyek az amerikai piac nagy részét alkotják. Az alkalmazott implantátumok Teljes számára vonatkozó adatok hiánya szinte lehetetlenné teszi annak meghatározását, hogy a rák milyen gyakran fordul elő-jegyzi meg az ügynökség.
a betegség nem mellrák, hanem a rák egy olyan formája, amely megtámadja az immunrendszert, és általában az implantátumokat körülvevő hegszövetben alakul ki. Lassan növekszik, és általában sikeresen kezelhető az implantátumok eltávolításával.
nők ezrei hibáztatták implantátumaikat számos krónikus betegségért, beleértve a rheumatoid arthritist, a krónikus fáradtságot és az izomfájdalmat. A testület több tucat nőtől fog hallani; sokan felszólították az Ügynökséget, hogy tegyen új figyelmeztetéseket és korlátozásokat az implantátumokra.
” ne hagyj figyelmen kívül minket. Valódiak vagyunk ” – mondta Holly Davis, a dél-karolinai Charlestonból.
a 60 éves Davis azt mondta, hogy krónikus fájdalmat, hajhullást, kiütéseket és memóriavesztést tapasztalt, miután 2002-ben kettős mastectomia után szilikon géllel töltött implantátumokat kapott. Davis elmondta, hogy megtudta, hogy az implantátumai megrepedtek, amikor 2017-ben eltávolították őket; tünetei azóta megszűntek.
ő és más betegek azt akarják, hogy az FDA megkövetelje a gyártóktól, hogy szabványosított kockázati nyilvánosságra hozatali információkat adjanak minden implantátumot fontolgató nőnek.
“tudnunk kell, hogy mire jelentkezünk—ez nem lehet meglepetés az úton” – mondta Davis.
az Egyesült Államokban a legtöbb nő szilikon implantátumokat választ, amelyeket természetesebbnek tartanak, mint a sós implantátumokat. Mindkét típusnak szilikon külső héja van.
a panelisták olyan kutatóktól is hallottak, akik részben állatkísérletek alapján feltételezik, hogy az implantátumokból szivárgó szilikon bizonyos betegeknél kiválthatja vagy súlyosbíthatja az immunrendszer rendellenességeit.
1992-ben az FDA ideiglenesen kivonta a szilikon gél implantátumokat a piacról, mert attól tartanak, hogy mellrákot, lupust és más rendellenességeket okozhatnak. De amikor a tanulmányok úgy tűnt, hogy kizárják a betegség legnagyobb részét, a szabályozók 2006-ban visszaküldték őket a piacra.
de a kutatás kritikusai a hétfői ülésen észrevették hiányosságait.
“az akkori tanulmányok nem voltak túl jók, és nem rendelkeztek statisztikai hatalommal a ritka betegségek meghatározására” – mondta Diana Zuckerman, az Országos Egészségügyi Kutatóközpont nonprofit szervezetének elnöke, amely tavaly több mint 20 mellimplantátum-vizsgálat elemzését tette közzé. A csoport arra a következtetésre jutott, hogy gyakorlatilag mindegyik túl kicsi vagy túl rövid volt, vagy nem azokra a betegekre összpontosítottak, akiknek implantátumuk elég hosszú volt ahhoz, hogy problémákat okozzanak.
az FDA honlapján azt mondja, hogy nincs “nyilvánvaló összefüggés” a mellimplantátumok és a krónikus, legyengítő betegségek, például a kötőszöveti betegségek között.
azonban a hónap elején az FDA úgy tűnt, hogy jelzi a gondolkodás változását.
Az ügynökség azt mondta, hogy elkezdi tanulmányozni, hogy a mellimplantátumokban, a fém csípőkben és más eszközökben használt bizonyos anyagok kiválthatják-e a betegek egészségügyi problémáit.”úgy gondoljuk, hogy a jelenlegi bizonyítékok, bár korlátozottak, arra utalnak, hogy egyes egyének hajlamosak lehetnek immungyulladásos reakció kialakulására, ha bizonyos anyagoknak vannak kitéve” – mondta az Ügynökség egy nyilatkozatában.
fedezze fel tovább
az FDA évtizedes vitát folytat a mellimplantátum biztonságáról
2019 az Associated Press. Minden jog fenntartva.