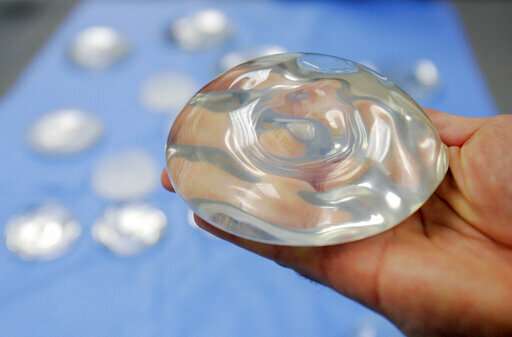
米国の医療当局は、何百万人ものアメリカの女性が使用する乳房インプラントの安全性を再検討しています。
食品医薬品局によって組み立てられた専門家パネルは、1960年代半ばから販売されているデバイスと病気や合併症のリスクについての最新の証拠を議論するために月曜日に二日間の会議を開きました。
豊胸は、毎年約300,000人の女性が手術を受けている米国で最も人気のある形です。 別の100,000人の女性は癌の外科の後で胸の再建のためのインプラントを受け取ります。
パネルは、研究者、形成外科医、患者やメーカーから聞いて、次のステップをお勧めします。 FDAは、グループの助言に従うことを要求されていませんが、しばしばそうです。今のところ、FDAは新たな制限や警告を提案していません。
今のところ、FDAは新しい制限や警告を提案していません。 代理店の長年の立場は、女性が瘢痕、痛み、腫れ、インプラントの破裂などの合併症があることを理解している限り、インプラントは本質的に安全である
FDAおよび世界中の他の規制当局は、最近確認されたまれな癌へのリンクと、インプラントが他の慢性疾患に寄与する可能性があるという未確認の主張の何千ものを管理する方法に取り組んできました。
“乳房インプラントの病気を理解しようとすることが不可欠です”と、インプラントメーカー AllerganのエグゼクティブであるStephanie Manson Brown氏は述べています。 しかし、彼女は、問題の医学的に認識された定義やそれを診断するための標準化された方法はないと付け加えた。
乳房インプラント関連未分化大細胞リンパ腫として知られている癌のほとんどの確認された症例は、瘢痕組織および滑りを減少させるように設
昨年、欧州連合の規制当局は、がんへのリンクを引用して、Allerganが販売しているテクスチャインプラントの承認を更新することを拒否しました。 これにより、同社は欧州市場から製品を引き抜くことができました。
しかし、FDAは、癌が質感のあるインプラントにのみ関連しているのか、米国市場の大部分を占める滑らかなインプラントを含むのかは不明であると述べている。 使用中のインプラントの総数に関するデータの欠如は、癌がどのくらいの頻度で発生するかを決定することをほとんど不可能にする、と同機関は指摘この疾患は乳癌ではなく、免疫系を攻撃し、通常はインプラント周囲の瘢痕組織に形成される癌の一形態である。
この疾患は乳癌ではない。
それはゆっくり育ち、通常インプラントを取除くことによって首尾よく扱うことができます。
何千人もの女性が、関節リウマチ、慢性疲労、筋肉痛などの慢性的な病気のためにインプラントを非難しています。 パネルは何十人もの女性から聞きます; 彼らの多くは、インプラントに新しい警告と制限を置くために代理店に呼びかけています。”私たちを無視しないでください。
“私たちを無視しないでください。 私たちは本物です”とサウスカロライナ州チャールストンのホリー-デイビスは言った。
デイビス、60は、彼女が2002年に二重乳房切除後のシリコーンゲル充填インプラントを受けた後、慢性的な痛み、脱毛、発疹や記憶喪失を経験したと述べました。 デイビスは、2017で除去されたときにインプラントが破裂したことを学んだと言いました。
彼女と他の患者は、FDAは、インプラントを検討しているすべての女性に標準化されたリスク開示情報を与えるためにメーカーを要求したいです。
“私たちはサインアップしているものを知る必要があります—それは道の下で驚きではありません”とDavisは言いました。
米国では、ほとんどの女性は生理食塩水のインプラントよりも自然に見えると考えられているシリコーンインプラントを選択します。 両方のタイプにシリコーンの外貝があります。
パネリストはまた、インプラントから漏れたシリコーンが特定の患者の免疫系障害を誘発または悪化させる可能性があることを、動物研究に部分的に基づいて理論化している研究者から聞いた。
1992年に、FDAは一時的にあるため、彼らは乳癌、狼瘡および他の障害を引き起こす可能性が懸念の市場からシリコーンゲルインプラントを引っ張った。 しかし、研究が病気の懸念の大部分を排除しているように見えたとき、規制当局は2006年にそれらを市場に戻しました。しかし、その研究の批評家は月曜日の会議でその欠点を指摘した。
“当時の研究はあまり良くなかったし、希少疾患を決定するための統計的な力を持っていなかった、”ダイアナZuckerman、非営利、国立健康研究センターの社長は、昨年20以上の乳房インプラント研究の分析を発表したと述べた。 グループは、事実上すべてが小さすぎたり短すぎたり、問題を発症するのに十分な長さのインプラントを持っていた患者に焦点を当てていないと結FDAは、豊胸手術と結合組織疾患などの慢性衰弱性疾患との間に「明らかな関連性」はないと同社のウェブサイトで述べています。
しかし、今月初めにFDAは、その考え方の変化を示すように見えました。
代理店は、乳房インプラント、金属腰および他のデバイスに使用される特定の材料が患者の健康上の問題を引き起こす可能性があるかどうか
“我々は、現在の証拠は限られているが、一部の個人が選択された材料にさらされたときに免疫炎症反応を発症する素因がある可能性があることを示唆していると考えている”と同機関は声明で述べている。 FDAは、乳房インプラントの安全性に関する数十年にわたる議論を取り上げています。
©2019The Ap通信。 すべての権利を保有します。 引用:米国の専門家は、新しい懸念の中で乳房インプラントの安全性を重み付け(2019、March25)から25March2021を取得しましたhttps://medicalxpress.com/news/2019-03-experts-revisit-breast-implant-safety.html