- Alcool isopropylique Propriétés chimiques, utilisations, production
- description
- Processus de production
- Utilisations
- Toxicité
- Utilisation limitée
- Propriétés chimiques
- Occurrence
- Utilisations
- Utilisations
- Utilise
- Utilisations
- Utilise
- Définition
- Méthodes de production
- Méthodes de production
- Valeurs de seuil d’arôme
- Description générale
- Air &Réactions à l’eau
- Profil de réactivité
- Danger
- Danger pour la santé
- Risque d’incendie
- Réactivité chimique
- Applications pharmaceutiques
- Sécurité
- Synthèse chimique
- Cancérogénicité
- stockage
- Méthodes de purification
- Incompatibilités
- Précautions
- Statut réglementaire
Alcool isopropylique Propriétés chimiques, utilisations, production
description
L’isopropanol est également connu sous le nom d’alcool isopropylique. C’est l’alcool secondaire le plus simple et l’un des isomères du n-propanol. C’est une sorte de liquide inflammable incolore avec une forte odeur similaire à l’odeur du mélange d’éthanol et d’acétone. Il est soluble dans l’eau, l’alcool, l’éther, le benzène, le chloroforme et la plupart des solvants organiques et est miscible avec l’eau, l’alcool, l’éther et peut former un azéotrope avec l’eau. Densité (densité): 0.7863g / cm3, point de fusion: -88,5 ℃, point d’ébullition: 82,5 ℃, point d’éclair: 11,7 ℃, point d’allumage: 460 ℃, indice de réfraction: 1,3772. Sa vapeur peut provoquer une légère irritation des yeux, du nez et de la gorge; elle peut être absorbée par la peau. Sa vapeur peut former un mélange explosif avec l’air. Sa limite d’explosion est de 2,0% à 12% (en volume). Il appartient à une matière dangereuse explosive modérée et à une substance inflammable et peu toxique. La toxicité de ses vapeurs est deux fois plus élevée que celle de l’éthanol tandis que l’administration orale provoque la toxicité inverse.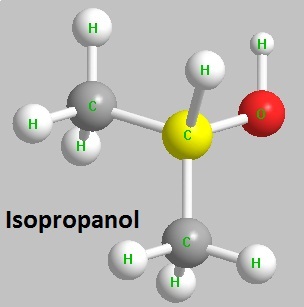
La figure 1 est la formule structurelle de l’isopropanol.
Dans de nombreux cas, l’isopropanol peut remplacer l’éthanol comme solvant et constitue un bon solvant et des matières premières chimiques qui peuvent être appliquées non seulement à la peinture, aux produits pharmaceutiques, aux pesticides, aux cosmétiques et à d’autres industries, mais également à la production d’acétone, d’ester isopropylique, d’isopropylamine (la matière première pour la production d’atrazine), d’éther di-isopropylique, d’acétate d’isopropyle et de cristal de thymol, etc. C’était le premier produit fabriqué à partir de la matière première pétrolière dans l’histoire du développement de la pétrochimie.
Processus de production
En 1855, le Français M. Berthelot a signalé pour la première fois la production d’isopropanol par la réaction d’hydratation entre le propylène et l’acide sulfurique, appelée hydratation indirecte. En 1919, les Américains C. Ellis avaient mené un développement industriel à ce sujet. À la fin de 1920, l’American Standard Oil Company du New Jersey a adopté l’approche de la loi Ellis et a établi l’équipement de production pour la mise en production formelle. En 1951, la société britannique Imperial Chemical Industries a commencé à produire de l’isopropanol avec la méthode d’hydratation directe à partir de propylène. Depuis lors, de nombreux pays ont utilisé cette méthode et apporté des améliorations connexes.
Réaction d’hydratation indirecte: le propylène est d’abord mis à réagir avec de l’acide sulfurique pour obtenir de l’hydrogénosulfate d’isopropyle, qui génère de l’isopropanol après hydrolyse, et la réaction de la formule:
CH3CH = CH2 + H2SO4 → (CH3) 2CHOSO3H
(CH3) 2CHOSO3H + H2O─ → (CH3) 2CHOH + H2SO4
la concentration de l’acide sulfurique appliqué est généralement supérieure à 60% (en masse), et la réaction est conduite à 2 ~ 2,8MPa et 60 ~ 65 ° C; La réaction d’hydrolyse se produit à une légère augmentation de la pression et à moins de 30 ° C.
Hydratation directe: le propylène a directement une réaction d’hydratation avec de l’eau en présence d’un catalyseur lors du chauffage et de l’augmentation de la pression pour générer de l’isopropanol avec une sélectivité de 96%. La réaction est : CH3CH = CH2 + H2O → (CH3) 2CHOH; le catalyseur utilisé comprend un composé de tungstène, un phosphate et une résine échangeuse d’ions; le catalyseur couramment utilisé est un catalyseur d’acide phosphorique avec support (voir catalyseur d’acide solide) avec des conditions de 2 ~ 6 MPa, 240 ~ 260 ° C. Par rapport à la méthode indirecte, cette méthode n’a pas de problème concernant la corrosion de l’acide sulfurique et la concentration d’acide dilué et, par conséquent, elle domine dans la production industrielle.
Les informations ci-dessus sont éditées par le Chemicalbook de Dai Xiongfeng.
Utilisations
L’alcool isopropylique est un produit chimique et une matière première importants. Il est principalement appliqué à divers domaines, y compris les produits pharmaceutiques, les cosmétiques, les plastiques, les parfums, la peinture et est également utilisé comme agent déshydratant et agent de nettoyage dans l’industrie électronique. Il peut également être utilisé comme réactif pour la détermination du baryum, du calcium, du magnésium, du nickel, du potassium, du sodium et du strontium. Il peut également être utilisé comme matériau de référence pour l’analyse chromatographique.
Dans l’industrie manufacturière de la carte de circuit imprimé, il est utilisé comme agent de nettoyage et pour la production de trous de PCB pour la conductivité. Beaucoup de gens trouvent qu’il peut non seulement nettoyer la carte mère avec d’excellentes performances, mais aussi obtenir les meilleurs résultats. En outre, il est utilisé pour d’autres appareils électroniques, y compris le nettoyage de la cartouche de disque, des lecteurs de disquettes, de la bande magnétique et de la pointe laser du pilote de disque du lecteur de CD ou de DVD.
L’alcool isopropylique peut également être utilisé comme solvant d’huile et de gel ainsi que pour la fabrication de concentré d’alimentation en farine de poisson. L’isopropanol de mauvaise qualité peut également être utilisé dans les carburants automobiles. En tant que matière première de production d’acétone, la quantité d’utilisation d’isopropanol diminue. Plusieurs composés sont synthétisés à partir de l’isopropanol, tels que l’ester d’isopropyle, la méthyl isobutylcétone, la di-isopropylamine, l’éther di-isopropylique, l’acétate d’isopropyle, le thymol et de nombreux types d’esters. Nous pouvons fournir de l’isopropanol de qualité différente en fonction de l’utilisation finale. La qualité conventionnelle de l’isopropanol anhydre est supérieure à 99%, tandis que la teneur en isopropanol de qualité spéciale est supérieure à 99,8% (pour les arômes et les médicaments).
Toxicité
La valeur de la DJA n’est pas spécifiée (FAO/OMS, 2001).
DL5050 : 45rag/kg (rat, par voie orale).
Utilisation limitée
FEMA (mg/kg): boissons gazeuses: 25; bonbons: 10 à 75; cuit au four: 75.
Propriétés chimiques
L’alcool isopropylique est un liquide clair, incolore, mobile, volatil et inflammable avec une odeur spiritueuse caractéristique ressemblant à celle d’un mélange d’éthanol et d’acétone; il a un goût légèrement amer taste.It est miscible avec l’eau, l’éther éthylique et l’alcool éthylique. L’alcool isopropylique est incompatible avec les oxydants forts, l’acétaldéhyde, le chlore, l’oxyde d’éthylène, les acides et les isocyanates.
Occurrence
Signalée dans les arômes de pomme et de cognac (estérifiés). On le trouve également dans la pomme, la banane, le pamplemousse et le citron vert, le melon, la papaye, la poire, l’oignon, les pois, le rutabaga, la tomate, le pain de blé, les fromages, le lait, l’œuf à la coque, le bœuf cuit, le porc et le mouton, la bière hopoil, le rhum, le cacao, le café, le whisky écossais, les vins de raisin, l’arachide, la noix de pécan, le soja, le miel, les haricots, l’eau-de-vie de prune, la noix, le crabe, la palourde, la figue de barbarie et la sauge sclarée.
Utilisations
L’alcool isopropylique est utilisé dans la production d’acétone, d’halogénures d’isopropyle, de glycérine et d’isopropoxyde d’aluminium; largement utilisé comme solvant industriel pour les peintures, les vernis et les insecticides; comme antiseptique (alcool à friction); et en synthèse organique pour introduire le groupe isopropyle ou isopropoxy dans la molécule. Étant un solvant de laboratoire commun comme le méthanol, les risques d’exposition sont toujours élevés; cependant, sa toxicité est relativement faible.
Utilisations
l’alcool isopropylique est un vecteur, un antibactérien et un solvant pour les lotions de soins de la peau. L’alcool isopropylique est fabriqué à partir de propylène, un dérivé du pétrole.
Utilise
Par rapport à l’éthanol, 50% de moins est nécessaire pour la précipitation des acides nucléiques, minimisant ainsi le volume total à centrifuger pour la récupération de l’ADN ou de l’ARN.
Utilisations
Convient pour la CLHP, la spectrophotométrie, les tests environnementaux
Utilise
Dans les compositions antigel; comme solvant pour les gommes, la gomme laque, les huiles essentielles; dans l’extraction des alcaloïdes; dans les huiles à séchage rapide; dans les encres à séchage rapide; dans l’alcool éthylique dénaturant; dans les frottements corporels; lotions pour les mains, lotions après-rasage et cosmétiques similaires. Solvant pour la créosote, les résines, les gommes; dans la fabrication d’acétone, de glycérol, d’acétate d’isopropyle. Aide pharmaceutique (solvant).
Définition
ChEBI: Un alcool secondaire qui est le propane dans lequel l’un des hydrogènes attachés au carbone central est substitué par un groupe hydroxy.
Méthodes de production
L’alcool isopropylique peut être préparé à partir de propylène; par réduction catalytique de l’acétone, ou par fermentation de certains carbohydrates.
Méthodes de production
Deux méthodes de production de base sont utilisées dans le commerce: (1) l’absorption du propylène dans l’acide sulfurique pour former de l’alkylhydrogénosulfate, suivie de l’hydrolyse de l’ester; et (2) par hydratation directe avec de l’eau, à l’aide d’un catalyseur. Un inconvénient inhérent au premier processus est la nécessité de manipuler de l’acide sulfurique. De plus, le premier procédé donne un peu plus de 70% d’isopropanol par rapport au second procédé, dans lequel le propylène liquide est utilisé comme charge. Tous les processus d’hydratation directe peuvent être représentés par: C3H6 + H2O??→ C3H7OH + chaleur.
Valeurs de seuil d’arôme
Détection: 40 à 601 ppm
Description générale
Liquide volatil et incolore avec une forte odeur de moisi comme l’alcool à friction. Point d’éclair de 53 ° F. Les vapeurs sont plus lourdes que l’air et légèrement irritantes pour les yeux, le nez et la gorge. Densité d’environ 6,5 lb/ gal. Utilisé dans la fabrication de cosmétiques, de préparations pour la peau et les cheveux, de produits pharmaceutiques, de parfums, de formulations de laque, de solutions de teinture, d’antigels, de savons, de nettoyants pour vitres. Vendu en solution aqueuse à 70% comme alcool à friction.
Air &Réactions à l’eau
Hautement inflammables. Soluble dans l’eau.
Profil de réactivité
L’isopropanol réagit avec l’air ou l’oxygène pour former des peroxydes dangereusement instables. Le contact avec la 2-butanone augmente le taux de formation de peroxyde. An explosive reaction occurs when Isopropanol is heated with (aluminum isopropoxide + crotonaldehyde). Forms explosive mixtures with trinitromethane and hydrogen peroxide. Reacts with barium perchlorate to form a highly explosive compound. Ignites on contact with dioxygenyl tetrafluoroborate, chromium trioxide and potassium-tert-butoxide. Vigorous reactions occur with (hydrogen + palladium), nitroform, oleum, COCl2, aluminum triisopropoxide and oxidizing agents. Reacts explosively with phosgene in the presence of iron salts. Incompatible with acids, acid anhydrides, halogens and aluminum . L’isopropanol peut réagir avec le PCl3, formant un gaz HCl toxique. (Logsdon, John E., Richard A. Loke., alcool sopropylique. Encyclopédie Kirk-Othmer de la technologie chimique. John Wiley &Fils, Inc. 1996.).
Danger
Inflammable, risque d’incendie dangereux, explosivelimits dans l’air 2-12%. Toxique par ingestion et inhalation. Irritant pour les yeux et les voies respiratoires supérieures, système nerveux central. Cancérogène douteux.
Danger pour la santé
L’exposition à l’alcool isopropylique provoque une irritation des yeux et des muqueuses. L’exposition à l’alcool isopropylique pendant 3 à 5 min (400 ppm) a provoqué une légère irritation des yeux, du nez et de la gorge, et à 800 ppm, ces symptômes sont devenus sévères. L’ingestion ou une dose orale de 25 mL dans 100 mL d’eau a produit une hypotension, une flétrissure faciale, une bradycardie et des étourdissements. L’ingestion en grande quantité a provoqué une trachéobronchite hémorragique étendue, une bronchopneumonie et un œdème pulmonaire hémorragique. Un contact cutané prolongé avec de l’alcool isopropylique a provoqué un eczéma et une sensibilité. L’absorption cutanée retardée est attribuée à un certain nombre d’empoisonnements pédiatriques survenus à la suite d’un bain d’éponge répété ou prolongé avec de l’alcool isopropylique pour réduire la fièvre. Dans plusieurs cas, les symptômes comprenaient une détresse respiratoire, une stupeur et un coma. Les animaux de laboratoire exposés à l’alcool isopropylique développent un empoisonnement avec des symptômes de paralysie de la jambe arrière, d’instabilité, de manque de coordination musculaire, de dépression respiratoire et de stupeur. L’alcool isopropylique est un puissant dépresseur du SNC et, à fortes doses, provoque une dépression cardiovasculaire.
Risque d’incendie
HAUTEMENT INFLAMMABLE: Sera facilement enflammé par la chaleur, les étincelles ou les flammes. Les vapeurs peuvent former des mélanges explosifs avec l’air. Les vapeurs peuvent se rendre à la source d’inflammation et revenir en arrière. La plupart des vapeurs sont plus lourdes que l’air. Ils se répandront le long du sol et s’accumuleront dans des zones basses ou confinées (égouts, sous-sols, réservoirs). Risque d’explosion de vapeur à l’intérieur, à l’extérieur ou dans les égouts. Le ruissellement vers les égouts peut créer un risque d’incendie ou d’explosion. Les contenants peuvent exploser lorsqu’ils sont chauffés. De nombreux liquides sont plus légers que l’eau.
Réactivité chimique
Réactivité avec l’eau Pas de réaction; Réactivité avec les Matériaux communs : Pas de réactions; Stabilité Pendant le transport: Stable; Agents Neutralisants pour les Acides et les Caustiques: Non pertinents; Polymérisation: Non pertinente; Inhibiteur de la polymérisation: Non pertinent.
Applications pharmaceutiques
L’alcool isopropylique (propan-2-ol) est utilisé dans les formules cosmétiques et pharmaceutiques, principalement comme solvant dans les formulations topiques.(Il n’est pas recommandé pour une utilisation orale en raison de sa toxicité.
Bien qu’il soit utilisé dans les lotions, les propriétés dégraissantes marquées de l’alcool isopropylique peuvent limiter son utilité dans les préparations utilisées à plusieurs reprises. L’alcool isopropylique est également utilisé comme solvant à la fois pour le revêtement de film de comprimés et pour la granulation de comprimés, où l’isopropylalcool est ensuite éliminé par évaporation. Il a également été montré pour augmenter de manière significative la perméabilité cutanée du nimésulide à partir du carbomère 934.
L’alcool isopropylique a une certaine activité antimicrobienne et une solution aqueuse à 70% v / v est utilisée comme désinfectant topique.Sur le plan thérapeutique, l’alcool isopropylique a été étudié pour le traitement des nausées ou des vomissements postopératoires.
Sécurité
L’alcool isopropylique est largement utilisé dans les cosmétiques et les formulations pharmaceutiques topiques. Il est facilement absorbé par le tractus gastro-intestinal et peut être lentement absorbé par intactskin. Une exposition directe prolongée d’alcool isopropylique à la peau peutrésultat de déficits cardiaques et neurologiques. Chez les nouveau-nés, il a été rapporté que l’isopropylalcool causait des brûlures chimiques après une application topique.
L’alcool isopropylique est métabolisé plus lentement que l’éthanol, principalement en acétone. Métabolites et alcool isopropylique inchangésont principalement excrétés dans l’urine.
L’alcool isopropylique est environ deux fois plus toxique que l’éthanol et ne doit donc pas être administré par voie orale; l’alcool isopropylique a également ungoût désagréable. Les symptômes de la toxicité de l’alcool isopropylique sont similaires à ceux de l’éthanol, sauf que l’alcool isopropylique n’a pas d’action initialement euphorique et que la gastrite et les vomissements sont plus importants; Voirl’alcool. L’osmolalité Delta peut être utile comme test de dépistage rapide pour identifier les patients à risque de complications dues à l’ingestion d’isopropylalcool. La dose orale létale est estimée à environ 120-250 ml, bien que des symptômes toxiques puissent être produits par 20 mL.
Les effets indésirables suivants l’administration parentérale de jusqu’à 20 ml d’alcool isopropylique dilué avec de l’eau n’ont inclus qu’une sensation de chaleur et une légère baisse de la pression artérielle. Cependant, l’alcool isopropylique n’est pas couramment utilisé dans les produits parentéraux.
Bien que l’inhalation puisse provoquer une irritation et un coma, l’inhalation d’alcool isopropylique a été étudiée dans des applications thérapeutiques.
L’alcool isopropylique est le plus fréquemment utilisé dans les préparations pharmaceutiques topiques où il peut agir comme un irritant local. Lorsqu’il est appliqué à l’œil, il peut provoquer des brûlures cornéennes et des lésions oculaires.
DL50 (chien, voie orale): 4,80 g / kg
DL50 (souris, voie orale): 3,6 g / kg
LD50 (souris, IP): 4,48 g / kg
LD50 (souris, IV): 1,51 g/ kg
LD50 (lapin, voie orale): 6,41 g/ kg
LD50 (lapin, peau): 12,8 g/ kg
LD50 (rat, IP): 2,74 g /kg
DL50 (rat, IV): 1,09 g/kg
DL50 (rat, oral): 5,05 g/kg
Synthèse chimique
Synthétiquement préparée à partir d’acétylène ou de propylène.
Cancérogénicité
Des souris CD-1 ont été exposées par inhalation à 0, 500, 2500 ou 5000 ppm de vapeur d’isopropanol pendant 6 h/jour, 5 jours/semaine pendant 18 mois. Un groupe supplémentaire de mice (tous les niveaux d’exposition) a été affecté à un groupe de récupération qui a été exposé à l’isopropanol pendant 12 mois, puis maintenu jusqu’à la fin de l’étude à 18 mois. Aucune fréquence accrue de lésions néoplasiques n’a été observée chez aucun des animaux exposés à l’isopropanol. Les lésions non plasmatiques étaientlimité aux testicules (mâles) et au rein. Dans les testicules, l’élargissement des vésicules séminales s’est produit en l’absence de changements inflammatoires ou dégénératifs associés. Les effets du rein comprenaient une protéinose tubulaire et / ou une tubulardilatation. L’incidence des effets testiculaires et rénaux n’a pas augmenté chez les animaux en convalescence exposés à l’isopropanol.
stockage
L’alcool isopropylique doit être conservé dans un endroit frais, sec et bien ventilé, dans des contenants hermétiquement fermés munis d’une étiquette appropriée. Le stockage extérieur ou détaché est préférable. Le stockage intérieur doit être une salle ou une armoire de stockage de liquides inflammables. Les travailleurs ne doivent pas stocker d’alcool isopropylique à une température supérieure à 37 °C (100 °F). Les contenants d’alcool isopropylique doivent être protégés contre les dommages physiques et le contact avec l’air et doivent être conservés séparément des oxydants puissants, de l’acétaldéhyde, du chlore, de l’oxyde d’éthylène, des acides et des isocyanates. L’alcool isopropylique doit être transporté au laboratoire le plus proche le plus rapidement possible dans des récipients frais.
Méthodes de purification
L’alcool isopropylique est préparé commercialement par dissolution du propène dans H2SO4, suivie d’une hydrolyse de l’ester sulfate. Les principales impuretés sont l’eau, les alcools inférieurs et les produits d’oxydation tels que les aldéhydes et les cétones. La purification de l’isopropanol suit sensiblement la même procédure que pour l’alcool n-propylique. L’isopropanol forme un mélange à ébullition constante, b 80,3o, avec de l’eau. La majeure partie de l’eau peut être éliminée de cet isopropanol à 91% par reflux avec du CaO (200g /L) pendant plusieurs heures, puis distillation. Le distillat peut être séché davantage avec des tamis moléculaires CaH2, ruban de magnésium, BaO, CaSO4, calcium, CuSO4 anhydre ou Linde type 5A. La distillation de l’acide sulfanilique élimine l’ammoniac et d’autres impuretés basiques. Les peroxydes peuvent être éliminés par reflux avec du chlorure stanneux solide ou avec du NaBH4 puis l’alcool est distillé de manière fractionnée. Pour obtenir de l’isopropanol ne contenant que 0,002 M d’eau, du sodium (8g /L) est dissous dans un matériau séché par distillation à partir de CaSO4. On ajoute ensuite du benzoate d’isopropyle (35 ml) et, après 3 heures de reflux, on distille l’alcool à travers une colonne Vigreux de 50 cm (p 11). D’autres étapes de purification de l’isopropanol comprennent le reflux avec de l’isopropoxyde d’aluminium solide, le reflux avec du NaBH4 pendant 24 heures et l’élimination de l’acétone par traitement et distillation à partir de la 2,4-dinitrophénylhydrazine. Les peroxydes se reforment dans l’isopropanol s’ils sont maintenus plusieurs jours au contact de l’air.
Incompatibilités
Incompatibles avec des agents oxydants tels que le peroxyde d’hydrogène etl’acide nitrique, qui provoquent la décomposition. L’alcool isopropylique peut être éliminé des mélanges aqueux par addition de chlorure de sodium, de sulfate de sodium et d’autres sels, ou par addition d’hydroxyde de sodium.
Précautions
Les travailleurs doivent se laver soigneusement les mains et le visage après avoir manipulé de l’alcool isopropylique. Les travailleurs doivent porter des gants, des lunettes de sécurité et un écran facial, des bottes, un tablier et une combinaison entièrement imperméable est recommandée si une grande partie du corps est exposée.
Statut réglementaire
Inclus dans la base de données des ingrédients inactifs de la FDA (gélules orales, comprimés et préparations topiques). Inclus dans les médicaments non parentéraux autorisés au Royaume-Uni. Inclus dans la Liste canadienne des Ingrédients non médicinaux acceptables.