Introduction
Chez les patients atteints de SCAP admis aux soins intensifs, la mortalité varie de 25% à 40%.1-4 Dans de nombreuses séries, Legionella spp. se classe deuxième après Streptococcus pneumoniae dans la liste des agents responsables de la SCAP.5-9 L’incidence de la légionellose a augmenté aux États-Unis au cours des dernières décennies.10 Bien qu’il ait été suggéré qu’un diagnostic présomptif de LD puisse être posé même en cas de SCAP, la plupart des auteurs estiment que les caractéristiques cliniques et de laboratoire de la LD ne sont pas distinctives5–9,11–13; c’est pourquoi la couverture empirique de Legionella spp. est fortement recommandé dans la plupart des lignes directrices internationales pour la gestion du SCAP.1-4,13 Une fois que Legionella pneumophila a été confirmée comme agent étiologique d’une pneumonie sévère, certains experts suggèrent que la thérapie combinée serait préférable à la monothérapie, bien qu’il n’y ait aucune preuve solide pour le confirmer.1-9, 11-15 En cas de thérapie combinée, le macrolide ou la fluoroquinolone en plus de la rifampicine est l’approche généralement suggérée; encore une fois, les preuves scientifiques à l’appui de cette affirmation sont rares.14,16 À notre connaissance, seules quelques études monocentriques et rétrospectives se sont concentrées sur des patients en soins intensifs atteints de PAC due à L. pneumophila.17-21 Notre hypothèse était que l’antibiothérapie combinée améliore les résultats chez les patients gravement malades atteints de SCAP causés par L. pneumophila; le principal résultat de la présente étude était de comparer la mortalité en soins intensifs; l’analyse a été effectuée chez tous les patients admis aux soins intensifs et par la suite uniquement chez les patients en état de choc. Les objectifs secondaires étaient de documenter l’épidémiologie et les options thérapeutiques.
Patients et méthodes
L’étude CAPUCI a rassemblé tous les patients admis pour la SCAP dans trente-trois hôpitaux en Espagne, du 1er décembre 2000 au 28 février 2002.22 Dans l’étude CAPUCI2, un projet approuvé par le RCEC, des données ont été enregistrées auprès de patients admis en soins intensifs pour la SCAP, de 2008 à 2011. Nous avons analysé les patients inscrits dans ces grandes séries pour mieux comprendre le traitement actuel et les résultats de la pac sévère admise en USI causée par L. pneumophila. Le comité d’éthique a renoncé au consentement éclairé en raison de la nature observationnelle de l’étude. Les patients ont été admis aux soins intensifs soit pour subir une ventilation mécanique, soit parce qu’ils étaient dans un état instable nécessitant des soins médicaux intensifs.23 Patients atteints d’une maladie chronique grave chez lesquels la pneumonie était un événement terminal attendu n’ont pas été inclus. Au moins l’un des tests suivants a été nécessaire pour établir un diagnostic de LD: isolement de L. pneumophila de tout échantillon de culture respiratoire sur un milieu sélectif d’extrait de levure de charbon tamponné; une détection positive du test d’antigène urinaire par immunoessai enzymatique; un test d’anticorps immunofluorescents indirects montrant une multiplication par quatre des anticorps IgG, en utilisant un kit ELISA commercial contre L. pneumophila. Les prescriptions d’antibiotiques et la décision d’initier un traitement en monothérapie ou en association ont été laissées à la discrétion du médecin traitant et n’ont pas été protocolisées. Les patients ont été observés jusqu’au décès ou à la sortie des soins intensifs. Les données sur les doses d’antibiotiques n’ont pas été enregistrées.
Définitions
Le CAP a été défini comme une infection aiguë des voies respiratoires inférieures caractérisée par : (1) un infiltrat pulmonaire aigu à la radiographie pulmonaire, (2) les résultats confirmatifs d’un examen clinique et (3) l’acquisition de l’infection à l’extérieur d’un hôpital, d’un établissement de soins de longue durée ou d’une maison de retraite. Le diagnostic de fumeur actif, d’alcoolisme et de bronchopneumopathie chronique obstructive (MPOC) a été établi avec des critères rapportés ailleurs.24,25 L’immunocompromise a été définie comme une immunodéficience primaire ou une immunodéficience secondaire à une radiothérapie, à l’utilisation de médicaments cytotoxiques ou de stéroïdes (doses quotidiennes de > 20 mg de prednisolone ou équivalent pour > 2 semaines), 26 ou du sida. Le choc a été défini comme le besoin de vasopresseur pendant > 4h après le remplacement du liquide; la propagation radiographique rapide a été définie comme une augmentation de la taille des opacités sur la radiographie thoracique par > de 50% à 48h. La monothérapie a été définie comme l’administration du même antibiotique unique au cours des 2 premiers jours d’admission aux soins intensifs. La thérapie combinée a été définie comme l’administration des deux mêmes antibiotiques dans les 2 premiers jours suivant l’admission aux soins intensifs.
Analyse statistique
La mortalité en soins intensifs a été choisie comme critère d’évaluation principal. Toutes les feuilles de calcul de données, les codes d’analyse et les extrants ont été stockés et archivés électroniquement. La validation des données consistait à rechercher des valeurs hors de portée et manquantes, ainsi qu’un manque de cohérence entre la détection des variables connexes. Les caractéristiques générales obtenues au départ, les facteurs de risque et d’autres variables ont été comparés et résumés. Les variables qualitatives ont été résumées en utilisant des fréquences absolues et relatives pour chaque groupe. Les différences entre les groupes ont été testées à l’aide du test exact de Fisher. Les variables quantitatives ont été résumées à l’aide de la moyenne, de l’écart-type et des cas valides pour chaque groupe. Les différences entre les groupes ont été testées à l’aide du test de Mann–Whitney–Wilcoxon. La méthode limite de produit de Kaplan–Meier a été utilisée pour construire des courbes de survie pour les patients recevant des schémas d’association et de monothérapie. Toutes les décisions statistiques étaient fondées sur un niveau de signification de 5 %. Toute la gestion des données et l’analyse statistique ont été effectuées à l’aide de SPSS 15.0 (SPSS Inc., Chicago, IL, États-Unis).
Résultats
Les données de 779 patients atteints de SCAP en USI ont été extraites. Un total de 25 patients ayant reçu un diagnostic de pneumonie à L. pneumophila ont été recrutés, dont 15 (60%) ont présenté un choc à l’admission. Tous les patients présentaient des formes sporadiques de la maladie du légionnaire. Sept patients (28%) sur 25 sont décédés après une médiane de 7 jours de ventilation mécanique; tous les décès étaient secondaires à une défaillance multiorganique et étaient liés à une pneumonie. L’âge médian des patients était de 55 ans et le score médian d’APACHE II était de 19. Treize patients (52 %) étaient fumeurs. Les conditions de comorbitie les plus courantes étaient: la cardiomyopathie (32%) et le diabète sucré (20%). Dix-neuf patients (76%) ont eu besoin de MV. L’âge était significativement similaire chez les patients en état de choc et sans choc. Le score APACHE II moyen et la durée de séjour avaient tendance à être plus élevés chez les groupes de patients en état de choc, mais sans atteindre de différences statistiques significatives. Le besoin de ventilation mécanique, la propagation radiographique rapide et la mortalité aux soins intensifs étaient significativement plus élevés dans le sous-ensemble des chocs. Une lésion rénale aiguë a été documentée chez 2 patients (8 %). D’autres caractéristiques de base de la population étudiée sont décrites dans le tableau 1. Le tableau 2 présente les méthodes de diagnostic utilisées pour détecter l’infection par Legionella spp.; 87,5% des patients étaient positifs pour la détection urinaire de l’antigène.
Rendement des tests diagnostiques pour 25 patients atteints de la maladie du légionnaire sévère admis aux soins intensifs.
| Test | No. of performed test | No. of positive results, n (%) |
| Urine antigen detection | 24 | 21 (87.5) |
| Sputum culture | 16 | 4 (25.0) |
| Bronchoscopic samples culture | 15 | 5 (33.3) |
| Pleural fluid culture | 3 | 1 (33.3) |
| Sérologie | 13 | 8(53.3) |
Unité de soins intensifs.
Dix patients ont été traités en monothérapie et 50% de ce groupe sont décédés: la lévofloxacine et la clarithromycine étaient les antibiotiques les plus administrés; chaque médicament a été prescrit à 4 patients. Tous les patients traités par lévofloxacine sont décédés alors que seulement 1 patient sur 4 ayant reçu de la clarithromycine n’a pas survécu. Quinze patients ont reçu une thérapie combinée; 2 patients sur 15 ont expiré. La thérapie combinée la plus utilisée était la rifampicine et la clarithromycine, cette combinaison a été administrée chez 3 patients: 1 personne sur 3 ayant reçu cette combinaison est décédée. La deuxième thérapie combinée la plus utilisée était la clarithromycine, la ciprofloxacine et la rifampicine, et la clarithromycine, la lévofloxacine et la rifampicine. Chacune des combinaisons précédentes a été administrée chez 2 patients. Un patient a expiré après avoir été traité avec de la clarithromycine, de la ciprofloxacine et de la rifampicine.
Les caractéristiques des patients ayant reçu un traitement en monothérapie ou en association sont présentées dans le tableau 3. Les patients traités en association présentaient un taux de mortalité en USI inférieur à celui des patients traités en monothérapie (OU de décès de 0,15; IC à 95% de 0,02 à 1,04; p = 0,08). Lorsque l’analyse a été effectuée chez des patients en état de choc, l’association entre la thérapie combinée et la diminution de la mortalité était plus forte avec une signification statistique (OU de décès 0,06; IC à 95% 0,004–0,86; p = 0,04). Les données démographiques pour les patients en état de choc ayant reçu un traitement en association par rapport à une monothérapie étaient comparables, comme le montre le tableau 4. Le temps de survie des patients traités en association par rapport à la monothérapie est représenté (p = 0,04) à l’aide d’une courbe de survie de Kaplan–Meier (Fig. 1).
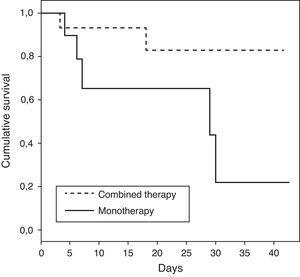
Courbe de survie de Kaplan–Meier pour les patients ayant reçu un traitement de choc en association par rapport à la monothérapie censurée à 40 jours (test de rang log: valeur p = 0,04).
Discussion
Il s’agit de la première étude signalant que les patients atteints de légionellose et de choc peuvent bénéficier de deux agents au lieu d’un. De plus, à notre connaissance, il s’agit de la plus grande série de SCAP de L. pneumophila chez des patients en USI qui a été analysée dans une étude prospective multicentrique: les études précédentes étaient généralement monocentriques et rétrospectives.14,17-21 De plus, notre population était homogène puisque tous les patients remplissaient les critères d’inclusion de la LD sporadique acquise dans la communauté.27 Un écueil généralisé des séries précédentes sur la LD sévère est que la détection de l’antigène de la légionelle n’a pas été utilisée dans le cadre des méthodes de diagnostic. Cet inconvénient doit être pris en compte car il a été suggéré que la détection positive de l’antigène urinaire pourrait être associée à une forme plus grave de la maladie.28
Les résultats d’au moins deux études ont démontré que l’antibiothérapie combinée améliore la survie chez les patients gravement malades présentant une infection grave et un état de choc.29,30 Une étude récente incluant une DL légère à modérée chez 49 patients cancéreux confirme que la thérapie combinée est corrélée à de meilleurs résultats, en particulier chez les patients atteints de pneumonie sévère.31 Gacouin et coll. rapportée en 2002, une série rétrospective de 43 cas de Légionelles sévères spp. pneumonie admise à l’USI: les auteurs ont conclu que le traitement combiné avec des quinolones était la meilleure option thérapeutique pour la LD sévère.21 Les données de notre étude suggèrent que la thérapie combinée est meilleure que la monothérapie dans le cadre de SCAP par L. pneumophila chez les patients en état de choc.
Les données de laboratoire et expérimentales soutiennent le concept selon lequel les fluoroquinolones et les nouveaux agents macrolides / azalides contre L. pneumophila sont supérieurs à l’érythromycine.5-7, 14, 32 L’azithromycine, une excellente option thérapeutique dans la LD sévère, 5-7, 14, 32-34 a été administrée chez un seul patient. La raison en est que l’azithromycine n’était pas disponible en Espagne lorsque l’étude CAPUCI a été réalisée. Le patient qui a reçu de l’azithromycine a été inscrit à l’étude CAPUCI II.
Dans notre série, différemment des études similaires antérieures, de nouvelles fluoroquinolones ou macrolides ont été administrés dans tous les cas. La clarithromycine s’est avérée être un agent anti-légionellose efficace dans les LD non sévères, mais l’efficacité clinique dans le cadre de l’USI n’a pas été établie jusqu’à présent.14,35,36 Trois patients sur quatre ayant reçu de la clarithromycine ont survécu. Bien que le petit nombre de patients de notre série soit clairement un inconvénient majeur, nos résultats suggèrent que la clarithromycine pourrait être un bon agent thérapeutique dans les LD sévères.
Des études récentes suggèrent que la lévofloxacine devrait être le médicament de choix pour le traitement des LD35,37, 38 légères à modérées; d’autre part, il existe un certain manque de cohérence quant à son utilisation en monothérapie dans les cas graves de LD, en particulier lorsque la ventilation mécanique est nécessaire.14,35-37 Le constat de décès chez nos quatre patients exclusivement traités par lévofloxacine soulève certaines inquiétudes quant à son utilisation en monothérapie chez ce sous-ensemble de patients gravement malades, bien que le petit nombre de patients ne permette pas de conclusions définitives. La controverse entre les nouveaux macrolides et les fluoroquinolones en tant que traitement de choix de la LD sévère dépasse la portée de cette discussion puisque cette étude n’a pas été conçue pour se concentrer sur cette question.
La rifampicine est très active contre L. pneumophila à la fois in vitro et sur le modèle animal5,14; cependant, son utilisation clinique en monothérapie a été exclue en raison de préoccupations de résistance accrue au médicament. Néanmoins, au moins une étude sur un modèle animal a nié une augmentation de la résistance aux antibiotiques.39 Les données expérimentales sur des modèles animaux montrent que le taux de destruction bactérienne est considérablement plus élevé lorsque la rifampicine est ajoutée à d’autres antibiotiques.40 L’association des macrolides et de la rifampicine a été la thérapie combinée recommandée pour traiter la LD sévère.5,14 Au contraire, dans les cas de LD non sévère, cette association n’était pas supérieure à celle de la monothérapie.36
Notre étude présente certaines limites. Premièrement, comme pour d’autres publications explorant cette question, les résultats ne proviennent pas d’une étude contrôlée randomisée. Deuxièmement, la petite taille de l’échantillon; cependant, il est peu probable qu’un essai clinique comparatif adéquat puisse être achevé. Les données de notre étude ont été recueillies à partir de deux périodes chronologiques différentes, de sorte qu’il peut y avoir des facteurs de confusion qui ne peuvent pas être corrigés ni ajustés. Une autre limitation pertinente est que l’azithromycine, une excellente option thérapeutique pour traiter la LD sévère, n’a été administrée qu’à un seul patient car elle n’était pas disponible en Espagne sous forme intraveineuse jusqu’à récemment. Enfin, le retard de l’antibiothérapie par rapport à l’apparition de la pneumonie n’a pas été enregistré. Des études plus récentes devraient être effectuées en comparant des antibiotiques récents, mais cela n’est pas réalisable en raison du petit nombre de patients actuellement compliqués avec le MV.
Conclusions
En résumé, nos résultats montrent une réduction de la mortalité en soins intensifs chez les patients atteints de SCAP causée par L. pneumophila et de choc, lorsque la thérapie combinée est administrée au lieu de la monothérapie. Nos résultats sont cohérents avec d’autres études observationnelles suggérant que la thérapie combinée améliore la survie dans le sous-ensemble des patients les plus gravement malades atteints de SCAP.
Soutien financier
2001/SGR414, RESPIRA ROUGE ISCIII (RTIC 03/11) et FISS (PI 04/1500).
Conflits d’intérêts
Le Dr Rello siège au bureau du président et aux conseils consultatifs de Pfizer. Les autres auteurs n’ont déclaré aucun conflit d’intérêts.
CAPUCI 2 était un projet soutenu par l’ESICM (European Society of Intensive Care Medicine) et soutenu par l’ECCRN (European Critical Care Research Network).