- Isopropylalkohol Kjemiske Egenskaper,Bruksområder,Produksjon
- beskrivelse
- Produksjonsprosess
- Bruker
- Toksisitet
- Begrenset bruk
- Kjemiske Egenskaper
- Forekomst
- Bruker
- Bruker
- Bruker
- Bruker
- Bruker
- Definisjon
- Produksjonsmetoder
- Produksjonsmetoder
- Aroma terskelverdier
- Generell Beskrivelse
- Luft & Vannreaksjoner
- Reaktivitetsprofil
- Fare
- Helsefare
- Brannfare
- Kjemisk Reaktivitet
- Farmasøytiske Anvendelser
- Sikkerhet
- kjemisk syntese
- Karsinogenitet
- lagring
- Rensemetoder
- Inkompatibilitet
- Forholdsregler
- Regulatorisk Status
Isopropylalkohol Kjemiske Egenskaper,Bruksområder,Produksjon
beskrivelse
Isopropanol er også kjent som isopropylalkohol. Det er den enkleste sekundære alkoholen og er en av isomerer av n-propanol. Det er en slags brannfarlig væske som er fargeløs med sterk lukt som ligner lukten av blandingen av etanol og aceton. Det er løselig i vann, alkohol, eter, benzen, kloroform og de fleste organiske løsningsmidler og kan blandes med vann, alkohol, eter og kan danne azeotrope med vann. Tetthet (spesifikk vekt): 0.7863g / cm3, smeltepunkt: -88.5 ℃, kokepunkt: 82.5 ℃, flammepunkt: 11.7 ℃, tennpunkt: 460 ℃, brytningsindeks: 1.3772. Dens damp kan forårsake liten irritasjon på øynene, nesen og halsen; det kan absorberes gjennom huden. Dens damp kan danne eksplosiv blanding med luft. Eksplosjonsgrensen er 2,0% til 12% (volum). Det tilhører et moderat eksplosivt farlig materiale og brannfarlig, lavt giftig stoff. Toksisiteten av dampene er dobbelt så høy som etanol, mens oral administrasjon forårsaker motsatt toksisitet.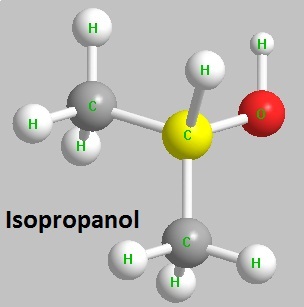
Figur 1 Er strukturformelen av isopropanol.I mange tilfeller kan isopropanol erstatte etanol som løsningsmiddel og er et godt løsningsmiddel og kjemiske råvarer som kan brukes til ikke bare maling, legemidler, plantevernmidler, kosmetikk og andre næringer, men også produksjon av aceton, isopropylester, isopropylamin (råmaterialet for produksjon av atrazin), di-isopropyleter, isopropylacetat og tymolkrystall etc. Det var det første produktet som er laget av petroleumsråmaterialet i historien om utviklingen av petrokjemikalier.
Produksjonsprosess
I 1855 rapporterte Franskmannen M. Berthelot først produksjonen av isopropanol gjennom hydreringsreaksjonen mellom propylen og svovelsyre, kalt indirekte hydrering. I 1919 hadde Amerikanerne C. Ellis gjennomført industriell utvikling på dette. På slutten Av 1920 vedtok American Standard Oil Company Of New Jersey tilnærmingen Til Ellis Act og etablerte produksjonsutstyr for å sette inn formell produksjon. I 1951 Begynte Det Britiske selskapet Imperial Chemical Industries å produsere isopropanol med direkte hydratiseringsmetode fra propylen. Siden da har mange land brukt denne metoden og gjort relaterte forbedringer.
Indirekte hydratiseringsreaksjon: propylen blir først reagert med svovelsyre for å oppnå isopropylhydrogensulfat, som genererer isopropanol etter hydrolyse, og reaksjonen av formelen:
CH3CH = CH2 + H2SO4 → (CH3) 2CHOSO3H
(CH3) 2CHOSO3H + H2O ─ → (CH3) 2CHOH + H2SO4
konsentrasjonen av den påførte svovelsyren er generelt større enn 60% (etter masse), og reaksjonen utføres ved 2~2,8 mpa og 60~65 ° c; Hydrolysereaksjonen skjer ved svakt økt trykk og ved under 30 ° c.
Direkte Hydrering: propylen HAR DIREKTE HYDRATISERINGSREAKSJON MED VANN I NÆRVÆR AV EN KATALYSATOR VED OPPVARMING OG ØKT TRYKK FOR Å GENERERE ISOPROPANOL MED en selektivitet PÅ 96%. Reaksjonen er: CH3CH = CH2 + H2O → (CH3) 2CHOH; den brukte katalysatoren inkluderer wolframforbindelse, fosfat og ionbytterharpiks; den vanlige katalysatoren er fosforsyrekatalysator med bærer (se fast syrekatalysator) med betingelser på 2~6mpa, 240~260 ° C. Sammenlignet med den indirekte metoden har denne metoden ikke noe problem med svovelsyrekorrosjon og fortynnet syrekonsentrasjon, og derfor er den dominerende i industriell produksjon.
ovennevnte informasjon er redigert Av Chemicalbook Of Dai Xiongfeng.
Bruker
Isopropylalkohol er en viktig kjemiske produkter og råvarer. Det brukes hovedsakelig på ulike felt, inkludert farmasøytisk, kosmetikk, plast, dufter, maling, samt å bli brukt som dehydreringsmiddel og rengjøringsmiddel i og elektronikkindustrien. Det kan også brukes som reagens for bestemmelse av barium, kalsium, magnesium, nikkel, kalium, natrium og strontium. Det kan også brukes som referansemateriale for kromatografisk analyse.
i industrien av kretskort, er det brukt som et rengjøringsmiddel, og produksjon AV PCB hull for ledningsevne. Mange finner at det ikke bare kan rense hovedkortet med utmerket ytelse, men også få de beste resultatene. I tillegg brukes den til andre elektroniske enheter, inkludert rengjøring av diskpatron, diskettstasjoner, magnetbånd og laserspissen på diskdriveren PÅ CD-eller DVD-spilleren.
Isopropylalkohol kan også brukes som løsemiddel av olje og gel, så vel som for fremstilling av fiskemel feed konsentrat. Isopropanol av lav kvalitet kan også brukes i bilbrensel. Som råmaterialet til produksjon av aceton reduseres bruksmengden av isopropanol. Det er flere forbindelser som syntetiseres fra isopropanol, som isopropylester, metylisobutylketon, di-isopropylamin, di-isopropyleter, isopropylacetat, tymol og mange typer estere. Vi kan levere isopropanol av forskjellig kvalitet avhengig av sluttbruk den. Den konvensjonelle kvaliteten på vannfri isopropanol er mer enn 99%, mens isopropanolinnholdet er høyere enn 99,8% (for smaker og stoffer).
Toksisitet
adi-verdi er ikke spesifisert (FAO / WHO, 2001).
LD5050: 45rag/kg (rotte, oral).
Begrenset bruk
FEMA (mg/kg): brus: 25; søtsaker: 10 til 75; bakt bra: 75.
Kjemiske Egenskaper
Isopropylalkohol Er en klar, fargeløs, mobil, flyktig, brennbar væske med en karakteristisk, spirituell lukt som ligner en blanding av etanol og aceton; den har en litt bitter taste.It er blandbar med vann, etyleter og etylalkohol. Isopropylalkohol er uforenlig med sterke oksidasjonsmidler, acetaldehyd, klor, etylenoksid, syrer og isocyanater.
Forekomst
Rapportert funnet i eple-og konjakkaromaer (forestret). Også funnet i eple, banan, grapefrukt og limejuice, melon, papaya, pære, løk, erter, rutabaga, tomat, hvetebrød, oster, melk, kokt egg, kokt biff, svinekjøtt og fårekjøtt, hopoil øl, rom, kakao, kaffe, scotch whisky, drue viner, peanut, pecan, soyabønner, honning, bønner, plomme brandy, valnøtt, krabbe,musling, stikkende pære og clary salvie.
Bruker
Isopropylalkohol brukes i produksjon av aceton, isopropylhalogenider, glyserin og aluminiumisopropoksid; brukes mye som et industrielt løsemiddel for maling, polering og insektmidler; som et antiseptisk (gniddende alkohol); og i organisk syntese for innføring av isopropyl-eller isopropoksygruppen i molekylet. Å være et vanlig laboratorieoppløsningsmiddel som metanol, er eksponeringsrisikoen alltid høy; imidlertid er toksisiteten relativt lav.
Bruker
isopropylalkohol er en bærer, anti-bakteriell, og løsemiddel for hudpleie lotions. Isopropylalkohol er laget av propylen, et petroleumderivat.
Bruker
sammenlignet med etanol, er 50% mindre nødvendig for nukleinsyreutfelling, og minimerer dermed det totale volumet som skal sentrifugeres FOR DNA – eller RNA-utvinning.
Bruker
Egnet FOR HPLC, spektrofotometri, miljøtesting
Bruker
i frostvæskeblandinger; som løsemiddel for tannkjøtt, shellak, essensielle oljer; i ekstraksjon av alkaloider; i hurtigtørkende oljer; i hurtigtørkende blekk; i denaturerende etylalkohol; i kroppsskrubb; håndkrem, etterbarberingskrem og lignende kosmetikk. Løsemiddel for kreosot, harpiks, tannkjøtt; i produksjon av aceton, glyserol, isopropylacetat. Farmakeutisk hjelpemiddel (løsemiddel).
Definisjon
ChEBI: En sekundær alkohol som er propan der en av hydrogenene festet til det sentrale karbonet er erstattet av en hydroksygruppe.
Produksjonsmetoder
Isopropylalkohol kan fremstilles fra propylen; ved katalytisk reduksjon av aceton, eller ved gjæring av visse karbohydrater.
Produksjonsmetoder
To grunnleggende produksjonsmetoder er i kommersiell bruk: (1) absorpsjon av propylen i svovelsyre for å danne alkylhydrogensulfat, etterfulgt av hydrolysen av esteren; og (2) ved direkte hydrering med vann ved bruk av en katalysator. En iboende ulempe i den første prosessen er behovet for å håndtere svovelsyre. Videre gir den første prosessen litt mer enn 70% isopropanol sammenlignet med den andre prosessen, hvor flytende propylen brukes som ladestammen. Alle direkte hydratiseringsprosesser kan representeres AV: C3H6 + H2O ??→ C3H7OH + varme.
Aroma terskelverdier
Deteksjon: 40 til 601 ppm
Generell Beskrivelse
Flyktig, fargeløs væske med en skarp muggen lukt som rubbing alkohol. Flammepunkt på 53°F. Damp er tyngre enn luft og mildt irriterende for øyne, nese og hals. Tetthet ca 6,5 lb / gal. Brukes i å lage kosmetikk, hud og hår preparater, legemidler, parfyme, lakk formuleringer, fargestoff løsninger, frostvæske, såper, vindu rengjøringsmidler. Selges i 70% vandig løsning som rubbing alkohol.
Luft & Vannreaksjoner
meget brannfarlig. Vannløselig.
Reaktivitetsprofil
isopropanol reagerer med luft eller oksygen for å danne farlig ustabile peroksider. Kontakt med 2-butanon øker frekvensen av peroksiddannelse. An explosive reaction occurs when Isopropanol is heated with (aluminum isopropoxide + crotonaldehyde). Forms explosive mixtures with trinitromethane and hydrogen peroxide. Reacts with barium perchlorate to form a highly explosive compound. Ignites on contact with dioxygenyl tetrafluoroborate, chromium trioxide and potassium-tert-butoxide. Vigorous reactions occur with (hydrogen + palladium), nitroform, oleum, COCl2, aluminum triisopropoxide and oxidizing agents. Reacts explosively with phosgene in the presence of iron salts. Incompatible with acids, acid anhydrides, halogens and aluminum . Isopropanol kan reagere Med PCl3, som danner giftig HCl-gass. (Logsdon, John E., Richard A. Loke., sopropylalkohol. Kirk-Othmer Encyclopedia Av Kjemisk Teknologi. John Wiley & Sons, Inc. 1996.).
Fare
Brannfarlig, farlig brannfare, eksplosivbegrensninger i luft 2-12%. Giftig ved inntak og innånding. Øye og øvre luftveier irriterende, sentralnedbrytning av nervesystemet. Tvilsomt karsinogen.
Helsefare
Eksponering for isopropylalkohol forårsaker irritasjon i øynene og slimhinnene. Eksponering for isopropylalkohol i 3-5 min (400 ppm) forårsaket mild irritasjon av øyne, nese og hals, og ved 800 ppm ble disse symptomene alvorlige. Inntak eller en oral dose på 25 mL i 100 mL vann ga hypotensjon, ansiktsbehandling, bradykardi og svimmelhet. Inntak i store mengder forårsaket omfattende hemorragisk tracheobronitt, bronkopneumoni og hemorragisk lungeødem. Langvarig hudkontakt med isopropylalkohol forårsaket eksem og følsomhet. Forsinket dermal absorpsjon tilskrives en rekke pediatriske forgiftninger som har oppstått etter gjentatt eller langvarig svampbading med isopropylalkohol for å redusere feber. I flere tilfeller inkluderte symptomer åndedrettsstress, stupor og koma. Laboratoriedyr utsatt for isopropylalkohol utvikler forgiftning med symptomer på bakbenet lammelse, ustøhet, mangel på muskelkoordinasjon, respiratorisk depresjon og stupor. Isopropylalkohol er et kraftig cns-depressant, og i store doser forårsaker kardiovaskulær depresjon.
Brannfare
SVÆRT BRANNFARLIG: Vil lett antennes av varme, gnister eller flammer. Damp kan danne eksplosive blandinger med luft. Damp kan reise til antennelseskilden og blinke tilbake. De fleste damper er tyngre enn luft. De vil spre seg langs bakken og samle seg i lave eller begrensede områder (kloakk, kjellere, tanker). Dampeksplosjonsfare innendørs, utendørs eller i kloakk. Avrenning til kloakk kan skape brann-eller eksplosjonsfare. Beholdere kan eksplodere ved oppvarming. Mange væsker er lettere enn vann.
Kjemisk Reaktivitet
Reaktivitet Med Vann Ingen reaksjon; Reaktivitet Med Vanlige Materialer: Ingen reaksjoner; Stabilitet Under Transport: Stabil; Nøytraliserende Midler For Syrer Og Etsende Stoffer: Ikke relevant; Polymerisering: Ikke relevant; Polymerisasjonsinhibitor: Ikke relevant.
Farmasøytiske Anvendelser
Isopropylalkohol (propan-2-ol) brukes i kosmetikk og farmasøytiskformuleringer, primært som et løsningsmiddel i topiske formuleringer.(Det anbefales ikke til oral bruk på grunn av dets toksisitet.
Selv om det brukes i lotioner, kan de merkede avfettingsegenskapeneav isopropylalkohol begrense bruken i preparater som brukesflere ganger. Isopropylalkohol brukes også som løsningsmiddel både for tablettfilmbelegg og for tablettgranulering, hvor isopropylalkoholen deretter fjernes ved fordampning. Det har også værtvist for å øke hudpermeabiliteten til nimesulid betydeligfra karbomer 934.Isopropylalkohol har noen antimikrobiell aktivitet og en 70% v/v vandig løsning brukes som et lokalt desinfeksjonsmiddel.Terapeutisk har isopropylalkohol blitt undersøkt forbehandling av postoperativ kvalme eller oppkast.
Sikkerhet
Isopropylalkohol er mye brukt i kosmetikk og aktuellfarmasøytiske formuleringer. Det absorberes lett framage-tarmkanalen og kan sakte absorberes gjennom intactskin. Langvarig direkte eksponering av isopropylalkohol i huden kanresultere i hjerte – og nevrologiske underskudd. Hos nyfødte har isopropylalkohol blitt rapportert å forårsake kjemiske forbrenninger etter aktuell søknad.Isopropylalkohol metaboliseres langsommere enn etanol, primært til aceton. Metabolitter og uendret isopropylalkoholutskilles hovedsakelig i urinen.Isopropylalkohol er omtrent dobbelt så giftig som etanol og bør derfor ikke administreres oralt; isopropylalkohol har også enubehagelig smak. Symptomer på isopropylalkoholtoksisitet er liketil de for etanol, bortsett fra at isopropylalkohol ikke har noen initialeuforisk virkning, og gastritt og oppkast er mer fremtredende; sealkohol. Delta osmolalitet kan være nyttig som rask skjermtest for å identifisere pasienter med risiko for komplikasjoner ved inntak av isopropylalkohol. Den dødelige orale dosen er anslått til ca 120-250mLalthough giftige symptomer kan være produsert av 20 mL.Bivirkninger etter parenteral administrering av opptil 20 ml isopropylalkohol fortynnet med vann har bare inkludert asensasjon av varme og en liten senking av blodtrykket. Isopropylalkohol brukes imidlertid ikke ofte i parenterale produkter.Selv om innånding kan forårsake irritasjon og koma, har inhalasjon av isopropylalkohol blitt undersøkt i terapeutiske applikasjoner.
Isopropylalkohol er mest brukt i topiske pharmaceuticalformulations der det kan virke som en lokal irriterende. Nårpåført øyet kan det forårsake hornhinneforbrenninger og øyeskader.
LD50 (hund, oral): 4,80 g/kg
LD50 (mus, oral): 3,6 g/kg
LD50 (mus, IP): 4,48 g/kg
LD50 (mus, IV): 1,51 g/kg
LD50 (kanin, oral): 6,41 g/kg
LD50 (kanin, hud): 12,8 g/kg
LD50 (rotte, IP): 2,74 G/kg
ld50 (rotte, iv): 1,09 G/kg
ld50 (rotte, oral): 5,05 G/kg
kjemisk syntese
syntetisk fremstilt FRA ACETYLEN eller propylen.
Karsinogenitet
CD-1-mus ble eksponert ved inhalasjontil 0, 500, 2500 eller 5000 ppm isopropanoldamp for6 timer/ dag, 5 dager / uke i 18 måneder. En ekstra gruppe av mus (alle eksponeringsnivåer) ble tildelt en gjenopprettingsgruppe som ble utsatt for isopropanol i 12 måneder og deretter opprettholdt til studieavslutning ved 18 måneder. Det var ingen økt frekvens av neoplastiske lesjoner i noen avisopropanol-eksponerte dyr. Ikke-neoplastiske lesjoner varbegrenset til testene (menn) og nyrene. I testene oppstod forstørrelse av de seminale vesiklene i fraværav tilhørende inflammatoriske eller degenerative endringer. Nyreeffekter inkluderte tubulær proteinose og / eller tubulardilatasjon. Forekomsten av testikulære og nyreeffekterble ikke økt i isopropanol-eksponert utvinningdyr.
lagring
Isopropylalkohol skal oppbevares på et kjølig, tørt, godt ventilert sted i tett lukkede beholdere med riktig etikett. Utendørs eller frittliggende lagring er å foretrekke. Innvendig lagring bør være et brannfarlig oppbevaringsrom eller skap. Arbeidere bør ikke oppbevare isopropylalkohol over 37°C (100°F). Beholdere av isopropylalkohol bør beskyttes mot fysisk skade og kontakt med luft, og bør lagres separat fra sterke oksidasjonsmidler, acetaldehyd, klor, etylenoksid, syrer og isocyanater. Isopropylalkohol skal transporteres til nærmeste laboratorium så raskt som mulig i kjølige beholdere.
Rensemetoder
Isopropylalkohol fremstilles kommersielt ved oppløsning av propen I H2SO4, etterfulgt av hydrolyse av sulfatesteren. Store urenheter er vann, lavere alkoholer og oksidasjonsprodukter som aldehyder og ketoner. Rensing av isopropanol følger i det vesentlige samme fremgangsmåte som for n-propylalkohol. Isopropanol danner en konstant kokende blanding, b 80,3 o, med vann. Det meste av vannet kan fjernes fra denne 91% isopropanolen ved refluxing Med CaO (200g / L) i flere timer, deretter destillasjon. Destillatet kan tørkes videre Med CaH2, magnesium bånd, BaO, CaSO4, kalsium, Vannfri CuSO4 Eller Linde TYPE 5A molekylær sikter. Destillasjon fra sulfanilsyre fjerner ammoniakk og andre grunnleggende urenheter. Peroksider kan fjernes ved refluxing med fast stannous klorid Eller Med NaBH4 deretter alkohol er fraksjonalt destillert. For å oppnå isopropanol som bare inneholder 0,002 m vann, oppløses natrium (8g/L) i materiale tørket ved destillasjon Fra CaSO4. Isopropylbenzoat (35 ml) tilsettes deretter, og etter tilbakeløping i 3 timer destilleres alkoholen gjennom En 50 cm Vigreux-kolonne (p 11). Andre rensetrinn for isopropanol inkluderer tilbakeløping med fast aluminium isopropoksid, tilbakeløping Med NaBH4 for 24 timer, og fjerning av aceton ved behandling med, og destillasjon fra, 2,4-dinitrofenylhydrazin. Peroksider re-form i isopropanol hvis den holdes i flere dager i kontakt med luft.
Inkompatibilitet
Uforenlig med oksidasjonsmidler som hydrogenperoksid ognitronsyre, som forårsaker dekomponering. Isopropylalkohol kan væresaltet ut fra vandige blandinger ved tilsetning av natriumklorid, natriumsulfat og andre salter, eller ved tilsetning av natriumhydroksyd.
Forholdsregler
Arbeidere bør vaske hender og ansikt grundig etter håndtering av isopropylalkohol. Arbeidere bør bruke hansker, vernebriller og ansiktsskjold, støvler, forkle og en full ugjennomtrengelig drakt anbefales hvis eksponering er mulig for en stor del av kroppen.
Regulatorisk Status
Inkludert I FDA Inaktive Ingrediensdatabasen(orale kapsler, tabletter og aktuelle preparater). Inkludert i nonparenteralmedisiner lisensiert i STORBRITANNIA. Inkludert I Den Kanadiske Listen overakseptable Ikke-medisinske Ingredienser.