Jakaantumiskerroin
jakaantumiskerroin on tutkittavan aineen tasapainojakauma näytefaasin ja kaasufaasin välillä.
näytteet on valmistettava niin, että haihtuvien aineosien pitoisuus päätilassa on mahdollisimman suuri ja näytematriisin muista yhdisteistä johtuva ei-toivottu kontaminaatio minimoidaan. Voit auttaa määrittämään pitoisuus analyytin headspace, sinun täytyy laskea jakaantumiskerroin (K).
| K values of common solvents in air-water systems at 40°C | ||||||||
| Solvent | Cyclohexane | n-Hexane | Tetrachlorethylene | 1,1,1-Trichlormethane | O-Xylene | Toluene | Benzene | Dichlormethane |
| K Value | 0.077 | 0.14 | 1.48 | 1.65 | 2.44 | 2.82 | 2.90 | 5.65 |
| Solvent | n-Butylacetate | Ethylacetate | Methylethylketone | n-Butanol | Isopropanol | Ethanol | Dioxane | |
| K Value | 31.4 | 62.4 | 139.5 | 647 | 825 | 1355 | 1618 | |
Calculating the Partition Coefficient
Partition Coefficient (K) = Cs/Cg
where:
Cs is the concentration of analyte in sample phase;
Cg on analyytin pitoisuus kaasufaasissa
Jakaantumiskertoimet yleisissä yhdisteissä
yhdisteet, joilla on alhaiset K-arvot, pyrkivät jakautumaan helpommin kaasufaasiin ja joilla on suhteellisen korkea vaste ja alhaiset havaitsemisrajat. Esimerkki tästä olisi heksaani vedessä: 40°C: n lämpötilassa heksaanin K-arvo olisi ilma-vesijärjestelmässä 0,14.
yhdisteet, joilla on korkeat K-arvot, jakaantuvat herkemmin kaasufaasiin, ja niiden vasteet ovat suhteellisen alhaiset ja havaitsemisrajat korkeat.
esimerkki tästä olisi etanoli vedessä: 40°C: n lämpötilassa etanolin K-arvo on ilma-vesijärjestelmässä 1355.
Jakaantumiskertoimen arvot muille yleisille yhdisteille on esitetty yllä olevassa taulukossa.
Jakaantumiskertoimen muuttaminen
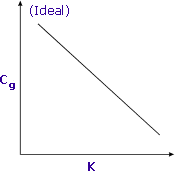 |
epäorgaanisten suolojen lisääminen
suuret suolapitoisuudet vesinäytteissä vähentävät polaaristen orgaanisten haihtuvien aineiden liukoisuutta näytematriisissa ja edistävät niiden siirtymistä päätilaan, jolloin K arvot. Suolauksen poistovaikutuksen suuruus K: ssa ei kuitenkaan ole sama kaikille yhdisteille.
yhdisteet, joiden K-arvot ovat jo suhteellisen alhaiset, kokevat hyvin vähän muutoksia jakautumiskertoimessa lisättyään suolaa vesipitoiseen näytematriisiin.
yleensä polaarimatriiseissa (vesinäytteissä) olevat haihtuvat polaariset yhdisteet kokevat K: n suurimmat siirtymät ja niiden vasteet ovat suuremmat sen jälkeen, kun suola on lisätty näytematriisiin.
yhteiset suolat, joita käytetään matriisivaikutusten vähentämiseen:
- ammoniumkloridi
- ammoniumsulfaatti
- natriumkloridi
- natriumsitraatti
- natriumsulfaatti
- kaliumkarbonaatti
K: n arvo riippuu myös Faasisuhteesta. Tätä käsitellään seuraavassa jaksossa.
Vaihesuhde
vaihesuhde (β) määritellään pään tilan suhteellisena tilavuutena verrattuna näytepullossa olevan näytteen tilavuuteen.
| lasketaan Vaihesuhde Vaihesuhde (β) = Vg / Vs missä: Vs is näytefaasin tilavuus |
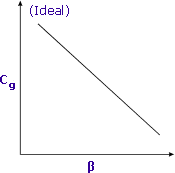 |
| herkkyys kasvaa, kun β on minimoitu |
pienemmät β-arvot (eli suurempi otoskoko) tuottavat suurempia vasteita haihtuville yhdisteille.
β-arvon pienentäminen ei aina anna herkkyyden parantamiseksi tarvittavaa vasteen lisäystä.
Kun β-arvoa pienennetään kasvattamalla näytteen kokoa, yhdisteet, joilla on korkeat K-arvot, jakaantuvat vähemmän päätilaan verrattuna yhdisteisiin, joiden K-arvot ovat alhaiset, ja saanto vastaavasti pienempiä muutoksia Cg: ssä.
näytteet, jotka sisältävät korkeita K-arvoja sisältäviä yhdisteitä, on optimoitava alhaisimman K-arvon saamiseksi ennen kuin faasisuhteessa tehdään muutoksia.
Jakaantumiskertoimen ja Vaihesuhteen yhdistäminen
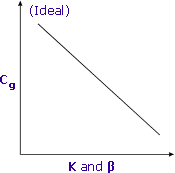
Alempi K ja β johtavat korkeampaan Cg: hen ja parempaan herkkyyteen
Jakaantumiskertoimet ja vaihesuhteet yhdessä määrittävät haihtuvien yhdisteiden lopullisen pitoisuuden näytepullojen päätilassa.
haihtuvien yhdisteiden pitoisuus kaasufaasissa voidaan ilmaista seuraavasti:
CG = Co / (K + β)
missä
Cg on haihtuvien analyyttien pitoisuus kaasufaasissa
ja
Co on haihtuvien analyyttien alkuperäinen pitoisuus näytteessä.
sekä K: n että β: n pienimpien arvojen tavoittelu johtaa korkeampiin haihtuvien analyyttien pitoisuuksiin kaasufaasissa ja siten parempaan herkkyyteen.