A XeF4 vagy Xenon-tetrafluorid egy xenon-és Fluoridatomokból álló kémiai vegyület. Ez a világ első felfedezett bináris vegyülete. Ez egy olyan típusú nemesgáz, amelynek kémiai egyenlete
Xe + 2 F2 – > XeF4
a XeF4 szilárd fehér megjelenésű, sűrűsége 4,040 g cm−3 szilárd formában. Rendes körülmények között színtelen kristályosnak tűnik. Magas hőmérséklete 115,7 Celsius fok vagy 240,26 Fahrenheit fok. A többi Xenon-Fluoridhoz hasonlóan a Xenon-tetrafluorid exergonikus képződéssel rendelkezik. Normál hőmérsékleten és nyomáson stabil állapotban marad. Azonnal reagál a vízzel, és molekuláris oxigént, hidrogén-fluoridot és tiszta xenongázt bocsát ki.
| Name of molecule | Xenon Tetrafluoride (XeF4) |
| No of Valence Electrons in the molecule | 36 |
| Hybridization of XeF4 | sp3d2 hybridization |
| Bond Angles | 90 degrees and 180 degrees |
| Molecular Geometry of XeF4 | Square Planar |
To know more about its physical properties and chemical properties, one needs to know its Lewis szerkezete és molekuláris geometriája. Nézzük meg a Xenon-tetrafluorid Lewis-szerkezetét.
A Lewis-szerkezet létrehozásához ismernünk kell az XeF4 vegyértékelektronjait, hogy felépíthessük, és ismernünk kell az atomok elhelyezkedését a molekulában.
tartalom
XeF4 vegyérték elektronok
ebben a molekulában van egy atom Xenon és négy atom fluor. Kiszámoljuk mindkét Atom vegyértékelektronjait, hogy meghatározzuk az XeF4 vegyértékelektronjainak teljes számát.
A Xenon Vegyértékelektronjai = 8
a fluor Vegyértékelektronjai = 7*4 (mivel négy fluor atom van, 4-gyel megszorozzuk)
a xef4 vegyértékelektronjainak teljes száma: 8 + 7*4
: 8 + 28
: 36
ezért összesen 36 vegyérték elektron van az Xef-Ben4.
XeF4 Lewis szerkezet
most, hogy ismerjük a xenon-tetrafluorid vegyértékelektronjait, könnyebb lesz felhívni a Lewis szerkezetét. Ez a Lewis dot szerkezet a vegyérték elektronok képi ábrázolása a molekula egyes atomjai körül, az általa kialakított kötéssel együtt.
a szerkezetben lévő kötéseket vonalak segítségével mutatjuk be, míg a kötésképződésben nem részt vevő elektronokat pontokként mutatjuk be. Azokat az elektronokat, amelyek nem alkotnak kötést, nem kötő elektronoknak vagy magányos elektronpároknak nevezzük.
itt, mivel a Xenon a legkevésbé elektronegatív atom, a középpontba helyezzük, és az összes többi fluor atom körül, így:

most, hogy az összes atomot elhelyeztük, mutassunk kötéseket az egyes Fluor és Xenon atomok között. A molekula minden egyes kötése két elektronot vesz fel, és mivel ebben a molekulában négy egyetlen kötés van, 8 elektron 36-ból elhasználódik.
kezdje el a többi vegyértékelektron elhelyezését az atomok körül. Minden fluor atomnak hat vegyértékelektronja lesz körülötte, mivel egy elektront használtak a kötés létrehozásához.
észreveheti, hogy már 24 elektronot helyeztünk el a 28-ból a fluor atomok körül. A fennmaradó nem kötődő elektronokat vagy magányos elektronpárokat a xenonra helyezzük, mivel ez kivétel az oktett szabály alól.
helyezze ezt a két nemkötő elektronpárt a xenonra, és most van egy Lewis-szerkezete, ahol két magányos elektronpár van a Xenonon, és hat nemkötő elektron minden fluor atomon.
XeF4 hibridizáció
a központi Xenonatom pályái hibridizálódnak, ami új hibridizált pályák kialakulását eredményezi. A xenonnak hat elektronja van az 5p pályáin, két elektronja pedig az 5S pályáin. A xenon alapállapotában nincsenek elektronok a d-pályákon és az f-pályákon. De amikor ez az atom gerjesztett állapotban van, a p-pályákon két elektron mozog a d-pályákra; ennek eredményeként összesen négy párosítatlan elektron van. Ebből kettő p-pályán van, a másik két párosítatlan elektron pedig d-pályán van. Ezek a hibridizált pályák sp3d2 hibridizációhoz vezetnek az XeF4 – ben.
XeF4 molekuláris geometria
könnyebb megérteni egy adott molekula molekuláris geometriáját, ha ismerjük annak Lewis szerkezetét. Mivel a xenonnak két magányos elektronpárja van, olyan szerkezetet vesz fel, amely segít ezeknek a magányos pároknak elkerülni a taszító erőket. Annak érdekében, hogy ezek a taszítások minimálisra csökkenjenek, a magányos Párok merőleges síkban lesznek. Mivel négy fluor atom van, a molekulának olyan elrendezése lesz, hogy molekuláris geometriája négyzet alakú. Az XeF4 elektronikus geometriája oktaéderes, így a molekuláris geometria Xenon-tetrafluorid négyzet sík.

XeF4 kötési szögek
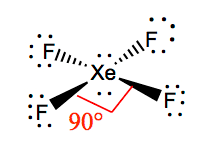
az F-Xe-F kötési szögei 90 fok, a magányos Párok szöge 180 fok. A fluor atomok 90 fokban helyezkednek el egymástól, ami az elektronok szimmetrikus eloszlását eredményezi a molekula síkjában. Ezek a kötési szögek hozzájárulnak a négyzet alakú sík molekuláris geometria kialakulásához.
XeF4 polaritás – az XeF4 poláris vagy nem poláris?
bár a xenon és a fluor atomok közötti kötések polárisak, a XeF4 nem poláros molekula. Vajon hogyan? Az összes Xe-F kötés kölcsönösen ellentétes egymással, így a dipólus Momentum összege nulla. Mivel a Xenon atomon négy elektron található, amelyek nem kötődő elektronpárokként lokalizálódnak. Mivel a molekulában az atomok és elektronok általános elrendezése olyan, hogy a dipólusok vektorösszege nulla, az XeF4 nem poláros molekula.
Záró megjegyzések
A Xenon-tetrafluorid egyike azoknak a molekuláknak, amelyeket viszonylag könnyű megérteni. Lewis szerkezete az egyik legkevésbé bonyolult szerkezet, mivel az összes fluor Atom szimmetrikus mintázatban van elrendezve. A molekula magányos párjai merőleges síkban helyezkednek el oktaéderes alakban, hogy taszító erőiket minimálisra csökkentsék.
Összefoglalva ezt a blogbejegyzést, azt mondhatjuk, hogy az XeF4 36 vegyértékelektronnal rendelkezik. Két magányos pár nem kötődő elektronja van a xenon központi atomján. A molekula oktaéderes elektrongeometriával és négyzet alakú molekuláris geometriával rendelkezik. Az XeF4 nem poláros molekula, sp3d2 hibridizációval rendelkezik.