Das XeF4 oder Xenontetrafluorid ist eine chemische Verbindung aus Xenon- und Fluoridatomen. Es ist die weltweit erste entdeckte binäre Verbindung. Es ist eine Art Edelgas mit der chemischen Gleichung
Xe +2 F2 -> XeF4
Das XeF4 hat ein festes weißes Aussehen und eine Dichte von 4,040 g cm−3 in fester Form. Unter normalen Bedingungen erscheint es wie ein farbloses kristallines. Es hat eine sublime Temperatur von 115,7 Grad Celsius oder 240,26 Grad Fahrenheit. Wie die anderen Xenonfluoride weist auch das Xenontetrafluorid eine exergonische Bildung auf. Bei normaler Temperatur und normalem Druck bleibt es in einem stabilen Zustand. Es reagiert sofort mit Wasser und setzt molekularen Sauerstoff, Fluorwasserstoff und reines Xenongas frei.
| Name of molecule | Xenon Tetrafluoride (XeF4) |
| No of Valence Electrons in the molecule | 36 |
| Hybridization of XeF4 | sp3d2 hybridization |
| Bond Angles | 90 degrees and 180 degrees |
| Molecular Geometry of XeF4 | Square Planar |
To know more about its physical properties and chemical properties, one needs to know its Lewis-Struktur und molekulare Geometrie. Lassen Sie uns die Lewis-Struktur von Xenontetrafluorid herausfinden.
Um die Lewis-Struktur zu erstellen, müssen wir die Valenzelektronen von XeF4 kennen, um seine Struktur zu erstellen und die Platzierung von Atomen im Molekül zu kennen.
Inhalt
XeF4 Valenzelektronen
In diesem Molekül haben wir ein Atom Xenon und vier Atome Fluor. Wir werden die Valenzelektronen dieser beiden Atome berechnen, um die Gesamtzahl der Valenzelektronen von XeF4 zu bestimmen.
Valenzelektronen von Xenon = 8
Valenzelektronen von Fluor = 7*4 ( da es vier Fluoratome gibt, multiplizieren wir es mit 4)
Gesamtzahl der Valenzelektronen von Xef4: 8 + 7*4
: 8 + 28
: 36
Daher gibt es insgesamt 36 Valenzelektronen in XeF4.
XeF4 Lewis-Struktur
Nun, da wir die Valenzelektronen von Xenontetrafluorid kennen, wird es für Sie einfacher sein, seine Lewis-Struktur zu zeichnen. Diese Lewis-Punktstruktur ist eine bildliche Darstellung von Valenzelektronen um einzelne Atome in einem Molekül zusammen mit der Bindung, die es bildet.
Die Bindungen in der Struktur sind mit Linien dargestellt, während die Elektronen, die nicht an der Bindungsbildung beteiligt sind, als Punkte dargestellt sind. Elektronen, die keine Bindung eingehen, werden als nichtbindende Elektronen oder einzelne Elektronenpaare bezeichnet.
Da Xenon das am wenigsten elektronegative Atom ist, platzieren wir es in der Mitte und alle anderen Fluoratome um es herum wie folgt:

Nachdem wir nun alle Atome platziert haben, zeigen wir die Bindungen zwischen jedem Fluor- und Xenonatom. Jede Bindung im Molekül nimmt zwei Elektronen auf, und da es in diesem Molekül vier Einzelbindungen gibt, werden 8 von 36 Elektronen verbraucht.
Beginnen Sie, den Rest der Valenzelektronen um die Atome zu legen. Jedes Fluoratom hat sechs Valenzelektronen um sich herum, da ein Elektron verwendet wurde, um die Bindung herzustellen.
Sie werden vielleicht bemerken, dass wir bereits 24 von 28 Elektronen um die Fluoratome herum platziert haben. Die verbleibenden nicht gebundenen Elektronen oder einzelne Elektronenpaare werden auf Xenon platziert, da dies eine Ausnahme von der Oktettregel darstellt. Platzieren Sie diese beiden Paare von nichtbindenden Elektronen auf Xenon, und jetzt haben Sie eine Lewis-Struktur, in der sich zwei einzelne Elektronenpaare auf Xenon und sechs nichtbindende Elektronen auf jedem Fluoratom befinden.
XEF4-Hybridisierung
Die Orbitale des zentralen Xenonatoms werden hybridisiert, was zur Bildung neuer hybridisierter Orbitale führt. Xenon hat sechs Elektronen in seinen 5p-Orbitalen und zwei Elektronen in 5s-Orbitalen. Es gibt keine Elektronen in d-Orbitalen und f-Orbitalen im Grundzustand von Xenon. Wenn sich dieses Atom jedoch in einem angeregten Zustand befindet, bewegen sich zwei Elektronen in den p-Orbitalen zu d-Orbitalen, wodurch insgesamt vier ungepaarte Elektronen vorhanden sind. Davon befinden sich zwei in p-Orbitalen und die anderen beiden ungepaarten Elektronen in d-Orbitalen. Diese hybridisierten Orbitale führen zur sp3d2-Hybridisierung in XeF4.
XeF4 Molekulare Geometrie
Es ist einfacher, die molekulare Geometrie eines gegebenen Moleküls zu verstehen, sobald wir seine Lewis-Struktur kennen. Da Xenon zwei einsame Elektronenpaare hat, wird es eine Struktur aufnehmen, die diesen einsamen Paaren hilft, die Abstoßungskräfte zu vermeiden. Um diese Abstoßungen auf ein Minimum zu beschränken, befinden sich die einzelnen Paare in einer senkrechten Ebene. Und da es vier Fluoratome gibt, wird das Molekül eine solche Anordnung haben, dass seine Molekülgeometrie quadratisch planar ist. XeF4 hat eine elektronische Geometrie von oktaedrisch, wodurch die Molekülgeometrie von Xenontetrafluorid quadratisch planar wird.

XeF4-Bindungswinkel
Die Bindungswinkel von F-Xe-F betragen 90 Grad, und einzelne Paare haben Winkel von 180 Grad. Die Fluoratome befinden sich in einem Winkel von 90 Grad zueinander, was zu einer symmetrischen Verteilung der Elektronen in der Molekülebene führt. Diese Bindungswinkel tragen zur Bildung einer quadratischen planaren Molekülgeometrie bei.
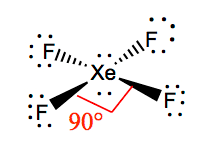
XEF4 Polarität – Ist XeF4 polar oder unpolar?
Obwohl die Bindungen zwischen Xenon- und Fluoratomen polar sind, ist XeF4 ein unpolares Molekül. Sie fragen sich, wie? Alle Xe-F-Bindungen stehen im Gegensatz zueinander, wodurch die Summe des Dipolmoments Null wird. Da sich am Xenonatom vier Elektronen befinden, die als nicht bindende Elektronenpaare lokalisiert sind. Da die Gesamtanordnung der Atome und Elektronen im Molekül so ist, dass die Vektorsumme der Dipole Null ist, ist XeF4 ein unpolares Molekül.
Abschließende Bemerkungen
Xenontetrafluorid ist eines dieser Moleküle, das relativ leicht zu verstehen ist. Seine Lewis-Struktur ist eine der am wenigsten komplizierten Strukturen, da alle Fluoratome im symmetrischen Muster angeordnet sind. Die einzelnen Paare im Molekül befinden sich in einer senkrechten Ebene in einer oktaedrischen Form, um ihre Abstoßungskräfte auf einem Minimum zu halten.
Um diesen Blogbeitrag zusammenzufassen, können wir sagen, dass XeF4 36 Valenzelektronen hat. Es hat zwei einsame Paare von nichtbindenden Elektronen am Zentralatom von Xenon. Das Molekül hat oktaedrische Elektronengeometrie und quadratische planare Molekülgeometrie. XeF4 ist ein unpolares Molekül und hat sp3d2 Hybridisierung.