El Tetrafluoruro de Xenón o XeF4 es un compuesto químico compuesto de átomos de Xenón y Fluoruro. Es el primer compuesto binario descubierto en el mundo. Es un tipo de gas noble que tiene la ecuación química de
Xe +2 F2 -> XeF4
El XeF4 tiene un aspecto blanco sólido y una densidad de 4,040 g cm−3 en forma sólida. En condiciones normales, parece un cristalino incoloro. Tiene una temperatura sublime de 115,7 grados Celsius o 240,26 grados Fahrenheit. Al igual que los otros fluoruros de Xenón, el Tetrafluoruro de Xenón tiene una formación exergónica. A temperatura y presión normales, se mantiene en condiciones estables. Reacciona con el agua al instante y libera oxígeno molecular, fluoruro de hidrógeno y gas xenón puro.
| Name of molecule | Xenon Tetrafluoride (XeF4) |
| No of Valence Electrons in the molecule | 36 |
| Hybridization of XeF4 | sp3d2 hybridization |
| Bond Angles | 90 degrees and 180 degrees |
| Molecular Geometry of XeF4 | Square Planar |
To know more about its physical properties and chemical properties, one needs to know its Estructura y geometría molecular de Lewis. Averigüemos la estructura de Lewis del tetrafluoruro de xenón.
Para hacer la estructura de Lewis, necesitamos conocer los electrones de valencia de XeF4 para hacer su estructura y conocer la ubicación de los átomos en la molécula.
Contenido
XeF4 electrones de Valencia
En esta molécula, tenemos un átomo de Xenón y cuatro átomos de Flúor. Calcularemos los electrones de valencia de ambos átomos para determinar el número total de electrones de valencia de XeF4.
Electrones de valencia de Xenón = 8
Electrones de valencia de Flúor = 7 * 4 (como hay cuatro átomos de flúor, lo multiplicaremos por 4)
Número total de electrones de valencia de Xef4: 8 + 7*4
: 8 + 28
: 36
Por lo tanto, hay un total de 36 electrones de valencia en XeF4.
Estructura de Lewis XeF4
Ahora que conocemos los electrones de valencia del Tetrafluoruro de Xenón, le será más fácil dibujar su estructura de Lewis. Esta estructura de puntos de Lewis es una representación pictórica de electrones de valencia alrededor de átomos individuales en una molécula junto con el enlace que forma.
Los enlaces en la estructura se muestran mediante líneas, mientras que los electrones que no participan en la formación de enlaces se muestran como puntos. Los electrones que no forman ningún enlace se denominan electrones no enlazantes o pares de electrones solitarios.
Aquí, como el Xenón es el átomo menos electronegativo, lo colocaremos en el centro y todos los demás átomos de flúor a su alrededor de la siguiente manera:

Ahora que hemos colocado todos los átomos, mostraremos los enlaces entre cada átomo de flúor y Xenón. Cada enlace en la molécula ocupa dos electrones, y como hay cuatro enlaces simples en esta molécula, 8 electrones de las 36 son utilizados.
Comience a colocar el resto de los electrones de valencia alrededor de los átomos. Cada átomo de flúor tendrá seis electrones de valencia a su alrededor, ya que se usó un electrón para hacer el enlace.
Puede notar que ya hemos colocado 24 electrones de 28 alrededor de los átomos de flúor. Los electrones no enlazantes restantes o pares solitarios de electrones se colocarán en Xenón, ya que es una excepción a la regla de octetos.
Coloque estos dos pares de electrones no enlazantes en Xenón, y ahora tiene una estructura de Lewis donde hay dos pares solitarios de electrones en Xenón y seis electrones no enlazantes en cada átomo de flúor.
Hibridación XeF4
Los orbitales del átomo de xenón central se hibridan, lo que da lugar a la formación de nuevos orbitales hibridados. El xenón tiene seis electrones en sus orbitales 5p y dos electrones en orbitales 5s. No hay electrones en los orbitales d y f en el estado fundamental del Xenón. Pero cuando este átomo está en un estado excitado, dos electrones en los orbitales p se mueven a los orbitales d; como resultado, hay cuatro electrones no emparejados en total. De los cuales, dos están en orbitales p, y los otros dos electrones no emparejados están en orbitales d. Estos orbitales hibridados conducen a la hibridación sp3d2 en XeF4.
Geometría molecular XeF4
Es más fácil entender la geometría molecular de una molécula dada una vez que conocemos su estructura de Lewis. Como el xenón tiene dos pares solitarios de electrones, tomará una estructura que ayuda a estos pares solitarios a evitar las fuerzas de repulsión. Para mantener estas repulsiones al mínimo, los pares solitarios estarán en un plano perpendicular. Y como hay cuatro átomos de flúor, la molécula tendrá una disposición tal que su geometría molecular es cuadrada plana. El XeF4 tiene una geometría electrónica octaédrica, haciendo que la geometría molecular del Tetrafluoruro de xenón sea cuadrada y plana.

Ángulos de enlace XeF4
Los ángulos de enlace de F-Xe-F son de 90 grados, y los pares solitarios tienen ángulos de 180 grados. Los átomos de flúor se encuentran a 90 grados entre sí, lo que resulta en la distribución simétrica de los electrones en el plano de la molécula. Estos ángulos de enlace contribuyen a la formación de geometría molecular plana cuadrada.
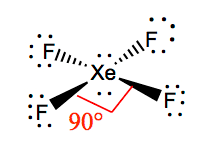
XeF4 Polaridad Es XeF4 Polar o no Polar?
Aunque los enlaces entre los átomos de xenón y flúor son polares, XeF4 es una molécula no polar. ¿Te preguntas cómo? Todos los enlaces Xe-F están en oposición entre sí, haciendo que la suma del momento dipolar sea cero. Como hay cuatro electrones en el átomo de xenón, que se localizan como pares de electrones no enlazantes. Como la disposición general de los átomos y electrones en la molécula es tal que la suma vectorial de los dipolos es cero, XeF4 es una molécula no polar.
Observaciones finales
El tetrafluoruro de xenón es una de esas moléculas relativamente fáciles de entender. Su estructura de Lewis es una de las menos complicadas, ya que todos los átomos de flúor están dispuestos en el patrón simétrico. Los pares solitarios en la molécula están ubicados en un plano perpendicular en forma octaédrica para mantener sus fuerzas repulsivas al mínimo.
Para resumir esta entrada de blog, podemos decir que XeF4 tiene 36 electrones de valencia. Tiene dos pares solitarios de electrones no enlazantes en el átomo central de Xenón. La molécula tiene geometría octaédrica de electrones y geometría molecular plana cuadrada. XeF4 es una molécula no polar y tiene hibridación sp3d2.